Белок переносчик эфиров холестерина
Содержание статьи
Белок, переносящий эфиры холестерина
Белок, переносящий эфиры холестерина (СЕТР), играет ключевую роль в метаболизме ЛП, способствуя обмену ТГ и эфиров холестерина (ЭХС) между частицами ЛП. Фермент осуществляет перенос ЭХС с ЛПВП на аполипопротеин В (ароВ)-содержащие ЛП, с последующим их захватом гепатоцитами и, таким образом, участвует в обратном транспорте ХС. При повышенном уровне ТГ и усиленном переносе ЭХС/ТГ СЕТР может индуцировать образование более мелких плотных частиц ЛПНП, отличающихся атерогенными свойствами, и снижение уровня ХС ЛПВП. Мутации гена CETP влияют на активность CETP и метаболизм ХС ЛПВП, имеют отношение к долгосрочному прогнозу и эффективности терапии статинами при ИБС. Профиль ЛП при СД характеризуется увеличением уровня ремнантных частиц ЛП, обогащенных ТГ, мелких плотных частиц ЛПНП и снижением уровня ХС ЛПВП. Эти условия способствуют усилению переноса ЭХС с ЛПВП. Тем не менее, сообщения об изменениях уровня СЕТР и его активности при СД противоречивы, что может быть связано с различиями в исходном уровне ТГ в исследованных популяциях.
F.V. Venrooij и соавторы изучали влияние двух распространенных типов полиморфизма гена СЕТР — TaqIВ и А-629С — на эффективность лечения аторвастатином у лиц с СД 2-го типа в рамках двойного слепого рандомизированного плацебо-контролируемого многоцентрового исследования DALI. В него вошли 217 мужчин и женщин, не состоявших в родстве, в возрасте 45-75 лет с CД 2-го типа, из них 84 % имели европейское происхождение. Аторвастатин применяли в дозах 10 и 80 мг в день. Частота аллелей (А-629С) гена СЕТР составила: 0,571 — для аллеля А (В1), 0,501 — для аллеля С (В2). Частота выявления генотипов в группах соответствовала распределению Харди-Вайнберга. Оба полиморфизма были в тесном, но неполном равновесном сцеплении — большинство носителей генотипа В1В1 имели также генотип СС. Как у мужчин, так и у женщин при генотипе В1В1 наблюдали более атерогенный липидный профиль — достоверно более низкий уровень ХС ЛПВП (соответственно (0,99±0,20) и (1,11±0,20) мМ/л, Р<0,01), достоверно выше содержание СЕТР ((2,62±0,81) и (2,05±0,40) мг/л, Р<0,001). У носителей генотипа В1В1 уровень ХС ЛПВП при лечении аторвастатином в дозах 80 и 10 мг повышался соответственно на 8,4 и 7,2 %. У лиц с генотипом В2В2 влияния терапии на уровень ХС ЛПНП не наблюдали. Снижение уровня ТГ после терапии аторвастатином было более выраженным у носителей генотипа В1В1 по сравнению с таковым у носителей генотипа В2В2 (при использовании аторвастатина в дозе 80 мг соответственно на 40 и 18 %; в дозе 10 мг — на 28 и 22 %). Для полиморфизма -А629С сходные результаты получены только при использовании аторвастатина в дозе 80 мг. У пациентов с генотипами В1В1 или СС наблюдали самое значительное дозозависимое снижение уровня СЕТР. Влияние аторвастатина на уровень ОХС и ХС ЛПНП не зависело от полиморфизма гена СЕТР.
В исследовании REGRESS изучали возможность правастатина замедлять прогрессирование атеросклероза у мужчин с симптоматической ИБС и ГХС. Пациенты в зависимости от генотипа СЕТР были разделены на три группы: В1В1, В2В2, В1В2. Частота выявления генотипа В2В2 составляла 16 %. Изначально у пациентов с генотипом В1В1 был более высокий уровень СЕТР и более низкий уровень ХС ЛПВП, чем у пациентов с генотипом В2В2. В группе плацебо у пациентов с генотипом В1В1 прогрессирование коронарного атеросклероза было максимальным, В1В2 занимали среднее положение, а у В2В2 отмечено минимальное прогрессирование атеросклероза. После терапии правастатином у пациентов с генотипом В1В1 или В1В2 прогрессирование атеросклероза было выражено в значительно меньше степени по сравнению с группой плацебо, а в группе В2В2 применение правастатина не оказывало ожидаемого эффекта (не установлено изменения среднего диаметра просвета венечной артерии).
D. Bercovich и соавторы исследовали влияние полиморфизма гена СЕТР на терапию флувастатином в дозе 40 мг в течение 20 нед у пациентов с семейной ГХС (n=76) [5]. Среднее снижение уровня ХС ЛПНП составило 21,5 %, ТГ — 8,3 %; повышение ХС ЛПВП — 13,4 %.
Аллель CETP-h23 и аллель MDR1-h4 гена множественной лекарственной устойчивости (MDR1) были связаны с повышением уровня ХС ЛПВП, CETP-H5 — со значительным снижением уровня ТГ и незначительным повышением ХС ЛПВП, в то время как аллель MDR1-h20 характеризовался снижением гиполипидемического ответа ТГ на статины. В мультивариантном регрессивном анализе показан независимый аддитивный эффект CETP-H5 и MDR1-h20 на степень снижения уровня TГ при терапии флувастатином.
S. Blankenberg и соавторы оценивали ассоциацию между полиморфизмом CETP и риском смертности при ИБС на фоне приема статинов. В исследование было включено 1211 пациентов, у 82 из которых был фатальный случай. У пациентов-носителей аллеля -629A отмечено значительное снижение активности CETP и повышение уровня ХС ЛПВП. Установлена существенная ассоциация между этим полиморфизмом и риском смерти. Смертность у гомозигот СС уменьшилась на 10,8 %, у гетерозигот СА — на 4,6 %, у гомозигот АА — на 4,0 % (Р<0,0001). Эта ассоциация не зависела от ХС ЛПВП и активности CETP. Клинический эффект терапии статинами был менее выражен у гомозигот СС. У пациентов с ИБС наличие аллеля CETP/-629A ассоциировалось с уменьшением смертности от сердечно-сосудистых причин, независимо от его влияния на метаболизм ХС ЛПВП и активность CETP. Таким образом, этот полиморфизм являлся предиктором выживаемости.
Источник
üäVìÃåmKعñbÚå6CöCNæîlZ ´øSX/§Ý³Ó6W×2ö´Å7sñÏ}áØÞ)²op{5mÌò4ÜOñçÿöSR3cÿóâ1o3^?%fyî§$ ã²1ûø¿u>Öý)£ßååÃ,OCÈFÆ7ÙÈ#5¢wr}ü@qõ©U]Íì]uÈ)r¨{Sqí:äÆqmW*G¥0õ¿qH°ºÆêKÓj¾âfBhÊEr¡¸N9c)ËD)ø¢wîÀäñõ p1â²@·¤ÄµIMJqÌ D#O 4©É` õ«%òOKûè;%ã[oýö½+ô5w,CïPRç!%cÇýóeWgÎñâg¥»iZR±«S_ø))|,Ô溷ÝÜÚ(ñϤøMJÕM±Êý¦ð«¶ÂMÆÎÖCò5rþiú EjS*Ø×ÇJþ9øx>.±|íM]ßÅxåà,;h¡×À
ßÕq/ä¡oð(~ï’æ86`7µù¡’Ó¶&Ãäá`º1tì×IÎI+´ CYöïݨçtÿ¦Ø64¯gYû)9Q·§,èR>aJ¬ÛÚ»3AY/³Ï{ñ-å7öHUV`~кiÓgÎ0ÚÙìÖ(1ëôí´»]·Rþ/Ôtc@T.èBWqs{Ii#(¡Ygå-óWæLN«¦. NiAéZñàñq
b~ÒÀþäûhUØCµë¹S¨éú¸R¢-tiû¸A|b°+°s
û×L1·M’¤ûO ¨Ìµ°ÆñÄÀ¾?:Y3Z;Ö6ä¹âÇ!íàÊ_.ÁlÆ®¶wLQÁ7B®a+t]}ƯJ~¦oWò3§f㧿òOƶ÷G>ô/*=FcÕg£Ù8¸B|ªr®è~üÁaòU$z¿³6#ËÁ ÂeØp9t4 ÎÅE)ý6H|:µ¨,q±ÑcA½B¹á}óĨîÎgAX9ÙËä$à=hkø¦X¡JçÚ·-^PNæ_@ÆâfM
Zù&¶³]uëì|Ü7Mv{Q×î ý8Mq¸Ö=u;B,ð1) ¦(øSÁ|O%Ùib~ê³¢wËfá Ùäãåã
ØÇú(ÓÿëjùTÈ.9ÆòÌtÀþ±û:ÄrðZQÂJ«wéÌøJ`îYN«Þ·1§rúüâijÓÿôv5X¯¦Ý³|ÌÓ>üàÕÄÏÞkKÎ×í¸ßÚJ]n§û|òjeø¼^¹b§aÇòá)%µOÙ³Á±ÙO)~},>Å_æ#Ý?ÅÕòòê)1ËÓp?%»XíxJÚºÚR½;djmÔÛ³
ùö.a¯üM1ËÓÐe/®þ({ýû6µõí4Ë~À©;7@DdMQèeJOE) ¡fòf»FM.
0$óðúj+9ßq)åRsÖ5W¿µ(ô>;ºuÁíFÃs²f×Xá c{D2tÅAm³ÂÄ£QácÈcyú>Ö®9ôT¸~²T%wíðÂ,ÈP-1ã z,ZMa+Á|ý¶x¼óq ÐñòNx¨Ü&ñ+
£éø.:(vËàÈk:@PÎøÝwk¼®x-,].0¡Yìk îv¸®x@ð»6n
G±»_*y¾ 8ã®b(cÿ> Aâ’~±B
£ãÁ)ñLÝ1GqÕSdHßuS>X dF;®üßpûuá¼^)ø/#.Ù¥3^¥ªánÖ½ÕÀÇëÎ=t³}¹9Ä{Êöñ»÷ÖÌÏðM-Ërý~~¦¥§¸
Ϊk¾à¸ !t0%l’X¾t³ÐvÒ¥§cf¨pnù|Z¿èG¤à¬$ýñÑÎT]_c
&¯Ø2äÞ’û:æwò|½³ëÏñ⢠(,àÍ´û±´|WÉëÜNÏiÓ
ÂAÇlné~Õ?±ÊK³T.ÒEjYÚÍV·}Q&ãN©ñUóÆ_zIaT];xG
Å
Ãw8éÕß>L’Çp¾úê)^ÕoßR’Ý x0¦iS¥ñ§>qò)+djl½¥;t±Ë$8eÅ
á’£ôvXÎ%`ÁRõÊ>6¢x¹LÞQA| 9fó,¾B+}V0$I’ä&ÁKË7ìãX°N`
QÁÓøÎ(P|Ïhw¦ÒU=|[Äý$ñ1¢à«ªq«Á·Ï[¬FìqTyÞ鳧2dµ¤É¼H(þ©ÎuEóXÑ
Û»Cw.Ôï²»Â:3mk_M+cøß.J½Å÷¤a’ù+~Ýgìé{×Õï>¯HÃyÇ:ý7æ¿VüäJd(tná
cÌ.êÏq¡Ä±ØÔ7[gØ?fhLFHÁº!àSIG«À]ÿ¬PfIäë»SÆæHòu¥àaGÒå´éÀ»|Yp4¶UÂEÅJö¿Í=îë°á¾Ùcî
IÖÀJN¸HIiCïÎ÷ UáÍÂñdÀÂMézGß$ÊKKgôÇßþ>J~)°cBÐøVàw¼®±äªè¸ÃRåfpÉHþk0ú#OØ[6
A ®¡8ñE£Rä÷ôíîýô Xé%¡çÅÇì~ìò¢’¸@Ắש ø)Á’Säk2䡹R²ØGq8!(2o ç
~Mõ}B×±Ãàð¸*|ÙÓÿ>áLn×±øÖ>6EqÇbHç3, ×S¥Û§ |ðL¸µÿ¦RÑà»LjðZè» ×ÂgÙ¥nYäµQB£^Î-PGµÐtÖTð®VÚoñvÛM¿²Éâ¯
IFMí2Jø)Ããææ¡å¬S_äÞ[ò= ënŹ·kÍñ\ñßìÁvùR°æÁè05(
%^îP´ë
ç 4ºn|, RãYÓªÐ%¾³ríAI ú Ð@oFç·ì9vÒûN^ÄÎHQ
ÿÍÀ¹àòp
z¯T¿&¤XL×__).bRæá8[²®Nû;3+êbo(èQS¸2A8qá7þÕ° ÷myË.~õ]ÌoH©Ð¡·ËW2;ëÝûØJB|àò>ÅW»X»²ì9Eü¥3ÏëA{¯Ää¶Êøí
-üWEÉSüHÏ÷Æ×`Dc¹f±ÍÄÔ÷]ïl÷XÀ3gÂ!³
CÛÚ¦ ÃêVÀe(
¹wK^^¹ZÃU·
Q]ò.üîØIxÝ¥bÈéî,eÁ´ïÓyxÝå+$tÏö¶6efQ¤b g¡ØùÅ%õAÅǵÐúâÅ(¬Jhç¯%e»Ú)Pa±rè@ãIoÒCw]n9.Å°sN¡K»5:®yÑѵ÷º±;̧%à®àÊ ±G¡Å«8%®=¸»¨M¹OÑEÁß®JEü2f lÿÂx1
ý,¹íg’¬Ø{¸åôåSXHÎ 4,l51~öóõhñà̱àè?®’¶@¿7¶¾ï&çf¡6¨Ã7(.8LãZæ
ï´å5ì!,Z
oÆ!$e¿qeÀí2¦ÀüÔP£²0KL®¬4[¡ìòà+nI½.(1µø6rx1)>LZ=N,(PfuÅ7Âx2>#7Ï9&pJMbØ[nmëA
Üàÿ;¤X¬5aDT³`Ú
X
,Qê*§Z
n¢UØÎY
@T¿]ÇCxI- ú¯X,ä8p
8ª·£I)rkÉÚܳºªóÏÇ,88¤þëº
Æ0èoÎà-L¥øtÁQäµkUÖóLì¸åøÀ¸¾à
/( åÁ+äí~>uIa¥N¾Ĭ@~óÉ-ÜÞ¡ì®ªÌ ØfRÝ××+8YZnh¶Ä½ôÐu§Prpíâ5#³bSïßöóékFU,a
P´+çIØ@ø¸ ê« ;?Dìlp?Kè&OûÎñièïf:4 3
¡T
Úåbéûõ³Fp䶲W/EaåªHúé$¯)ôWö׿Ðåx¤ëLFICPø~ÞÂ.RZ 8BÇ{g¸’fëLáò£óïäg_n´L Ã`+Ì.ûZá3e¡2VhAK ÔkÓm³²ÊHá ÎBæ8wr8eFâ²ÁÇ4§vâªé[Ýc¬5Ñp ÖÏ|.²©ÈÆ?BaûЧâCÓ.g2I¡W IÍPuë¥id±-b²FÄ^2c+´2néûο¢ø÷>Ih©p¿ðÎÂÜÖÙV,Ð0® ç»°NêXbk{ÕËC|}áóÀï#Cc
µôøcqðHa
ÄJ’ÞýNé4¨Añuù!¢ËX¡=/,M¸ËUá_X6#XF¡Ï±Ur ¡1稲¯Kuà¶$î^Á|PLCVÐèÒ²/*¢ò¢°cFÀ(ÇOèÐñq3_OÆÊVÄ830~
Á%EÉÌ7Fâ¤Ði³
hÒ)
ý¤L
~ã°ZÊDߪÐCTpmt-¤ì¢¯,#PagäoÕsÑkpX Ó8×½
X¢ ìëºÎ!¹*ò2Yxsʶ$¥s@hEUüQD|ØátdÝ%§$of}àåï/ÁÓ
,Âù #bfËYKF§X65(£ç
ÈßÑò92Ø&èÖôø±(úÆ.Àm-ñãÒór,ébäàCÀUTtBòµ¢°u!üÃÇY¹8
þkqðBsàݳ2~>ñ¿[BùÍ
07¼[=ÿôtj¯-¬Î¦¯CíÙ)é2ö³*Æ&¶B¼D¨¤cBf«ýdD¤Ùha³¤mç¿’]0q4aSÕ®Lâ ¼û#óÿ,Jy+ k¾éañ15øxJjS9ÉEqMáxÆØw9#ÒOMú£®I»ÜÐ/êLf±J±â¼ùÐñ;S!r¦ÈÆǯÂSàÀX(z¥3ü©À¼
ÉáçÀ¼S¢$U]©¹é^µÕ4öc¡Ä0Ï6óøAh¢ûéw£â»ó6ÅÇL1Àe@òÖªÁ§|ÿ¬ø
h+e1×Ç30ee
R^©ÇxÄ%Q1Þ3ËÃÇÖ%èA£ñ’®s>pbá4>mP8¦KfÇ#¢#kôOòýLàqÑÂ-gÒíºÅ5>wÍ2
×Üû¾¤
Ë7
«8ª ËHÀ.·Íÿp×2´#XÀO~Aö¼kq¶· üm¼$mçwUóF¾MY
@²ÿ3áJFÓ«ÁG¨îðÞy}]©ÞR¥àÄ|¯Pià$Æ4
._8æJ ØÒ>yYô¾íú+b³N2 úeêL¹LÄpÆ
VdcÈ7/6úÔèͤ¤]]Þ ØΰTR3ÙY)Ë¿Í÷³µë±4
Áða¿ã
=¨ãß5ôhUJWèÇ)C7Q!vãü0¹ÙþÔprá?÷-$N¼½YH~t9#úðÒtå#? ®l`=8-¤;¢ÉË,’Äc Íp`q]%_õªUL¨lMßÑÿÄ´É¥=ïr!ÇWÀ=1Xã;á±.`’ÆM¢p¤¢
˺ÿ ´¾)ó¤lcên¶n[ÜòûåëGþè~ιà}¡!°7¤¡5ê§@¡ÀÊ:Ø
¬´|ª«of+²ê+oP´f4Ç7Éàtª;Zq#Ô)?tO2v;³!AÓèʬRª,
c
W2]/NiAiòMg0¸+äe¸JÔnà½c¸Íºõ(hàÉ
ÇÊd¦ßÊ /Ô¬Ìæ¢WNsÄJLYd¶
£l1äÀ1I
¸ßi[2)óáP» ~`Iq§àJËEú6ýÐÆTdSt&lbQKQhÜܨ¥çÀßØàáëÍP-«e{ýI¦ 7QÖ0è5°øòqI,ãõ°dø¬
ÃSE!:Ý-øÎQÁy°=±mÕds¹+BûîKÐà`¯; ?Ö» HaÞHÌ}ÿæÇXé0`Â
axãäÖöÉ»©Añ-1$ç0/¾3wÛÉ|LÕëE Ù¤[Ë`(H¼SºRaÀ?Ìð¬Ò7bÐ2¡©4P-5òÀ$_ômz@ ¡kòmêj%Wk^ZkÊ/íóÈ#e óί(¨ûQh0i©ÑJjÐÀþ³ê ºß
J%é°fFø´ü
-Ñ)þVK
,ÄK}jð¸:Î1L2bñpyñ^£Ê»3iÑd`fÊÐÒȺ&j1»}Sù³¡Ð¤’KïÛo(oN²¶íÃ=»ñåñMW
~`Ò?÷íåëz$¡ÂÂLøwbý2íçãÑÇF(Ç]ÖÁ×)ä°tL4ûZº
¹îÁ9ÜDF?7ÁöSU% 3©3;%Ç7″
ãcãy«>ò×bpC¤$±iÊUgÐÃý ÓQq׿dÀèÃ=e+ÐHÄéðtÓÿcFñóB µ#jÂ2Âã±1¸»ÐL)¥ZÈòÉzúÊ(µÉ%aÀåÎHqþ
|¾ÚÁpÀ$cãï5j9 a:ØÇ+¡óðù_Qu@¨a)8üþ&ì¶1úPJgÔÈTàYBû4¸;Çt¯´¤ØkEºbÍ^v¯j@åä)â7- ]´èvjHffµánÄ)2$ÙKÜÄæïûÛ¼ ø±ðÊÕÃRx,ßÁl ¤ïç0G¦´?Ñv³XÕ¸Çgö|çæPMq1:@HÛ0u-,x{(¥cX
f(¬ÜAgMcÈpTÚqF É{ÏS@öI]X (9-Ôánmצ14J¹ÄÉ«`^Û°DoZà!ÎcëråCÀé×C°Õ¼ó0ÎÇBS>q'(ù1Ò*ÅhdeÐô·3$(Kz#ÊiõI(cä
·3ç¹}ìW/¨>M¨i*Há«LÐ1Ã^eRÈQ374ÑkFå 5`j&ô¬’Í´ß½v=¶)W=yE¦ÁqJð#6©¯4èJlà¢uXU>Û5Ù«ùàPüëÁ÷Ë5ÑcÌ
Y_#ÿ²â®/¦Á:ä÷¥à=c
ß,¤/!ØR E[ª`½¢ð
t5¹#ZØ>i6e²Vé£1Â%ÇVí>»¹ô
ýóù6¡Æààøà p_ºR&Ê)QLTâò/kÈw’ âñxN¨üÉnjx2Hñ’îÔ;]ó×ÁqBl0Ï8Å%MÜ.Ü))MeU}~£»«æ|EÖéûru¤KúíC· ¥´4ðïÞ3l,9m(Rl§Ð»¼â.L¢ òУÊЯ¬KÎÁÁFXB½p°Ñ˦R´Ün3røÐ&ÃÌ
ãú$e_éÈ[ó+´*·[@²R¹
©&£IK?ÞÔãÒ/Ð
.ä´w®E{ûÀÝæÓÍ»½-®ûlå °úÄIO·¸è)ñ^LÌ(¢ÜABy±4É¥üt-ìiC½¾¯ðºy/ã,[SF»¤Ò¿’ëæjT5«ß¡kÉÅ4,?FÉ*ÝQÛ5.w¢¼;©*¶¼¤Ù»pÉËÔ6åÓr|}5TsQ.cÂd3î°©!ÍÙ0;Þeõ²0*+jXXÀ.3Õʲ ZgýòÌÌ7ÏÇøS.HE¹Mð’¹KÓ`ıà$é±.Åð®½9á+§íïSÞX°T*D^ÆÊÎ P̧xÕ2fòh/3(8L`KeïÂVÄ`ËK걿ª¡QXxd§Jà)[ûV:»Õi)
jDÎúLBØÁ`
3)Kbä&!ª^ËZåûÈÔ Ç9ÆàXS*5Nc÷ñ|~¿ ÀS°JñJ’ÊÈÓK÷:ÆÈéÃÁtsk5¢@U:¼ò°*ltü¨Èèïf( Ô¸ÅÚ(ÃYâm)$aØ&m=°IÊ.ÓZ°»:dúO)ÜgýÍ$G3Wk¸M_âjH|N4°n[óò˳Jý±Vf×.~%çVQå,PwHÜ:È^®Oe[¶© Ϫ´¦
;¢ô)ÕéÓ
£- ¦>ç#µKþB+¥¯cbüeÅ/z%z Éq4¶òÿÙgIþtZШÛä¼ h×q¼Ìó¥ÑF8°K’
,j7».>.°¦í4íÈxÀì=Â)u§ äCSJ
¬_(Ê $$yêSΤ¸1Jô6PädVÒÓíðÓfåFäIJ8è2Våå£pSîPaJÈDk;RΪ
&ïËX2FMÉ·YwÞ}EùY)ÏÎLQxÑP,Å¥Z ý¡/jÀúöa¬UÕpç=ú¥J=*
1È&,wªüÕÅmÈ°Ó
㶠Êü( Àc8SgsRÓ.ñ§Áí={0
º¦êd|ÂÒAª»|2!YñÅ)@)¼¦
ª±9g²Þà#àA×mIqDa ô&y³`è©H¤ÁÉà¸@x®Vv|ÜeG> Ò0/2B=@=ÚÛS4cá¯6zx1TÑwPqh,7»iá»In°
àÃföz§2ht&ÒS¹¾èÊ[ÇTjúrêØ-I¼Ú8îS|èçëÎOªR
WÀÉÌ°ßw*ê¥Òf{SÕúdÚÕ¤(4* Ì
æð7ë@àCÆ|ÊT#Æ^fFdÛåøóÒºqy9n¼óg°´)õÔB¹=5ó ÿÞ«GÊ5-5t&¸ßåSºÂ÷MyEùæÔEJCQu)NH/RzG$XâpzkHj¼0ïÁDk¸¼ÄýªN´õÑÖ£H³*~¡fBe$ ¾cÛULdFàHkh#+êÀbУ/Î.cnÁA¡nf¬»* (½Pe7þº(qJ¡Ì(TZ
Ñ·yÊTY/r[eD)é¤É¦ª¼ú¡E¡AVf¥·0ÃM$TN¬FÃFkYÓ{T©6,NÁðÃ~ö»T)¸M3,èîZJCâÄì
ªÈüûãbÊ(øÐ>»®ã «$¤ ì`ä0q+9Aæaö¶ýe¿ _Íê,»i#Joàî¯ÀTé
d+·O6UzP½& [ÍY eÂ&bG´pkDt2á+nÐÖ?ãFl¡°ëAEucùÚ¢÷¢ØÐWiªEײîñJH®JÔòÙôG,ùÞ#²Ñ$æBZÖ£P9üJº×!LjC^oÉPWD1²b$È*kUckxQyeõP]|éWð
ü°O¬
Ñe¯ÊÞKK]’¶JNʲì2NJn0æ#ÑHÀ_ JÝ»ª4÷ZdÏGõȬk3ÅpteÊ¥(3igÀéhOfT»b£·eZÑÒ.M6((ÛÎÇ)Æã.ÇÜ)½®e`ÛjËg@ñ®q×>qèm-¾@èpÕõ&UE8s©^r®±ÂB/*â9xߢð£±#TÂ5´§IÏgÁدÊXÕܶt:Â)qÌ)r§È`äW/eáÙèúufNµæû>Skcß3¬oDrÎ1}ߪ¸:S@îâJSIZJ¬°põ°ò>BÁÆ6úvPÈãzø
ØPý6DS~?#bÌd Õ®Y# u¨8ʪyy_Áê29;®bû2z2(
Zƪի (ÓFk×½ÑçIhQ-Kò»¤t^È,PËõLáÞ ¤S¾×TcÆÇßO/þò
jÑÒ%3½ï²àqu×MMÑ©$¢ûÅ{ý6Í+ÊW$eÕϨSùç÷ý®yÀ$Ëy¢Iñ.(+;[Evd^%Lp{Än¿ç*CfÀÊñ|»$°âÊÁzæ}
O«Òý÷ä8B¤8âm*1gZÈ´¢G»SæêÃßÉSØtUp}ôì)úL²¥4´¤pØ÷UðA`°Î@iªäæ²àw A>$jåÐå+^U
.6¢xfßú²O>
MÝê1³8*@ľJפ{þKÒ¡Ù85ê¶FuVk^ÑÆ#¯ ÒÏæ³Yãöê¯(`²Ô¢´)yÿ¸ßÌgw S¨{møòÌèjfÌÊ×/·’Å7
äÒ°jV=Æó/ð»ï÷U|>K0 ØÃ`Ê~´,% YJvµª_-9õnÏaÀ°ÿ,×Xâ±»û.ðö³mÀ¿µèâ§ÞoTµP¾PoGÏȧH;Qî*n ¦ê#²ßÐdª0E^gL:YÒØs¡Ðmp#+¨»NE)uÕ»F5Ù ßüþºBT3äápûy:@R³y ÂkF >» ·+¯k¨õ9·`ag`²P+ÄüåRR ù²3³ìLÄÈou«í Ò5JüÙF§©ëÏ·VEÛ Àb½Ãq$_ËêYUOÿÕ:VkÑK`ûÍK 7fÃgAábýÇÂó¹Ãõä4f×È&àoPXͪ(3â©Y¨F°z$¸1fM¯wÕÝj§ÆåZDäû±×@
@ (ªÔ8rt½cÒQe¶¨Á,÷Ú®IĤ#5*:q²ñ.!túð®U^3¤ô!oÎeÜTóW¿ø|bÏïgbAÝÉ¡°öng*Z*HÅFº¥í³cUsø,íZ·ðætÞËSNhàÿ)ôÖZÌHqª»M¢=î¬àÙq¹§ÓÇx;Ðr>ÄX çØ>¦À!+1SÔOße*,H*¨KI¦L1uÕ¢ï7`Æa5ÕïÒUH®è¸^²æ59²äÿJOï1VÐöÈË)üÄE2ç(KÌä¬o1×°ßwÔrWÆ6Lp^©oº´ûn±·`á]lKEÛYö!~üQI
þÞãM)¤¼ìèWë
2(J!UÉg#B’,ìSDJêó1R¢!çRYÚ¶-À¡J-Ë4½©e¶TD8lEÌËÜ’õ°M`O&Ø¿§*Me°ÿweú¬2v%S¢YD¶Ã
¾
Источник
Холестерол используется как переносчик полиненасыщенных жирных кислот
Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.
Липопротеины высокой плотности
Общая характеристика
- образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника,
- в составе частицы примерно половину занимают белки, еще четверть фосфолипиды, остальное холестерин и ТАГ (50% белка, 25% ФЛ, 13% эфиров ХС и 5% свободного ХС, 7% ТАГ),
- структурным апобелком является апо А1, также содержат апоЕ и апоСII.
Функция
- Транспорт свободного ХС от тканей к печени.
- Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.
Метаболизм
1. Синтезированные в печени частицы (насцентные или первичные ЛПВП) содержат в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в ЛПВП по мере метаболизма в плазме крови.
Новосинтезированные ЛПВП выглядят на электронных микрофотографиях как двухслойные диски из двух монослоев фосфолипидов (таблеткообразная форма). Синтез апоЕ и апоС происходит главным образом в печени, в отличие от апо А-I, образующегося как в печени, так и в тонком кишечнике.
2-3. В плазме крови насцентный ЛПВП сначала превращается в ЛПВП3 (условно его можно назвать «зрелый»). В этом превращении главным является то, что ЛПВП
- забирает от клеточных мембран свободный холестерин при непосредственном контакте или при участии специфических транспортных белков,
- взаимодействуя с мембранами клеток, отдает им часть фосфолипидов из своей оболочки, доставляя таким образом полиеновые жирные кислоты в клетки,
- тесно взаимодействует с ЛПНП и ЛПОНП, получая от них свободный холестерин. В обмен ЛПВП3 отдают эфиры ХС, образованные благодаря переносу жирной кислоты от фосфатидилхолина (ФХ) на холестерин (ЛХАТ-реакция, см п.4).
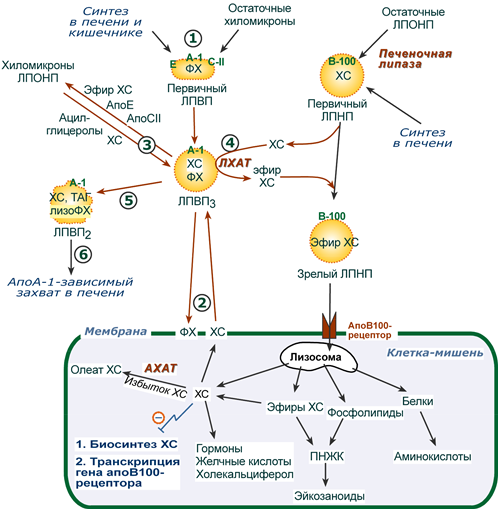
Транспорт холестерола и его эфиров в организме
(цифры соответствуют пунктам метаболизма ЛПВП по тексту)
4. Внутри ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от 2-го положения фосфатидилхолина (из оболочки самого ЛПВП) на получаемый свободный холестерин с образованием лизофосфатидилхолина (лизоФХ) и эфиров ХС. ЛизоФХ остается внутри ЛПВП, эфир холестерина отправляется в ЛПНП.
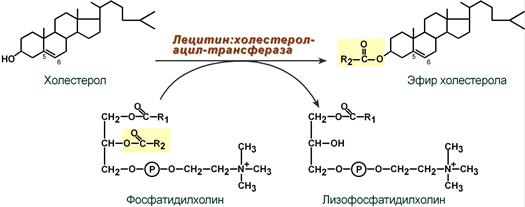
Реакция этерификации холестерола
при участии лецитин:холестерол-ацилтрансферазы
5. В результате первичный ЛПВП постепенно, через зрелую форму ЛПВП3, преобразуется в ЛПВП2 (остаточный, ремнантный). При этом происходят и дополнительные события:
- взаимодействуя с разными формами ЛПОНП и ХМ, ЛПВП получают ацил-глицеролы (МАГ, ДАГ, ТАГ), и обмениваются холестерином и его эфирами,
- ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм.
Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются.
6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается.
Липопротеины низкой плотности
Общая характеристика
- образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП,
- в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов),
- основным апобелком является апоВ-100,
- нормальное содержание в крови 3,2-4,5 г/л,
- самые атерогенные.
Функция
1. Транспорт холестерола в клетки, использующих его
- для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников),
- для превращения в холекальциферол (кожа),
- для образования желчных кислот (печень),
- для выведения в составе желчи (печень).
2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.
Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола.
Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.
Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения.
Также в мембраны всех клеток, как сказано выше (см «Метаболизм ЛПВП»), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП.
Метаболизм
1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и «выталкивание» белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый.
2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами.
3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
- ХС превращается в гормоны или включается в состав мембран,
- излишки мембранного ХС удаляются с помощью ЛПВП,
- принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов.
- при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция),
Синтез олеата холестерола при участии
ацил-SKoA-холестерол-ацилтрансферазы
На количество апоВ-100-рецепторов влияют гормоны:
- инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов,
- глюкокортикоиды уменьшают их количество.
Источник