Целевой уровень холестерина при стенокардии
Содержание статьи
Достижение целевого уровня холестерина липопротеинов низкой плотности: современные возможности
В обзоре приводится анализ основных характеристик, клинической эффективности и безопасности фиксированных комбинаций современных липидснижающих препаратов, показаны перспективы комбинированной терапии с использованием эзетимиба
Целевые уровни ХС-ЛНП в современных рекомендациях
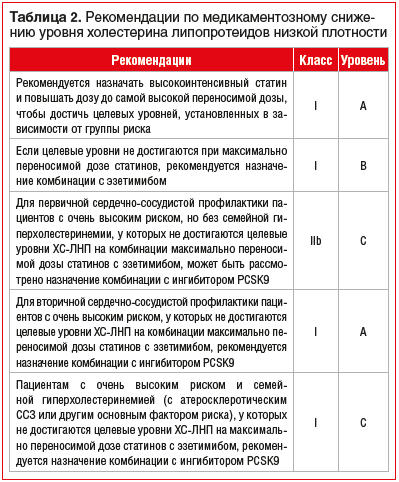
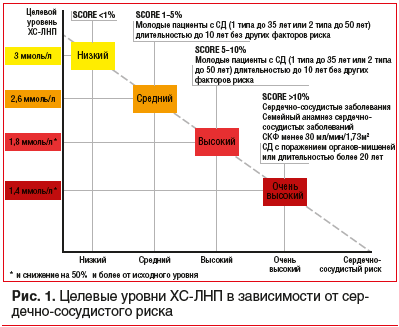
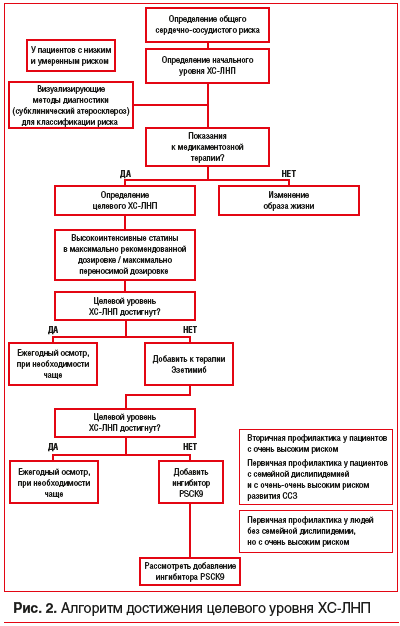
Сердечно-сосудистые заболевания (ССЗ) занимают первое место среди причин заболеваемости и смертности во всем мире [1]. Снижение уровня холестерина липопротеинов низкой плотности (ХС-ЛНП) с использованием ингибиторов ГМГ-КоА-редуктазы — краеугольный камень первичной и вторичной профилактики неблагоприятных сердечно-сосудистых исходов [2–8]. Согласно рекомендациям Европейского общества кардиологов 2019 г. пациентам с дислипидемией рекомендуется назначать высокоинтенсивный статин (например, аторвастатин или розувастатин), обеспечивающий необходимое снижение уровня ХС-ЛНП, и повышать дозу до максимальной переносимой, чтобы достичь целевых уровней ХС-ЛНП, установленных в зависимости от группы риска (табл. 1, 2). Целевые уровни ХС-ЛНП в зависимости от сердечно-сосудистого риска и алгоритм их достижения представлены на рисунках 1 и 2. У части пациентов, несмотря на использование высоких доз даже высокоинтенсивных статинов, не удается достичь целевых уровней ХС-ЛНП на фоне монотерапии. Даже при доказанности тезиса «чем ниже уровень ХС-ЛНП, тем ниже риск сердечно-сосудистой заболеваемости и смертности», несмотря на наличие четких клинических рекомендаций, показатели достижения целевого ХС-ЛНП среди пациентов, принимающих статины, составляют 33,7%, при этом у тех, кто получает статины для вторичной профилактики, — 58% [10], и им требуется комбинированная терапия с применением эзетимиба [11–15]. Прием фиксированной комбинации статина и эзетимиба повышает эффективность каждого препарата из пары (за счет синергического эффекта), увеличивает приверженность терапии и в некоторых случаях может быть более выгодным для пациента в экономическом отношении [16]. Целью данного обзора является анализ основных характеристик, клинической эффективности и безопасности фиксированных комбинаций современных липидснижающих препаратов для повышения возможности достижения целевого уровня ХС-ЛНП в соответствии с современными рекомендациями.

Симвастатин и эзетимиб
Первой фиксированной комбинацией статина и эзетимиба стала комбинация на основе симвастатина. Симвастатин 10–40 мг/сут снижает уровень ХС-ЛНП на 18–41% меньше, чем аторвастатин или розувастатин [17], что ограничивает его использование в случаях, когда требуется достижение современных целевых значений ХС-ЛНП. Биодоступность симвастатина составляет около 5%, время полувыведения — примерно 1–3 ч [18]. В целом препарат хорошо переносится, повышение уровня печеночных трансаминаз встречается у 1% пациентов [19].
Эзетимиб снижает уровень ХС-ЛНП, блокируя всасывание холестерина в тонком кишечнике и усиливая выделение холестерина с желчью. Множество исследований неоднократно демонстрировали синергический эффект назначения препаратов из класса статинов и эзетимиба [22–24].
Эффективность терапии эзетимибом и симвастатином была показана в рандомизированном двойном слепом плацебо-контролируемом исследовании IMProved Reduction of Outcomes: Vytorin Efficacy International Trial (IMPROVE-IT). Дизайн исследования был основан на сравнении монотерапии симвастатином (40 мг) и комбинированной терапии симвастатином и эзетимибом (40+10 мг) у пациентов после перенесенного инфаркта миокарда. В группе комбинированной терапии достигнутый уровень ХС-ЛНП был достоверно ниже (53,7 мг/дл против 69,5 мг/дл в группе монотерапии). Также было продемонстрировано уменьшение числа инфарктов и инсультов в группе комбинированной терапии (р<0,05) [25]. Интересны также результаты исследования 2017 г., которые показали, что протективный эффект комбинированной терапии был выше в группе с СКФ менее 45 мл/мин/1,73м2 [26].
Одновременный прием симвастатина и эзетимиба не увеличивал риск развития побочных эффектов статинов — миопатии и повышения уровня печеночных трансаминаз [27]. Более того, было показано, что комбинированный прием не увеличивает риск развития сахарного диабета 2 типа, что иногда наблюдается при терапии статинами в высоких дозах [28, 29].
Аторвастатин и эзетимиб
Аторвастатин в дозе 10–80 мг/сут снижает уровень ХС-ЛНП на 37–51%, уменьшает риск развития сердечно-сосудистых и цереброваскулярных осложнений, продемонстрировал свою эффективность при проведении как первичной, так и вторичной профилактики в серии клинических исследований и метаанализов [30].
Метаанализ, включивший 17 исследований, показал, что комбинированная терапия аторвастатином и эзетимибом снижает уровень ХС-ЛНП и триглицеридов и повышает уровень ХС-ЛВП (р<0,05) [31]. Комбинированная терапия продемонстрировала уменьшение атеросклероза коронарных артерий, по данным внутрисосудистого ультразвука, в сравнении с монотерапией аторвастатином [32]. Исследования показали сопоставимую частоту нежелательных реакций при комбинированной терапии аторвастатином и эзетимибом и монотерапии аторвастатином или эзетимибом, с единичными случаями повышения уровня печеночных трансаминаз, развитием миопатии или раздражением кишечника [33].
Розувастатин и эзетимиб
Розувастатин в дозе 5–40 мг/сут снижает уровень ХС-ЛНП на 46–55%, среднее снижение уровня холестерина и ХС-ЛНП — выше, чем у других препаратов из этой группы в эквивалентной дозировке. Биодоступность розувастатина составляет 20% (сопоставима с биодоступностью аторвастатина), время полувыведения — 19 ч. Большая часть препарата выделяется с желчью (72%), оставшаяся часть — с мочой. Препарат не метаболизируется системой цитохромов печени, в связи с этим практически не взаимодействует с другими препаратами. Такие побочные эффекты, как миопатия и рабдомиолиз встречаются редко (менее 0,1% и менее 0,01% соответственно) [19].
Эффективность и безопасность розувастатина были продемонстрированы в исследовании The Justification for the Use of statins in Prevention: an International Trial Evaluating Rosuvastatin (JUPITER) trial [33]. Назначение розувастатина снижало риск развития инфаркта, инсульта, уменьшало необходимость в реваскуляризации и госпитализации по поводу нестабильной стенокардии, а также риск смерти от всех причин на 44% по сравнению с плацебо (р<0,00001). Результаты исследования HOPE-3 (Heart Outcomes Prevention Evaluation 3) показали, что терапия розувастатином в сравнении с плацебо снижала риск развития сердечно-сосудистых осложнений у пациентов из группы со средним риском, в то время как только антигипертензивная терапия (кандесартаном) в сравнении с плацебо не приводила к снижению риска [35]. По сравнению с симвастатином и аторвастатином использование розувастатина уже в дозе 10 мг превосходит симвастатин в максимальной дозе 40 мг и эквивалентно применению аторвастатина 40 мг по способности снижать уровень ХС-ЛНП [1].
Эффективность комбинации розувастатина c эзетимибом была продемонстрирована в исследовании, включавшем 469 пациентов с высоким риском ССЗ, которые в течение 6 нед. получали либо монотерапию розувастатином (40 мг), либо комбинированную терапию розувастатином и эзетимибом (40+10 мг). Комбинированная терапия показала снижение уровня ХС-ЛНП на дополнительные 12% в сравнении с монотерапией (-69,8% против -57,1%). Более того, пациенты в группе комбинированной терапии чаще достигали целевого уровня ХС-ЛНП. Так, например, в группе с очень высоким риском 79,6% участников достигли целевых цифр (ХС-ЛНП менее 70 мг/дл), в то время как в группе монотерапии это удалось только в 35% случаев [36].
Безопасность и эффективность приема комбинированного препарата (эзетимиб 10 мг и розувастатин в дозе 5, 10 или 20 мг) были продемонстрированы в исследовании The Multiceneter Randomized Study of Rosuvastatin and Ezetimibe (MRS-ROSE). В ходе исследования сравнивалась эффективность комбинированного препарата с эффективностью монотерапии розувастатином в течение 8 нед. В зависимости от дозы розувастатина в комбинированном препарате уровень ХС-ЛНП снижался на 56–63%, что превышало эффективность монотерапии розувастатином в той же дозировке. Кроме того, у пациентов с сахарным диабетом или метаболическим синдромом отмечалось более значимое снижение уровня ХС-ЛНП, триглицеридов и общего холестерина среди получавших терапию комбинированным препаратом [37].
Исследование The Ildong Rosuvastatin & Ezetimibe for Hypercholestelomia (I-ROSETTE) показало, что безопасность и переносимость комбинированной терапии были сопоставимы с таковыми при монотерапии розувастатином [38].
Более высокая эффективность и благоприятный профиль безопасности комбинированной терапии розувастатином и эзетимибом по сравнению с увеличением дозы розувастатина были показаны в многоцентровом рандомизированном двойном слепом исследовании, проведенном в странах Северной и Южной Америки и Европы. 440 участников исследования были разделены на 2 параллельные группы (в зависимости от дозировки розувастатина), каждая из которых, в свою очередь, также разделялась на 2 группы: прием комбинированного препарата или увеличение дозы розувастатина (с 5 до 10 мг или с 10 до 20 мг, а в комбинированной терапии доза статина оставалась прежней). Целевого уровня ХС-ЛНП от 70 до 100 мг/дл достигли 59,4% пациентов, получавших комбинированную терапию, и только 30,9% при увеличении дозы розувастатина [39].
В январе 2019 г. в России зарегистрирован первый препарат фиксированной комбинации розувастатина и эзетимиба Розулип® Плюс. Препарат Розулип® Плюс показан в дополнение к диете пациентам с первичной гиперхолестеринемией (за исключением гетерозиготной семейной гиперхолестеринемии). Розулип® Плюс назначается в качестве заместительной терапии пациентам, липидный профиль которых адекватно контролировался одновременным применением отдельных препаратов розувастатина и эзетимиба в дозах, эквивалентных соответствующим дозам в фиксированной комбинации.
Перспективы комбинированной терапии с использованием эзетимиба
Бемпедоевая кислота — это липидснижающий препарат нового поколения, который способен снизить уровень ХС-ЛНП на 40%. Бемпедоевая кислота — это пролекарство, которое в печени превращается в бемпедоевый ацетил-коэнзим А, являющийся ингибитором фермента АТФ-цитрат липазы. В соответствии со своим механизмом действия этот препарат не только снижает уровень ХС-ЛНП, но и блокирует синтез жирных кислот [40–42].
Кoмбинация бемпедоевой кислоты (120 или 180 мг/сут) и эзетимиба (10 мг/сут) у пациентов с непереносимостью статинов и у тех, кто мог получать терапию статинами, привела к снижению уровня ХС-ЛНП на 43,1% и 47,7% соответственно в зависимости от дозировки препарата. Монотерапия бемпедоевой кислотой снижает уровень ХС-ЛНП на 27,5% и 30,1% (соответственно указанной дозе) и хорошо переносится [43]. В клиническом исследовании III фазы добавление этого препарата к терапии статинами и эзетимибом у пациентов с высоким и очень высоким риском развития ССЗ снижало уровень ХС-ЛНП на 28%, а риск развития ССЗ — на 33% [44]. Комбинация бемпедоевой кислоты и эзетимиба продолжает исследоваться как перспективная комбинация.
Заключение
Эзетимиб часто используется в качестве второго препарата для достижения целевого уровня ХС-ЛНП. Убедительно доказано, что комбинация статинов и эзетимиба эффективна и безопасна. В свете обновленных рекомендаций Европейского общества кардиологов 2019 г. комбинированная терапия розувастатином и эзетимибом привлекает особое внимание ввиду снижения рекомендуемых целевых значений ХС-ЛНП у пациентов с очень высоким риском менее 1,4 ммоль/л и снижения уровня ХС-ЛНП на 50% и более. Исследования продемонстрировали, что комбинация высокоинтенсивного статина (такого, как розувастатин) и эзетимиба снижает уровень ЛНП в среднем на 65% от исходного [9]. Достижение целевых значений ЛНП снизит риск развития сердечно-сосудистых осложнений, а видимый результат увеличит приверженность пациента терапии.
Препараты нового поколения на основе бемпедоевой кислоты демонстрируют многообещающие результаты по снижению уровня ХС-ЛНП как в монотерапии, так и в комбинации с другими препаратами (например, с эзетимибом) и интересны с точки зрения расширения возможностей достижения целевого ХС-ЛНП у пациентов, которые не могут принимать статины по разным причинам. Фиксированные комбинации липидснижающих препаратов позволяют уменьшить частоту нежелательных побочных реакций (например, уже доказано, что при совместном приеме эзетимиба со статинами снижается риск развития сахарного диабета), за счет синергического эффекта отмечается более значимое снижение уровня ХС-ЛНП и риска развития сердечно-сосудистых осложнений, более того, значительно повышается приверженность длительной липидснижающей терапии.
Источник
Гиполипидемическая терапия больных ИБС | #07-08/02 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
При лечении ИБС и других заболеваний, связанных с повышенным уровнем холестерина, необходимо стремиться к достижению целевого уровня холестерина в крови. Для этого многим больным назначаются гиполипидемические препараты
Ключевым моментом в патогенезе атеросклероза является отложение холестерина в стенке артерии. Еще в 1913 г. Н. Н. Аничков провозгласил принцип: без холестерина нет атеросклероза. В дальнейшем в ходе экспериментальных, эпидемиологических и клинических исследований было доказано, что, чем выше уровень холестерина в крови, тем выше риск развития и прогрессирования ишемической болезни сердца (ИБС), а также осложнений и смерти от нее.
Более точно степень риска отражает соотношение липидов и липопротеидов крови. Как правило, в клинической практике используются следующие четыре показателя: общий холестерин (ОХС); холестерин липопротеидов низкой плотности (ЛНПХС) — наиболее атерогенный; холестерин липопротеидов высокой плотности (ЛВПХС) — антиатерогенный; триглицериды (ТГ). Наиболее неблагоприятным в прогностическом плане принято считать сочетание высоких уровней ЛНПХС и ТГ с низким уровнем ЛВПХС.
Целевые уровни липидов крови
Среди рекомендаций по определению целевых уровней липидов крови наибольшее распространение получили европейские (1998) по профилактике и лечению ИБС и американские (2001) по диагностике и лечению гиперхолестеринемии.
Европейскими рекомендациями в качестве целевых определены уровень ОХС ниже 5,0 ммоль/л (190 мг/дл) и ЛНПХС менее 3,0 ммоль/л (115 мг/дл). Концентрации же ЛВПХС и ТГ не используются в качестве первичных целевых. Однако уровни ЛВПХС2,0 ммоль/л (180 мг/дл) являются показателями повышенного коронарного риска; это следует учитывать при выборе метода лечения пациента.
Американские рекомендации по вторичной профилактике (лечению) ИБС предусматривают в качестве основного только целевой уровень ЛНПХС20% (просто и быстро определяемой по специальным таблицам, составленным на основании данных Фремингемского исследования). Низкий уровень ЛВПХС рассматривается как сильный независимый фактор риска ИБС. Согласно американским, а также европейским рекомендациям, низким считается уровень ЛВПХС500 мг/дл. Повышенный уровень триглицеридов, являясь независимым фактором риска ИБС, свидетельствует об атерогенности богатых триглицеридами липопротеидов, т. е. частично метаболизированных липопротеидов очень низкой плотности (ЛОНП), обычно называемых ремнантными липопротеидами. В клинической практике ЛОНПХС наиболее доступен для оценки уровня атерогенных ремнантных липопротеидов. Суммарный уровень ЛНПХС+ЛОНПХС [называемый не-ЛВПХС (ОХС минус ЛВПХС)] американскими рекомендациями определен как вторичная цель лечения пациентов с высоким уровнем триглицеридов (>200 мг/дл). При наличии ИБС или ее эквивалентов целевым уровнем не-ЛВПХС является
Американские рекомендации по лечению гиперлипидемий у лиц с ИБС и другими атеросклеротическими заболеваниями более жесткие по сравнению с европейскими. Следует учитывать, что американские рекомендации в последней редакции изданы через три года после европейских, и за это время накопились новые данные, свидетельствующие о том, что большая степень снижения уровня ЛНПХС ведет к более выраженному улучшению состояния пациента. Дополнительные аргументы в пользу большего снижения ЛНПХС могут появиться в результате продолжающихся сегодня исследований, цель которых — ответить на вопрос, приводит ли снижение уровня ЛНПХС до 75 мг/дл (более низкого, чем это официально рекомендовано в настоящее время) к улучшению прогноза по сравнению со снижением ЛНПХС до уровня 100 мг/дл. По-видимому, в клинической практике при лечении пациентов с ИБС и другими атеросклеротическими заболеваниями сегодня следует придерживаться американских рекомендаций. Независимо от выбранных целевых уровней и решения о назначении гиполипидемических препаратов у каждого пациента с ИБС и другими атеросклеротическими заболеваниями необходимо учитывать возможность наличия дополнительных, кроме ЛНПХС, факторов риска — курения, артериальной гипертонии, низкого уровня ЛВПХС, избыточной массы тела, гиподинамии, повышенного потребления животных жиров. В случае выявления таких факторов риска должны быть даны рекомендации по их коррекции. Соблюдение гиполипидемической диеты позволяет снизить уровень ЛНПХС на 8-15% в зависимости от индивидуальных генетических особенностей пациентов, а также характера питания до начала диетотерапии. Эффект диетотерапии может быть оценен через 6 недель. Если показатель уровня холестерина не позволяет надеяться на его нормализацию только с помощью диеты (ЛНПХС>130 мг/дл), необходимо одномоментно начать диетотерапию и назначить гиполипидемический препарат. Различные пищевые добавки не обладают сопоставимым с медикаментозными препаратами гиполипидемическим действием, и их собственный клинический эффект не доказан. Они не заменяют гиполипидемические препараты, а могут применяться только в качестве дополнения к ним. У пациентов, госпитализированных с инфарктом миокарда или нестабильной стенокардией, в течение первых 24 часов с момента поступления в стационар следует исследовать уровень холестерина с целью использовать его для принятия решения о назначении гиполипидемического препарата. При этом нужно учитывать, что уровень холестерина при остром коронарном синдроме начинает снижаться в первые часы от его начала, достигает минимума через 24-48 ч и может сохраняться на этом уровне в течение нескольких месяцев. Поэтому у пациента, госпитализированного с острым коронарным синдромом, уровень холестерина, как правило, ниже его обычных показателей. Вполне обоснованной в связи с этим можно считать точку зрения, что всем пациентам с острым инфарктом или нестабильной стенокардией и уровнем ЛНПХС выше 100 мг/дл (2,6 ммоль/л) проведение медикаментозной гиполипидемической терапии необходимо начинать еще до выписки из больницы. В период госпитализации легче установить контроль за соблюдением рекомендаций врача. Так, по данным шведского исследования RIKS-HIA, годичная выживаемость пациентов с острым инфарктом миокарда, принимавших статины уже к моменту выписки из госпиталя, при прочих равных условиях была достоверно более высокой по сравнению с теми, кто к моменту выписки статины не принимал.
Результаты исследований с использованием клинических конечных точек не оставляют сомнений в том, что повышенный уровень холестерина (особенно ЛНПХС) у пациентов с заболеваниями, обусловленными атеросклерозом, необходимо снижать, причем эта терапия, включая терапию статинами, экономически выгодна. Метанализ исследований, посвященных вторичной профилактике, в ходе которых не применялись статины, показал, что снижение уровня ОХС на 10% приводит к уменьшению на 19, 12 и 15% частоты нефатального, фатального и всех инфарктов миокарда соответственно. В шестилетнем исследовании Coronary Drug Project было показано, что у мужчин, перенесших инфаркт миокарда и получавших терапию никотиновой кислотой (уровень ОХС снизился на 10%), отмечалось снижение частоты нефатальных инфарктов. Анализ, проведенный через 9 лет после прекращения исследования, также выявил достоверное снижение общей смертности на 11%. Стокгольмское исследование по вторичной профилактике ИБС показало, что комбинированная терапия клофибратом и никотиновой кислотой в течение 5 лет приводила к снижению смертности от ИБС на 36% и общей смертности на 26%, причем степень снижения смертности от ИБС была напрямую связана со степенью снижения уровня триглицеридов. Результаты исследований, посвященных вторичной профилактике ИБС с использованием статинов, окончательно рассеяли любые сомнения относительно необходимости гиполипидемической терапии при ИБС. В исследовании 4S, продолжавшемся 5,4 года (симвастатин 20-40 мг/день) у больных ИБС с высоким уровнем холестерина, где единственной главной конечной точкой была общая смертность, продемонстрировано ее достоверное (на 30%) снижение по сравнению с группой, получавшей плацебо. Снижения общей смертности на 22% удалось достичь также в ходе другого крупного исследования — LIPID, продолжавшегося 6,1 года (правастатин 40 мг/день) и охватывавшего широкий спектр больных ИБС с различным уровнем холестерина.
В ходе исследования CARE, длившегося 5 лет (правастатин 40 мг/день), были отмечены снижение частоты основных коронарных осложнений и достижение близкого к нормальному уровня холестерина у больных ИБС, перенесших инфаркт миокарда или страдавших нестабильной стенокардией. Эти исследования отмечали большее, чем при приеме других препаратов, снижение уровня ЛНПХС (на 25-35%), при этом терапия хорошо переносилась и была безопасной. Не отмечено также и роста смертности, не обусловленной ИБС. Частота основных коронарных осложнений снижалась на 24-34%, а необходимость реваскуляризации миокарда — на 20-37%. Важно, что положительный клинический эффект на фоне терапии статинами начинает проявляться сравнительно быстро, через один (исследование 4S)—два года (исследования CARE и LIPID). Чрезвычайно важен также другой положительный эффект — все исследования выявили снижение риска ишемического инсульта на 19-32%, что, по-видимому, обусловлено стабилизацией атеросклеротической бляшки, так как взаимосвязь между уровнем холестерина и частотой инсульта не доказана. В исследовании AVERT, продолжавшемся 1,5 года (аторвастатин 80 мг/день), было показано, что интенсивная терапия аторвастатином (снижение уровня ЛНПХС на 46%) у больных стабильной ИБС, по крайней мере, не уступала по эффективности с точки зрения прогноза баллонной ангиопластике коронарных артерий в сочетании с обычной гиполипидемической терапией. О пользе раннего начала терапии статинами свидетельствуют результаты исследования MIRACL, в ходе которого больным с острым инфарктом миокарда без формирования зубца Q или нестабильной стенокардией назначался аторвастатин в дозе 80 мг/день начиная с первых 24-96 часов заболевания. Частота основных коронарных осложнений через 4 месяца в группе, получавшей аторвастатин, была достоверно (на 16%) ниже по сравнению с группой, получавшей плацебо.
Исследования, проводившиеся с использованием различных гиполипидемических препаратов, показали, что интенсивная гиполипидемическая терапия замедляет прогрессирование атеросклероза коронарных артерий, шунтов после операции АКШ и сонных артерий. При этом очень небольшая, но статистически достоверная разница ангиографических показателей в группах сопровождается выраженным (на 40-80%) снижением частоты острых коронарных синдромов, что, вероятно, обусловлено стабилизацией атеросклеротической бляшки. Изучалась возможность профилактики рестенозов после баллонной ангиопластики коронарных артерий с помощью статина (флувастатина). И хотя препарат не влиял на частоту рестенозов, через 6 месяцев после проведения процедуры смертность была достоверно ниже в группе, получавшей флувастатин. Гиполипидемическая терапия нормализует нарушенную при гиперлипидемии функцию эндотелия, являющуюся одним из важных патогенетических звеньев развития атеросклероза. Помимо собственно гиполипидемического существует целый ряд других нелипидных антиатерогенных положительных эффектов гиполипидемических препаратов: антиишемический, антитромбогенный, противовоспалительный, влияние на пролиферацию гладкомышечных клеток артерий и др.
Основные классы гиполипидемических препаратов и их сравнительные характеристики представлены в таблице.
Статины, принимая во внимание их самую высокую среди всех классов гиполипидемических препаратов гипохолестеринемическую эффективность, доказанное в ходе клинических исследований улучшение прогноза у больных ИБС с различными ее формами, степенью тяжести, риска и выраженностью гиперлипидемии (мужчины и женщины, молодые и пожилые, с диабетом и без диабета, стабильная ИБС и острый коронарный синдром), хорошую переносимость и высокую безопасность, несомненно, являются препаратами выбора. Все статины снижают уровень триглицеридов. Наиболее эффективны в этом плане аторвастатин и симвастатин, причем, чем выше исходный их уровень, тем более выражен гипотриглицеридемический эффект. Статины неэффективны при лечении пациентов с хиломикронемией. Удвоение дозы любого из статинов приводит к дополнительному снижению уровня ЛНПХС примерно на 6%.Терапия статинами не нарушает синтез стероидов в надпочечниках и половых железах. Сочетанное применение статинов с никотиновой кислотой или фибратами в рутинной практике не рекомендуется, так как сопряжено с существенным повышением риска осложнений (миопатии, рабдомиолиза). Решение об использовании такого сочетания препаратов должно приниматься только в клиниках, специализирующихся на лечении гиперлипидемий. Нежелательные побочные эффекты статинов встречаются значительно реже, чем при лечении другими гиполипидемическими препаратами, и еще реже требуется в связи с этим их отмена. Основная проблема, связанная с лечением статинами во всем мире, — их относительная дороговизна. И тем не менее при оценке соотношения суммарная клиническая польза для больного/стоимость выясняется, что для большинства больных ИБС они наиболее выгодны.
Секвестранты желчных кислот, использовавшиеся когда-то в качестве основных гиполипидемических препаратов, сегодня применяются в основном в качестве дополнения к терапии, когда необходимо дальнейшее снижение уровня холестерина по сравнению с достигнутым на фоне приема статинов. Это сочетание эффективно и безопасно. Пациентам с выраженной гипертриглицеридемией секвестранты противопоказаны, так как они могут повышать уровень триглицеридов. Применение секвестрантов сравнительно часто сопровождается нежелательными побочными эффектами, связанными с нарушением процесса всасывания в кишечнике пищи и лекарственных препаратов. Преимущества секвестрантов обусловлены их невсасываемостью в кишечнике — они могут применяться у кормящих грудью матерей и детей.
Никотиновая кислота, применяющаяся с 1955 года, представляет собой первый гиполипидемический препарат. Отличительными особенностями никотиновой кислоты являются ее наибольшая по сравнению с другими препаратами способность повышать уровень ЛВПХС и снижать уровень Лп(а), а также умеренный вазодилатирующий эффект. Доказанная клиническая эффективность и безопасность, сочетающиеся с антиатерогенным влиянием на все оцениваемые в практике липопротеиды и аполипопротеиды, а также низкая по сравнению с другими препаратами стоимость относятся к несомненным преимуществам этого препарата. Проблему же представляет его сравнительно плохая переносимость — до 40% пациентов отказываются от приема препарата из-за побочных эффектов, главным образом приливов, частоту и выраженность которых можно уменьшить благодаря предварительному (за 30-60 мин) приему аспирина. У пролонгированных форм никотиновой кислоты, описанных выше, нежелательных побочных эффектов меньше, однако, по некоторым данным, у этих препаратов ниже эффективность и выше гепатотоксичность.
Фибраты (производные фибриковой кислоты) — наиболее эффективные гипотриглицеридемические препараты. Этим и определяется основное показание к их применению — высокий уровень триглицеридов [более 1000 мг/дл (11,5 ммоль/л)]. В ряде случаев они могут быть полезны и при комбинированной гиперлипидемии. Гемфиброзил и клофибрат снижают частоту коронарных осложнений при вторичной профилактике у пациентов с низким уровнем ЛВПХС. Лечение безафибратом и гемфиброзилом может сопровождаться положительной динамикой коронарного атеросклероза, по данным ангиографии. Сочетать терапию фибратами и статинами, как отмечалось выше, не рекомендуется из-за возрастания риска тяжелых мышечных осложнений. Тем более не рекомендуется назначать эти препараты в таком сочетании без консультации специалистов-липидологов. Из нежелательных побочных эффектов, присущих всем фибратам, необходимо отметить повышение концентрации холестерина в желчи, в связи с чем возрастает риск желчнокаменной болезни.
Таким образом, необходимо стремиться к достижению рекомендованного целевого уровня холестерина, для чего многим больным показано назначение гиполипидемических препаратов.
Препаратами выбора являются статины. Тем не менее необходимо оценивать конкретную клиническую ситуацию в целях выбора препарата, а в некоторых случаях и комбинации лекарственных средств.
По вопросам литературы обращайтесь в редакцию
Источник