Гемоглобин новорожденного переливание крови
Содержание статьи
етодика переливания эритроцитарной массы у новорожденных детей
Методика переливания эритроцитарной массы у новорожденных детей
Рекомендации по переливанию эритроцитарной массы у пациентов младше 4 мес:
1. Гематокрит менее 20% с маленьким количеством ретикулоцитов и симптомами анемии1.
2. Гематокрит менее 30% у новорожденных:
а. Оксигенотерапия более 35%.
б. Оксигенотерапия через носовые катетеры.
в. Постоянное положительное давление в дыхательных путях и/или периодическая принудительная ИВЛ со средним давлением в дыхательных путях менее 6 см вод.ст.
г. Выраженное апноэ или брадикардия2.
д. Выраженная тахикардия или тахипноэ3.
е. Медленная прибавка массы тела4.
3. Гематокрит менее 35% у новорожденных:
а. Оксигенотерапия более 35%.
б. Постоянное положительное давление в дыхательных путях/периодическая принудительная ИВЛ со средним давлением в дыхательных путях более 6 см.вод.ст.
4. Гематокрит меньше 45% у новорожденных:
а. Экстракорпоральная мембранная оксигенация.
б. Врожденный «синий» порок сердца.
* 1 Тахикардия, тахипноэ, плохо питающиеся.
2 Более шести эпизодов в течение 12 ч или два эпизода за 24 ч, требующих вентиляции мешком через маску, в то время как пациент получает терапевтические дозы метилксантинов.
3 ЧСС более 180 в минуту, ЧДД более 80 в минуту в течение 24 ч.
4 Набор менее 10 г/день, наблюдаемый в течение 4 дней, при одновременном получении более 100 ккал/кг в день.
Методика переливания эритроцитарной массы
1. Определение общего количества крови, которую необходимо перелить:
а. Расчет объема крови для трансфузии. Большинству новорожденных переливают 10-15 мл/кг ЭМ, которая увеличивает гемоглобин на 3 г/дл.
б. Расчет требуемого объема ЭМ: [ПОК х (Ht желаемый — Ht наблюдаемый)] х Ht-единицы ЭМ,
где ПОК — предполагаемый объем крови (примерно 80-85 мл/кг массы тела у доношенных новорожденных и 100-120 мл/кг массы тела у недоношенных); Ht — гематокрит.
2. Учитывают объем крови, необходимый для заполнения мертвого пространства трубок, фильтра, механизма насоса (варьирует в зависимости от систем, может достигать 30 мл).
3. Получают препарат крови:
а. В нескольких исследованиях зафиксирована информация о безопасности использования ЭМ, с добавлением антикоагулянта.
б. Не следует хранить ЭМ с добавлением дополнительных растворов для массивных трансфузий, за исключением удаления добавки путем центрифугирования (предполагается риск гиперосмолярности, гипергликемии, гипернатриемии, гиперкалиемии, гиперфосфатемии).
в. У новорожденных, получающих 10-15 мл ЭМ, количество ионов калия, получаемых при переливании, оценивается только в 0,15 ммоль/кг и не предполагает существенного риска для большинства новорожденных.
г. Снижается риск возможных отрицательных эффектов от донорской крови путем деления одной дозы на несколько более мелких для одного ребенка и их использования до истечения срока годности.
4. На этикетки выносится информация о необходимости перекрестных проб.
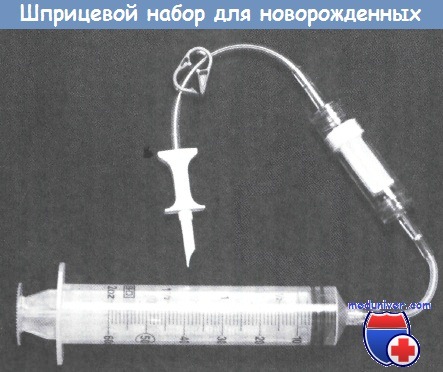 Шприцевый набор для новорожденных с фильтром. (Фотография любезно предоставлена Charter Medical Ltd., Winston-Salem, NC, USA.).
Шприцевый набор для новорожденных с фильтром. (Фотография любезно предоставлена Charter Medical Ltd., Winston-Salem, NC, USA.).
Эта система, при условии использования со стерильной методикой соединения, обеспечивает закрытый способ введения, который поддерживает постепенное опорожнение крови.
Шприц, заполненный компонентом крови (ЭМ, плазмой) должен быть введен пациенту в течение 24 ч, а шприц, заполненный разведенными тромбоцитами, — в течение 4 ч.
5. Подтверждают, что ограничения применены к препаратам крови и помечены на трансфузионной бирке:
а. ЦМВ: проверялось/не проверялось.
б. Облучение: да/нет.
в. Прямой (семейный) донор: да/нет.
г. Антиэритроцитарные антитела отрицательны: да/нет.
д. Серповидноклеточный тест отрицателен: да/нет.
е. Другие ограничения: да/нет.
6. Проверяют соответствие выбранной крови путем сравнения препарата крови, полученной от пациента, и информации на этикетке на пакете с донорским препаратом.
Рекомендуют применение устройства для чтения штрихкода:
а. Информация о группе крови на этикетке и результатами исследования этой крови.
б. Номер пациента в госпитале или истории болезни.
в. Идентификация пациента с помощью браслета на руке или ноге.
г. Группа и Rh-фактор крови у донора и реципиента.
д. Срок годности и срок заготовки.
е. Ограничения, как предписано врачом или указаниями лечебного учреждения.
7. Согревание ЭМ (эритроцитарной массы):
а. Нет необходимости в согревании небольших объемов разведенной ЭМ, особенно если трансфузия будет проведена в течение 2-3 ч.
б. ЭМ масса может быть согрета путем помещения шприца в инкубатор с обогреваемым воздухом на 30 мин перед трансфузией.
в. Нельзя согревать кровь путем воздействия на нее нагревательных ламп или фототерапевтического света, так как это может вызвать гемолиз.
8. Строго соблюдают стерильность во время всей процедуры.
9. Если банком крови предоставлена заранее профильтрованная ЭМ в шприце, присоединяют трубку прямо к нему.
10. Если ЭМ предоставлена в мешке, используют иглу с крупным просветом (18-го размера или более) для забора объема в шприц. Фильтр следует расположить между мешком и шприцем.
11. Заполняют трубку кровью. Освобождают шприц и трубку от пузырьков и монтируют в инфузионное устройство.
 Использование стерильного соединительного приспособления:
Использование стерильного соединительного приспособления:
а — единица эритроцитов для переливания у взрослых показана вместе с педиатрическим транспортным пакетом.
Его можно присоединить путем прокола пакета, из-за чего ЭМ следует использовать в течение 24 ч; или транспортный пакет может быть соединен с помощью стерильного соединительного устройства;
а, б — отдельные трубочки помещаются в держатели. Крышку закрывают;
в — сварочная пластина нагревается до 260 °С, расплавляя трубки. Благодаря держателю трубок они спаиваются вместе;
г — теперь из пакета можно извлекать столько препарата крови, сколько нужно. Поскольку поддерживается замкнутая система, срок использования крови не изменяется.
12. Проверяют проходимость сосудистого доступа.
13. Промывают катетер физиологическим раствором.
14. Записывают и следят за жизненно важными признаками.
15. Определяют гематокрит. Повторяют каждый час, если необходимо.
16. Начинают переливание при установленной скорости 5 мл/кг в час.
17. Осторожно переворачивают контейнер с кровью каждые 15-30 минут для уменьшения осаждения.
18. Останавливают переливание при появлении любых побочных изменений в состоянии пациента.
19. В конце инфузии промывают катетер физиологическим раствором.
20. Проверяют концентрацию гемоглобина и гематокрит у пациента, если необходимо, не ранее чем через 2 ч после трансфузии.
21. Если после трансфузии гематокрит/гемоглобин не поднялся до ожидаемого уровня, рассматривают следующие варианты:
а. Низкий гематокрит в пакете с эритроцитарной массой (ЭМ).
б. Неправильный расчет требуемой инфузии.
в. Продолжающаяся кровопотеря.
г. Трансфузионная реакция.
д. Гемолиз из-за несовместимости по системе AB0 или другой:
(1) Новорожденный имеет циркулирующие анти-А-, анти-В- и анти-АВ-антитела, которые связываются с А- или В-антигенами при трансфузии эритроцитов.
(2) Прямой антиглобулиновый тест (ПАТ) первоначально отрицательный стал положительным.
(3) Неожиданное повышение уровня билирубина.
(4) Новорожденный имеет эритроцитарные антитела другой системы, кроме AB0.
(5) Гемолиз вследствие механического повреждения эритроцитов или заболевания донора, сопровождающегося гемолизом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Также рекомендуем «Переливание цельной крови у новорожденных детей — показания, методика»
Оглавление темы «Неонатология»:
- Проблемы с кожей вокруг стомы и ее осложнения
- Уход за гастростомой и гастростомической трубкой
- Проблемы применения гастростомической трубки
- Особенности переливания крови и ее компонентов у новорожденных детей
- Исследования крови и ее компонентов перед переливанием
- Оборудование для переливания крови и ее компонентов у новорожденных детей
- Показания и противопоказания для переливания эритроцитарной массы у новорожденных детей
- Методика переливания эритроцитарной массы у новорожденных детей
- Переливание цельной крови у новорожденных детей — показания, методика
- Показания и противопоказания для переливания тромбоцитов у новорожденных детей
Источник
Внутриутробное переливание крови как метод лечения гемолитической болезни плода

При обсуждении такой темы, как гемолитическая болезнь плода и новорожденного, в центре внимания стоит вопрос о пролонгировании беременности и улучшении показателей крови. На данный момент единственным методом коррекции тяжелой анемии является заменное переливание крови (ЗПК). Однако к моменту рождения уровень гемоглобина и билирубина может достигать критических значений, что значительно усложняет лечение и побуждает искать альтернативные методы. Одним из таких методов является внутриутробное переливание крови, о котором мы и поговорим в этой статье.
Гемолитическая болезнь новорожденных (ГБН) — состояние, обусловленное иммунологической несовместимостью крови плода и матери по эритроцитарным антигенам. Несоответствие приводит к выработке материнским организмом антител к эритроцитарным антигенам плода, которые проникают через плацентарный барьер и вызывают гемолиз его эритроцитов. Как известно, повышенное разрушение эритроцитов приводит к усилению билирубинового обмена и снижению гематокрита и уровня гемоглобина. В дальнейшем нарастает повреждение печени, снижается синтез альбуминов, что приводит к развитию отечного синдрома, а большое количество неконъюгированного билирубина оказывает повреждающее воздействие на ЦНС и почки, вызывая билирубиновую энцефалопатию и билирубиновый инфаркт почек соответственно.
Лечение ГБН начинается сразу после рождения, но к этому моменту организм накапливает достаточно билирубина, чтобы он начал оказывать токсическое действие на ткани и органы ребенка, в то время как уровень гемоглобина и гематокрит падают до критических цифр, что приводит к тяжелой анемии.
Для успешного проведения манипуляции ЗПК необходимо соблюдать ряд условий:
- Оптимальный срок беременности для проведения данного вмешательства — промежуток между 18 и 35 неделями гестации, так как до 18 недели пуповина еще слишком мала для безопасного проведения кордоцентеза, а после 35 недели риск, связанный с проведением кордоцентеза, выше, чем риск осложнений после преждевременных родов.
- По результатам кордоцентеза, показатели гемоглобина для проведения трансфузии должны быть на два стандартных отклонения ниже нормальных показателей для данного срока гестации.
- Пиковая систолическая скорость кровотока (ПССК) в средней мозговой артерии плода (по результатам допплерографии) должна быть выше 1,50 МоМ (Multiples of the n).
Таблица 1. Нормальные значения гемоглобина плода на сроке 18-34 недели.
Срок гестации, недели | Показатель гемоглобина г/л | Два стандартных отклонения от нормального гемоглобина, г/л |
18 | 113 | 93 |
19 | 115 | 95 |
20 | 117 | 97 |
21 | 119 | 99 |
22 | 121 | 101 |
23 | 123 | 103 |
24 | 125 | 105 |
25 | 127 | 107 |
26 | 128 | 108 |
27 | 130 | 110 |
28 | 132 | 112 |
29 | 134 | 114 |
30 | 136 | 116 |
31 | 138 | 118 |
32 | 140 | 120 |
33 | 142 | 122 |
34 | 144 | 124 |
Таблица 2. Сравнение показателей ПССК в средней мозговой артерии плода и степени тяжести анемии.
Показатель ПССК, МоМ | Степень тяжести анемии |
1,29 | легкая |
1,50 | средняя |
1,55 | тяжелая |
После выполнения всех диагностических мероприятий и подтверждения необходимости в ЗПК производится подбор донора с учетом всех требований к компонентам крови для внутриутробного переливания, согласно приказу 183н. Кровь для переливания 0(I), резус-D-отрицательная смешивается с материнской кровью, чтобы уменьшить риск сенсибилизации к новым антигенам эритроцитов. Единицы крови отмывают и плотно упаковывают до конечного гематокрита от 75 до 85 процентов, чтобы уменьшить объем, вводимый плоду.
Процедура кордоцентеза проводится под контролем УЗИ в условиях операционной, чтобы в случае кровотечения провести экстренное кесарево сечение. Потенциальные места доступа к плоду включают пупочную вену, брюшную полость, пупочную артерию и сердце, но наиболее оптимальное место пункции — пупочная вена в области ее выхода из плаценты, так как пуповина в этом месте достаточно хорошо фиксирована.
Объем переливания зависит от фактического и целевого гематокрита, а также размера плода. Целевой гематокрит у плода составляет 37 ± 4 % в 17 недель, повышаясь до 43 ± 7 % к концу срока гестации. Однако достижение целевого гематокрита при тяжелой анемии за одно переливание может привести к увеличению постнагрузки на сердце, поэтому целесообразно проводить несколько процедур переливания, прежде чем будет достигнут целевой уровень.
После завершения процедуры производится повторный забор крови для определения гематокрита и гемоглобина плода. На протяжении 24 часов производится контроль сердцебиения и УЗИ плода.
Возможные осложнения при внутриутробном переливании крови не отличаются от рисков при проведении стандартного кордоцентеза: кровотечение из пунктированной пупочной вены, брадикардия плода, амнионит, разрыв плодных оболочек, преждевременные роды. Однако стоит учитывать, что польза проводимой процедуры выше, чем риски осложнений.
Говоря о преимуществах, выживаемость после процедуры составляет около 80-90 %, в то время как перинатальная потеря — 1-3 %. Исход зависит от срока первого переливания и выраженности отечного синдрома, но, в целом, это достаточно хороший результат, по сравнению с высокой смертностью детей с тяжелой степенью анемии в результате ГБН.
Источники:
- Неонатология: национальное руководство. Под редакцией Володина Н.Н. ГЭОТАР-Медиа, 2009
- Moise K. J. J. Intrauterine fetal transfusion of red cells // UpTo https://www.upto.com/contents/intrauterine-fetal-transfusion-of-red-cells. — 2018.
- Макогон А.В, Андрюшина И.В. Пиковая систолическая скорость кровотока в средней мозговой артерии как предиктор анемии плода. История развития и современное состояние диагностического метода. Ультразвуковая и функциональная диагностика, № 1, 2012.
- Иванова А.В, Захарова С.Ю, Косовцова Н.В, Павличенко М.В, Генералов А.Е. Особенности течения неонатального периода у новорожденных, получивших внутриутробное внутрисосудистое переливание крови по поводу гемолитической болезни плода. Российский вестник перинатологии и педиатрии, vol. 60, № 1, 2015.
- Weiner, Carl P. Risk factors for cordocentesis and fetal intravascular transfusion. American Journal of Obstetrics & Gynecology , Volume 165
- Приказ Министерства здравоохранения Российской Федерации (Минздрав России) от 2 апреля 2013 г. N 183н г. Москва «Об утверждении правил клинического использования донорской крови и (или) ее компонентов».
- Schumacher B, Moise KJ Jr. Fetal transfusion for red blood cell alloimmunization in pregnancy.
- Van Kamp, I. L., Klumper, F. J., Meerman, R. H., Oepkes, D. , Scherjon, S. A. and Kanhai, H. H. Treatment of fetal anemia due to red‐cell alloimmunization with intrauterine transfusions in the Netherlands, 1988-1999. Acta Obstetricia et Gynecologica Scandiica, 83, 2004.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
Анемия недоношенных
Анемия недоношенных — это патология, возникающая у детей, которые были рождены ранее 37 недель беременности, и выражающаяся в снижении гемоглобина крови. Основные проявления сводятся к бледности слизистых оболочек и кожи, снижению двигательной активности и сосания, ухудшению аппетита, тахикардии. Клиническая симптоматика при начальных стадиях анемии может отсутствовать вовсе. Диагностика основывается на изучении клинического анализа крови, который может дополняться биохимическими исследованиями. Для лечения используются гемотрансфузии, эритропоэтин, препараты железа, витамины Е, В12 и фолиевая кислота.
Общие сведения
Благодаря развитию современной медицины процент выживаемости детей с III — IV степенью недоношенности увеличился на 50-70%, а с I-II степенями — до 95%. Обратной стороной ситуации явился рост случаев заболеваемости, в том числе анемией недоношенных. Её описание впервые встречается в работах Д. Шульмана, датируемых 1959 годом. Частота выявления патологии на сегодняшний день колеблется от 16 до 91%. Тяжесть течения напрямую зависит от гестационного возраста ребёнка. Чем он ниже, тем серьёзнее проявления заболевания. Так, у детей, рождённых до 30 недель с массой тела до 1,5 кг, состояния, требующие переливания эритромассы, возникают более чем в 90% случаев. У недоношенных обоих полов анемия обнаруживается с одинаковой частотой.
Анемия недоношенных
Причины
Главными причинами, обусловливающими развитие анемического синдрома, являются функциональная незрелость костного мозга и усиленный распад клеток крови, в которых располагается фетальный гемоглобин. Особое значение отводится уровню эритропоэтина — почечного гормона, играющего ключевую роль в адаптации организма в условиях тканевой гипоксии и необходимого для эритропоэза. Синтез эритропоэтина у недоношенных изначально высок, но вскоре после рождения резко снижается. Также важными моментами в развитии анемии недоношенных являются:
- Дефицит железа. Постоянно увеличивающийся общий объём крови требует немалых количеств микроэлемента, баланс которого отрицательный. Кроме того, у детей с малым сроком гестации отмечается низкая способность к использованию Fe, которое остаётся после распада эритроцитов. Срок жизни последних составляет в 2 раза меньше — около 50-70 дней. Также у недоношенных увеличено выведение железа с каловыми массами.
- Нарушение баланса фолиевой кислоты. Запасы витамина В9 у новорождённого малы, а потребность растущего организма в нем очень велика. Фолиевая кислота, продуцируемая микрофлорой кишечника и депонируемая в печени, расходуется за 2-4 недели. Недостаточность стремительно формируется и прогрессирует при дефиците фолата у матери во время вынашивания плода или в период лактации.
- Недостаточность витамина Е. Он участвует в синтезе гема и защищает мембраны эритроцитов от окисления. Его запасы также низки и составляют у доношенных около 20 мг, а у недоношенных при массе 1000 г всего 3 мг. Через кишечник витамин всасывается в крайне малом количестве. На его усвояемость неблагоприятно влияют асфиксия, инфекции и родовые травмы. Назначение средств, содержащих железо, и вскармливание коровьим молоком повышают его потребность.
Патогенез
У плода кроветворение начинается рано. До 2-х недель эритроциты синтезируются желточным мешком, до 16 недель — печенью и селезёнкой. Начиная с 20 недели, главным кроветворным органом становится красный костный мозг. Но у глубоко недоношенных детей очаги экстрамедуллярного кроветворения существуют еще в течение 1-2 месяцев после рождения. После их затухания на костный мозг ложится повышенная нагрузка, поэтому в условиях его функциональной незрелости и недостатка веществ, откладывающихся в депо на последних месяцах беременности (кобальт, медь, витамины из групп С и В), число гемоглобина в эритроцитах резко снижается.
Все ткани и внутренние органы недополучают нужного количества кислорода. Возникают дистрофические изменения кожного покрова, мочевыводящих путей, слизистых ЖКТ, поперечнополосатой мускулатуры, мышечной оболочки сердца и др. Снижается активность многих ферментных систем. Особенно стремительно анемия недоношенных развивается при наличии инфекционного поражения, внутричерепной родовой травмы и пренатальной гипотрофии.
Классификация
Заболевание может протекать в лёгкой (Hb 85-100 г/л), средней (70-84 г/л) и тяжёлой (69 г/л и ниже) форме. Лёгкая степень тяжести симптоматически может не проявляться, для остальных характерна развёрнутая клиническая картина. Тактика лечения напрямую зависит от уровня гемоглобина. Выделяются следующие фазы данной патологии:
- Ранняя. Выявляется в период с 4 по 8 недели внеутробной жизни. Возникает из-за угнетения эритропоэза и постоянно увеличивающейся массы тела, для которой требуется все большее число эритроцитов. Баланс железа сохранён или даже увеличен.
- Промежуточная. Эритропоэз восстанавливается, о чём свидетельствует появление в крови ретикулоцитов, которые ранее у ребёнка не определялись. Но разрушение эритроцитов и объём крови постоянно нарастают, расходуются запасы Fe, которых хватает на 16-20 недель.
- Поздняя. Связана с истощением депо железа и развитием Fe-дефицитной анемии. Проявления заболевания отчётливо заметны после 16-20 недели, и без должного лечения они только прогрессируют.
В педиатрии ряд авторов отдельно выделяют мегалобластную и гемолитическую анемию недоношенных. Первый тип связан с недостаточностью фолатов и их неустойчивым балансом. Второй формируется при дефиците витаминов из группы Е в период особой чувствительности эритроцитов к процессам окисления. Оба вида встречаются на протяжении с 6 по 10 недели новорожденности и не несут большой угрозы для жизни детей.
Симптомы анемии недоношенных
Клиническая картина зависит от формы и степени тяжести анемического синдрома. При показателях гемоглобина свыше 90 г/л симптоматика анемии недоношенных может отсутствовать или проявляться незначительно. Ранний тип имеет более благоприятное течение. Характерными особенностями являются ухудшение сосания груди или бутылочки со смесью, уменьшение активности движений ребёнка, прогрессирующая бледность слизистых структур и кожи, возникновение систолического шума в области верхушки сердца. Частота дыхательных движений и сердечных сокращений могут, как увеличиваться, так и уменьшаться.
Поздняя форма имеет высокие темпы развития. Она проявляется нарастающей бледностью, повышенным шелушением кожи, сонливостью, слабостью, вялостью, заторможенностью, снижением аппетита, вплоть до полного отказа от грудного или искусственного вскармливания. Тоны сердца приглушены, отмечается тахикардия, которая направлена на компенсацию гипоксического состояния путём увеличения перфузии тканей. Важными характерными симптомами В12 и фолиеводефицитной анемии являются периферическая невропатия, умеренная гепато- и спленомегалия, «лакированный» язык. При гиповитаминозе Е из клинических проявлений выделяются гемолитические кризы и отёчный синдром.
Осложнения
На современном этапе их формирование происходит крайне редко ввиду оказания своевременной медицинской помощи. Из осложнений можно встретить хроническую гипоксию тканей и внутренних органов. Она приводит к отставанию в физическом и умственном развитии, функциональной нестабильности органов желудочно-кишечного тракта и сердечно-сосудистой системы. Это сопровождается длительным расстройством стула, перепадами артериального давления и пульса, в тяжёлых случаях нарушениями сердечного ритма — экстрасистолиями, атриовентрикулярными блокадами, фибрилляцией предсердий и прочими.
Диагностика
Выявлением анемии недоношенных занимаются врачи неонатологи и педиатры. При патронаже новорожденных обращают внимание на окраску слизистых и кожных покровов, антропометрические показатели, физическое развитие. Любой подозрительный на анемию случай в обязательном порядке подтверждается результатами лабораторных тестов крови:
- Общий анализ крови. Основными диагностическими критериями являются снижение Hb, эритроцитов, сниженное или нормальное число ретикулоцитов, несколько повышенное или нормальное СОЭ. Кроме того, обнаруживается деформация эритроцитов (пойкилоцитоз) и изменение их размера (анизоцитоз). При проведении анализа на геманализаторе определяется снижение среднего размера эритроцита, среднего содержания и концентрации Hb в эритроците.
- Биохимический анализ крови. Наиболее важно его проведение в поздней фазе. Исследуют железосвязывающую способность сыворотки, уровень ферритина и железа. Последние клинические рекомендации включают определение рТФР — растворимых трансферриновых комплексов, которые снижаются при недостатке Fe.
Дифференциальную диагностику проводят с гемолитической болезнью новорождённых и другими наследственными патологиями — серповидно-клеточной анемией, талассемиями, болезнью Миньковского-Шоффара, недостаточностью ферментов пентозофосфатного цикла. Для уточнения диагноза привлекают врачей-генетиков, гематологов.
Лечение анемии недоношенных
Ранняя форма анемии активной терапии не требует, поскольку является физиологическим процессом. Для её коррекции важны нормальное питание, дополнительные источники фолатов, витаминов С, Е и В. Гемотрансфузии проводятся только при гематокрите ниже 30% и гемоглобине менее 70 г/л. Одним из эффективным лекарств, снижающих необходимость в переливании эритроцитарной массы, является человеческий эритропоэтин. При его введении потребность в Fe возрастает, что требует дополнительного назначения микроэлемента. В качестве источника антиоксидантов назначается перорально витамин Е.
Лечение поздней формы основывается на ферротерапии. Высокой эффективности и хорошей переносимости добиваются путём внутривенного введения препаратов, содержащих железо. В среднем активный курс приёма Fe составляет около 7 недель, а поддерживающий — до 1 года. Не менее важны полноценный сон, свежий воздух, лечебная гимнастика и грудное вскармливание. Введение овощного прикорма начинают с 4 месяцев, мясного — с 7 месяцев.
Прогноз и профилактика
Прогноз при грамотном подходе к лечению благоприятный, ранние и отдалённые осложнения встречаются в единичных случаях. В качестве профилактики со стороны матери важно соблюдение принципов питания, терапии токсикоза и лечения хронической патологии. Принимать фолиевую кислоту беременным рекомендуется в последнем триместре, а недоношенным детям с рождения. В первые 3 месяца жизни при низкой массе тела в форме капель используется витамин Е. Препараты Fe следует назначать на первом году жизни, начиная с 8 недели. Наблюдение педиатра осуществляется на протяжении года. Прививки недоношенным детям с анемией не противопоказаны.
Источник