Гемоглобин с оксидом углерода
Содержание статьи
Транспорт кислорода и углекислого газа кровью
Транспорт кислорода и углекислого газа кровью, формы анемии
Транспорт О2 с помощью гемоглобина
Красный пигмент гемоглобин (Нb) состоит из белковой части (глобина) и собственно пигмента (гема). Молекулы составляют четыре белковые субъединицы, каждая из которых присоединяет гем-группу с двухвалентным атомом железа, находящимся в ее центре. В легких каждый атом железа присоединяет одну молекулу кислорода. Кислород переносится в ткани, где он отделяется. Присоединение О2 называется оксигенацией (насыщением кислородом), а его отсоединение – дезоксигенацией.
Транспорт СО2

Около 10% углекислого газа (СО2), конечного продукта окислительного метаболизма в клетках тканей, переносится кровью физически растворенным п 90% — в химически связанной форме. Большая часть углекислого газа сначала диффундирует из клеток тканей в плазму, а оттуда в эритроциты. Там молекулы СО2 химически связываются и превращаются с помощью ферментов в намного более растворимые бикарбонат-ионы (НСО3-), которые переносятся в плазме крови. Образование СO2 из НСО3- значительно ускоряется с помощью фермента карбоангидразы, присутствующего в эритроцитах.
Большая часть (около 50-60%) образованных бикарбонат-ионов поступает из эритроцитов обратно в плазму в обмен на хлорид-ионы. Они переносятся в легкие и выделяются в процессе выдоха после превращения в СO2. Оба процесса — образование НСО3- и освобождение СO2, соответственно связаны с оксигенацией и дезоксигенацией гемоглобина. Дезоксигемоглобин — заметно более сильное основание, чем оксигемоглобин, и может присоединить больше ионов Н+ (буферная функция гемоглобина), таким образом способствуя образованию НСО3- в капиллярах тканей. В капиллярах легких НСО3- опять проходит из плазмы крови в эритроциты, соединяется с Н+-ионами и превращается опять в СO2. Этот процесс подтверждается тем фактом, что окисленная кровь выделяет больше протонов Н+. Намного меньшая доля СО2 (около 5-10%) связана непосредственно с гемоглобином и переносится как карбаминогемоглобин.
Гемоглобин и угарный газ
Оксид углерода (угарный газ, СО) является бесцветным газом без запаха, который образуется во время неполного сгорания и, как кислород, может обратимо связываться с гемоглобином. Однако сродство угарного газа к гемоглобину заметно больше, чем у кислорода. Таким образом, даже когда содержание СО во вдыхаемом воздухе составляет 0,3%, 80% гемоглобина связывается с угарным газом (НbСО). Так как угарный газ в 200-300 раз медленней, чем кислород, освобождается от связи с гемоглобином, его токсическое действие определяется тем, что гемоглобин больше не может переносить кислород. У тяжелых курильщиков, например, 5-10% гемоглобина присутствует как НbСО, в то время как при его содержании в 20% появляются симптомы острого отравления (головная боль, головокружение, тошнота), а 65% могут быть смертельным.
Содержание гемоглобина в крови (Нb)
Часто для оценки гемопоэза или для распознавания различных форм анемии определяют среднее содержание гемоглобина в эритроците (СГЭ). Оно вычисляется по формуле:
СГЭ = (содержание гемоглобина (г/100 мл крови) / количество эритроцитов (10ˉ6г/мкл))*10
Значение среднего содержания гемоглобина в эритроците лежит между 38 и 36 пикограммами (пг) (1 пг = 10ˉ¹² г). Эритроциты с нормальным СГЭ называются нормохромными (ортохромными). Если СГЭ низкое (например, из-за постоянной потери крови или дефицита железа), эритроциты называются гипохромными; если СГЭ высокое (например, при пернициозной анемии благодаря дефициту витамина В12), они называются гиперхромными.
Формы анемии
Анемия определяется как дефицит (снижение количества) эритроцитов или сниженное содержание гемоглобина в крови. Диагноз анемии обычно ставится по содержанию гемоглобина, нижняя граница нормы достигает 140 г/л у мужчин и 120 г/л у женщин. Почти при всех формах анемии надежным симптомом заболевания является бледный цвет кожи и слизистых оболочек. Часто во время физических нагрузок заметно увеличивается сердечный ритм (увеличивая скорость кровообращения), а уменьшение кислорода в тканях приводит к одышке. Кроме того, встречается головокружение и легкая утомляемость.
Кроме железодефицитной анемии и хронической потери крови, например, из-за кровоточащих язв или опухолей в желудочно-кишечном тракте (гипохромные анемии), анемия может возникать при дефиците витамина В12. фолиевой кислоты или эритропоэтина. Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в незрелых клетках костного мозга и, таким образом, заметно влияют на деление и созревание эритроцитов (эритропоэз). При их нехватке образуется меньше эритроцитов, но они заметно увеличены из-за повышенного содержания гемоглобина (макроциты (мегалоциты), предшественники: мегалобласты), поэтому содержание гемоглобина в крови практически не изменяется (гиперхромная, мегалобластическая, макроцитарная анемия).
Дефицит витамина В12 нередко возникает из-за нарушения всасывания витамина в кишечнике, реже — вследствие недостаточного приема с пищей. Эта так называемая пернициозная анемия наиболее часто является результатом хронического воспаления в слизистой кишечника с уменьшением образования желудочного сока.
Витамин В12 всасывается в кишечнике только в связанном виде с фактором, находящимся в желудочном соке «внутренним фактором (Кастла)», который защищает его от разрушения пищеварительным соком в желудке. Так как печень может запасать большое количество витамина В12, то перед тем, как ухудшение всасывания в кишечнике повлияет на образование эритроцитов, может пройти 2-5 лет. Как и в случае дефицита витамина В12, дефицит фолиевой кислоты, другого витамина группы В, приводит к нарушению эритропоэза в костном мозге.
Есть две другие причины анемии. Одна из них — разрушение костного мозга (аплазия костного мозга) радиоактивным излучением (например, после аварии на атомной электростанции) или в результате токсичных реакций на лекарства (например, цитостатики) (апластическая анемия). Другая причина — это уменьшение продолжительности жизни эритроцитов в результате их разрушения или увеличенного распада (гемолитическая анемия). При сильной форме гемолитической анемии (например, следующей за неудачным переливанием крови), кроме бледности может наблюдаться изменение цвета кожи и слизистых оболочек на желтоватый. Эта желтуха (гемолитическая желтуха) вызвана увеличивающимся разрушением гемоглобина до билирубина (желтого желчного пигмента) в печени. Последнее приводит к увеличению уровня билирубина в плазме и его отложению в тканях.
Примером анемии, возникающей в результате наследственного нарушения синтеза гемоглобина, клинически проявляющейся как гемолитическая, служит серповидноклеточная анемия. При этой болезни, которая практически встречается только у представителей негроидных популяций, имеется молекулярное нарушение, приводящее к замене нормального гемоглобина на другую форму гемоглобина (HbS). В HbS аминокислота валин заменена на глутаминовую кислоту. Эритроцит, содержащий такой неправильный гемоглобин, в дезоксигенированном состоянии принимает форму серпа. Серповидные эритроциты более жесткие и плохо проходят через капилляры.
Наследственное нарушение у гомозигот (доля HbS в суммарном гемоглобине 70-99%) приводит к закупорке небольших сосудов и, таким образом, к постоянному повреждению органов. Пораженные этой болезнью люди обычно достигают зрелости только при интенсивном лечении (например, частичной замене крови, приеме анальгетиков, избегании гипоксии (кислородного голодания) и иногда — пересадке костного мозга). В некоторых регионах тропической Африки с высоким процентом малярии 40% популяции являются гетерозиготными носителями данного гена (когда содержание HbS менее 50%), у них таких симптомов не обнаруживается. Измененный ген обусловливает устойчивость к малярийной инфекции (селективное преимущество).
Регуляция образования эритроцитов
Образование эритроцитов регулируется гормоном почек эритропоэтином. Организм обладает простой, но очень эффективной системой регуляции для поддержания содержания кислорода и вместе с тем количества эритроцитов относительно постоянным. Если содержание кислорода в крови падает ниже определенного уровня, например, после большой потери крови или во время пребывания на больших высотах, постоянно стимулируется образование эритропоэтина. В результате усиливается образование эритроцитов в костном мозге, что увеличивает способность крови к переносу кислорода. Когда дефицит кислорода преодолевается увеличением числа эритроцитов, образование эритропоэтина опять уменьшается. Пациенты, нуждающиеся в диализе (искусственном очищении крови от продуктов обмена веществ), с нарушением функционирования почек (например, с хронической почечной недостаточностью) часто испытывают явный дефицит эритропоэтина и поэтому почти всегда страдают от сопутствующей анемии.
Невероятные курсы массажа! СПб.
Источник
Гемоглобин: роль в газообмене и процессе дыхания
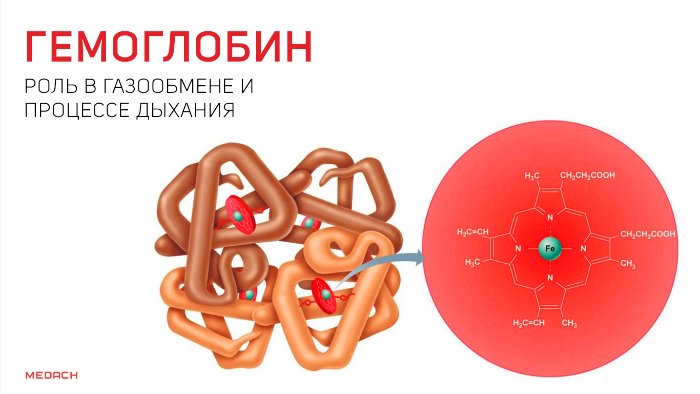
Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
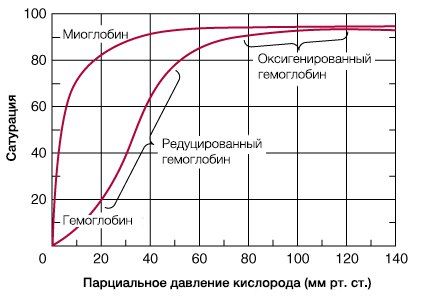
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
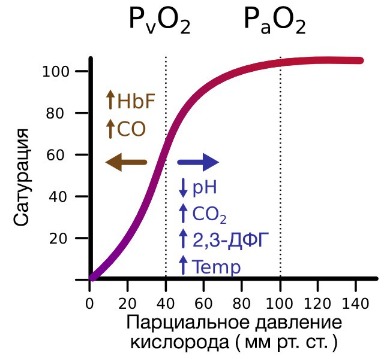
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
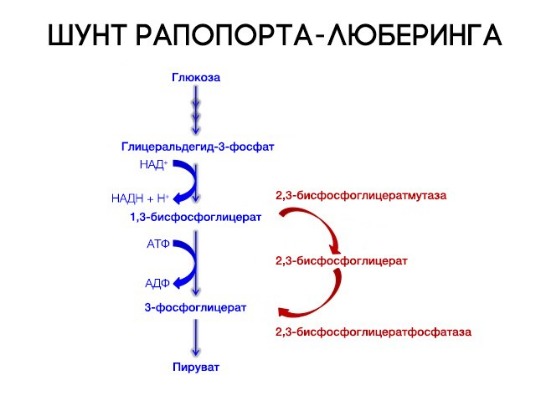
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник