Гемоглобин соединенный с кислородом
Содержание статьи
Гемоглобин и его соединения
Гемоглобин и его соединения
Гемоглобин – особый белок хромопротеида, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. У мужчин в крови содержится в среднем 130–160 г/л гемоглобина, у женщин – 120–150 г/л.
Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода. При этом валентность железа, к которому присоединяется кислород, не изменяется, т. е. железо остается двухвалентным. Гемоглобин, присоединивший к себе кислород, превращается в оксигемоглобин. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. Гемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. Гемоглобин, соединенный с углекислым газом, носит название карбгемоглобина. Это соединение также легко распадается. В виде карбгемоглобина переносится 20% углекислого газа.
В особых условиях гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином. Карбоксигемоглобин является прочным соединением. Гемоглобин блокирован в нем угарным газом и неспособен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни.
При некоторых патологических состояниях, например, при отравлении сильными окислителями (бертолетовой солью, перманганатом калия и др.) образуется прочное соединение гемоглобина с кислородом – метгемоглобин, в котором происходит окисление железа, и оно становится трехвалентным. В результате этого гемоглобин теряет способность отдавать кислород тканям, что может привести к гибели человека.
В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц.
Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. У плода содержится гемоглобин F. В эритроцитах взрослого человека преобладает гемоглобин А (90%). Различия в строении белковой части определяют сродство гемоглобина к кислороду. У фетального гемоглобина оно намного больше, чем у гемоглобина А. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови.
Ряд заболеваний связан с появлением в крови патологических форм гемоглобина. Наиболее известной наследственной патологией гемоглобина является серповидноклеточная анемия. Форма эритроцитов напоминает серп. Отсутствие или замена нескольких аминокислот в молекуле глобина при этом заболевании приводит к существенному нарушению функции гемоглобина.
В клинических условиях принято вычислять степень насыщения эритроцитов гемоглобином. Это так называемый цветовой показатель. В норме он равен 1. Такие эритроциты называются нормохромными. При цветовом показателе более 1,1 эритроциты гиперхромные, менее 0,85 – гипохромные. Цветовой показатель важен для диагностики анемий различной этиологии.
Читайте также
Гемоглобин
Гемоглобин
Обычно исследуют капиллярную кровь, которую получают путем укола иглой-скарификатором в мякоть IV пальца левой руки (реже – мочки уха) или венозную кровь из локтевой вены (при работе на автоматических анализаторах).За идеальную норму принимают концентрацию
Гликолизированный гемоглобин
Гликолизированный гемоглобин
Гликолизированный гемоглобин (HbAlc) – используется как показатель риска развития осложнений сахарного диабета. В соответствии с рекомендациями ВОЗ этот тест признан оптимальным и необходимым для контроля за качеством лечения
Гемоглобин
Гемоглобин
Норма: не обнаруживается («ОТРИЦАТЕЛЬНО»).NB! Положительный результат отражает присутствие свободного гемоглобина или миоглобина в моче. Это результат внутрисосудистого, внутрипочечного, мочевого гемолиза эритроцитов с выходом гемоглобина или повреждения и
Гемоглобин
Гемоглобин
Снижение содержания гемоглобина говорит об анемии. Она может развиться в результате потери гемоглобина при кровотечениях, при заболеваниях крови, сопровождающихся разрушением эритроцитов. Низкий гемоглобин также возникает вследствие переливания
Гликозилированный гемоглобин
Гликозилированный гемоглобин
Это биохимический показатель крови, отражающий среднее содержание сахара в крови за длительный период времени (до 3 месяцев), в отличие от исследования глюкозы крови, которое дает представление об уровне глюкозы крови только на момент
Гемоглобин
Гемоглобин
Норма: не обнаруживается («ОТРИЦАТЕЛЬНО»).
NB! Положительный результат отражает присутствие свободного гемоглобина или миоглобина в моче. Это результат внутрисосудистого, внутрипочечного, мочевого гемолиза эритроцитов с выходом гемоглобина или повреждения и
«ГЕМОГЛОБИН»
«ГЕМОГЛОБИН»
Вымойте говяжью печень, нарежьте ее ломтиками и слегка обжарьте на масле, чтобы она оставалась полусырой. Затем положите на ломтик черного хлеба и посыпьте сверху тертым сыром. На сыр положите ломтик сала и плотно, штука к штуке, уложите поверх сала маслины,
ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Фосфорорганические соединения снижают активность холинэстеразы в организме, что способствует накоплению ацетилхолина. Самый распространенный из фосфорорганических пестицидов – тиофос – представляет собой прозрачную бесцветную
ХЛОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ХЛОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Кроме желудочно-кишечного тракта, для хлорорганических пестицидов «входными воротами» служат дыхательные пути и слизистые оболочки. Большинство этих веществ являются жирорастворимыми, поэтому они могут накапливаться в жировой ткани
Гемоглобин
Гемоглобин
Гемоглобин (ИЬ) составляет 95% от белков эритроцита. Отсутствие ядра в эритроците предоставляет место для большего количества молекул гемоглобина. Это означает, что клетка может нести больше кислорода. Дело в том, что кислород очень плохо растворяется в плазме
Как увеличить гемоглобин
Как увеличить гемоглобин
Игнатьева Татьяна Во время беременности вы можете столкнуться и с так называемой «физиологической анемией», когда уровень гемоглобина опускается до 100 мг% (в норме для женщин 120–140 мг%). Это происходит из-за увеличения объёма крови, усиления
Фенольные соединения
Фенольные соединения
Эти вещества содержат ароматические кольца с гидроксильной группой, а также их функциональные производные. Фенольные соединения, в ароматическом кольце которых имеется более одной гидроксильной группы, называют полифенолами.Большинство
Скелет и его соединения
Скелет и его соединения
Скелет (от греч. skeleton – высохший, высушенный) – формообразующая конструкция тела – выполняет множество функций. Главными из них являются опора, защита, преодоление силы тяжести. Кости представляют собой систему рычагов, которые под влиянием
Источник
Гликированный гемоглобин и его норма

Гликированный гемоглобин – это один из показателей биохимического анализа крови. Позволяет выявить среднее значение уровня сахара в крови за последние три месяца. В анализах может обозначаться как HbA1C или A1C.
Содержание:
Кому и как часто нужно сдавать кровь на гликированный гемоглобин
Какой уровень HbA1C считается нормой
Как правильно сдавать анализ на гликированный гемоглобин
Знать его значение важно для того, чтобы своевременно выявить сахарный диабет,контролировать течение заболевания и эффективность применяемой терапии.
Кому и как часто нужно сдавать кровь на гликированный гемоглобин
Исследование крови на гликированный гемоглобин дает основные сведения о состоянии и намного удобнее иных анализов, позволяет выявить несоблюдение режима питания и плохой контроль сахара со стороны пациента.
Результат выражается в процентах. Например, уровень может быть 6,5%. Цифра показывает долю гемоглобина, соединившегося с глюкозой, то есть гликированного. Токсины, образующиеся в результате реакции в избытке, дают осложнения на почки, органы зрения и нижние конечности. Оставшиеся 93,5% вещества остаются свободными и продолжают доставлять кислород в ткани.
Для выявления гестационного диабета у беременных не подходит, так как показывает повышение сахара с опозданием. Анализ показан женщинам, планирующим рождение ребенка.
Всем здоровым людям по достижении 45 лет измерять показатель гликированного гемоглобина достаточно один раз в три года. Это позволит выявить диабет II типа на ранней стадии.
До 45 лет регулярная сдача анализа нужна при нахождении в группе риска:
По ожирению или нахождению на учете по излишней массе тела.
При малоподвижном образе жизни.
Если среди близких родственников есть страдающие сахарным диабетом.
При обнаружении толерантности к глюкозе или уровне гликированного гемоглобина более 5,7%.
При наличии диагноза артериальная гипертензия.
Если в период беременности был гестационный диабет.
Присутствует уменьшение чувствительности к инсулину.
При высоком риске развития сахарного диабета сдавайте анализ на установление уровня гликированного гемоглобина не режеодного раза в год.
При хорошо контролируемом течении, когда показатель удается удерживать на уровне не более 7%, анализ сдают раз в 6 месяцев.
На начальных этапах терапии и при изменении схемы лечения HbA1C контролируют ежеквартально.
Лицам старше 60 лет нужно сдавать анализ ежегодно, а при ухудшении зрения и общего самочувствия, подозрении на сахарный диабет – безотлагательно.
Какой уровень HbA1C считается нормой
Официальные нормы показателя одинаковы как для мужчин, так и для женщин. Не зависит он и от возраста с небольшими исключениями.
Нормальнымсчитается уровень гликированного гемоглобина до 5,7%. Лучшим считается показатель 5,5%.
Нахождение результата в диапазоне 5,7%-6,4% свидетельствует о риске развитиясахарного диабета II типа. В данном случае важно принять меры для снижения вероятности заболеть, проконсультироваться у врача. При уровне до 6% обязателен переход на низкоуглеводную диету.
Показатель 5,6-5,9% считается слегка повышенным, какие-либо симптомы нарушения обмена углеводов отсутствуют, но может присутствовать лишний вес.
При уровне HbA1C в пределах 6,1-6,4% некоторые специалисты уже ставят диагноз пред диабет и назначают лечение. Если пустить развитие болезни на самотек, то в течение 6-10 лет появятся проблемы с почками, зрением и ногами. Риск смерти от сердечно-сосудистого заболевания в таком случае повышается на 25%. Преддиабетическое состояние требует перехода на здоровый образ жизни.
По результату анализа, показавшему HbA1C более 6,5% возможен сахарный диабет, но требуются дополнительные исследования для подтверждения диагноза. Как правило, он подтверждается. Цифра 6,5-7,5% свидетельствует о патологии средней тяжести.
Для лиц с сахарным диабетомрекомендовано поддерживать показатель на уровне до 7%. Однако удерживание цифры в пределах 5,5-5,7% продлит жизнь и поможет избежать инвалидности.
Показатель от 8% свидетельствует о плохом контроле и стремительном развитии осложнений, вплоть до потери сознания и комы.
Установление и поддержание HbA1C в норме важно для снижения развития опасных осложнений:
Инфаркта и инсульта.
Диабетической ретинопатии или нейропатии, поражения почек.
У детей с сахарным диабетом желательно поддерживать показатель гликированного гемоглобина на уровне 5,4% до подросткового периода. Цифра 4-5,9% свидетельствует, что болезни нет. 6-7% — течение заболевания контролируется хорошо. При показателе от 7,1% фиксируется тяжелое состояние.
Как правильно сдавать анализ на гликированный гемоглобин
От пациента не требуется особой подготовки перед походом в лабораторию. Данный анализ необязательно сдавать натощак, можно перекусить и попить воды. Кровь берут из вены, а результат выдают на следующий день.
Если анализ сдается для выявления всех биохимических параметров крови, то принимать пищу перед сдачей не следует.
Чтобы получить достоверный результат, сдавайте кровь на исследование в независимой лаборатории, которая занимается диагностикой, но не лечением, и заинтересована в честном результате.
На показатель гликированного гемоглобина влияют имеющиеся заболевания и состояния, об их наличии в обязательном порядке нужно сообщить врачу на приеме.
Цифра может получиться завышеннойпри железодефицитной анемии. Занизитьреальный уровень могут:
кровотечения, которые были недавно или возникают периодически;
недавнее переливание крови;
некоторые болезни, например, гемолитические анемии различного генеза.
К сожалению, на протяжении длительного периода гликированный гемоглобин может быть выше нормы, но без проявления симптомов. Поэтому важно регулярно сдавать кровь на анализ и поддерживать показатель на уровне 5,5-5,7% как женщинам, так и мужчинам любого возраста.
Официальная медицина не признает опасность результата в пределах 6%. Но людям, желающим прожить дольше, лучше начинать лечение диабета в легкой форме. Результат свыше 6,5% дает право врачу ставить точный диагноз.
Источник
Гемоглобин: роль в газообмене и процессе дыхания
Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
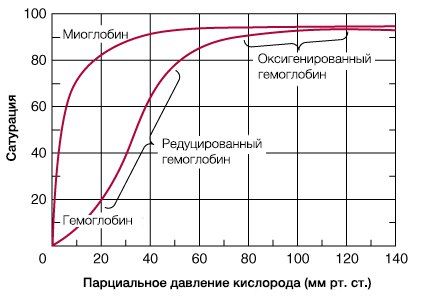
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
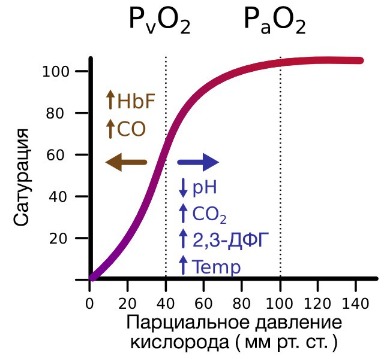
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
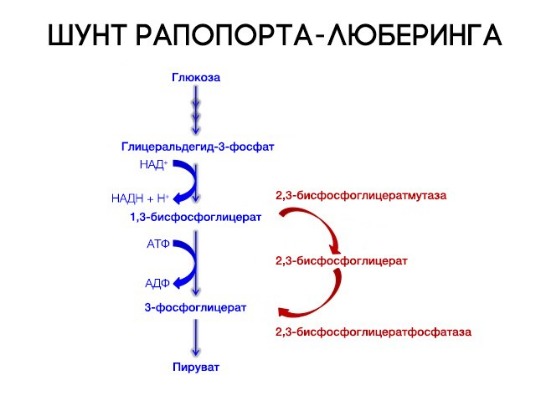
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник