Холестерин синтезируется в печени
Содержание статьи
Биосинтез холестерина
Биосинтез холестерина — образование в живом организме органического спирта холестерина стероидной природы. Синтез холестерина происходит в клетках печени (50 %), кишечнике и коже. В клетке он идёт в гладком эндоплазматическом ретикулуме и цитозоле. Биосинтез холестерина служит основой синтеза других стероидных соединений. Начальные этапы синтеза являются общими с этапами синтеза других изопреноидов.
Нумерация атомов в молекуле холестерина
В 1940-е годы Блох с сотр. установил, что все атомы углерода холестерина происходят из ацетата, причём оба атома включаются в одинаковых количествах. В настоящее время установлена следующая цепь биосинтеза холестерина, включающая в себя несколько ступеней. (Образование промежуточных соединений этого пути может происходить и другими способами).
- Превращение трёх молекул активного ацетата в пятиуглеродный мевалонат.
- Превращение мевалоната в активный изопреноид — изопентенилпирофосфат.
- Образование тридцатиуглеродного изопреноида сквалена из шести молекул изопентенилдифосфата.
- Циклизация сквалена в ланостерин.
- Последующее превращение ланостерина в холестерин.
Синтез мевалоната[править | править код]
Синтез мевалоната протекает в три этапа.
- Образование ацетоацетил-КоА из двух молекул ацетил-КоА с помощью тиолазного фермента ацетоацетилтрансферазы. Реакция обратима. Происходит в цитозоле.
- Образование β-гидрокси-β-метилглутарил-КоА из ацетоацетил-коА с третьей молекулой ацетил-КоА с помощью гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтазы). Реакция также обратима. Происходит в цитозоле.
- Образование мевалоната восстановлением ГМГ и отщеплением HS-KoA с помощью НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза). Происходит в гЭПР. Это первая практически необратимая реакция в цепи биосинтеза холестерина, а также она лимитирует скорость биосинтеза холестерина. Отмечены суточные колебания синтеза этого фермента. Активность его увеличивается при введении инсулина и тиреоидных гормонов, снижается при голодании, введении глюкагона, глюкокортикоидов.
Схема этапа:
Существуют и другие пути синтеза мевалоната.
Синтез изопентенилпирофосфата[править | править код]
1, 2. Вначале мевалоновая кислота дважды фосфорилируется с помощью АТФ: до 5-фосфомевалоната, а затем до 5-пирофосфомевалоната. 3. 5-пирофосфомевалонат фосфорилируется по 3 атому углерода, образуя нестабильный промежуточный продукт — 3-фосфо-5-пирофосфомевалонат. 4. Последний декарбоксилируется и дефосфорилируется, образуется изопентенилпирофосфат.
Синтез сквалена[править | править код]
- Изопентенилпирофосфат изомеризуется в диметилаллилпирофосфат.
- Конденсация изопентенилпирофосфата (С5) с диметилаллилпирофосфатом (С5) и образование геранилпирофосфата (С10). При этом высвобождается молекула пирофосфата.
- Конденсация изопентенилпирофосфата (С5) с геранилпирофосфатом (С10). Образуется фарнезилпирофосфат (С15) и высвобождается ещё одна молекула пирофосфата.
- Конденсация двух молекул фарнезилпирофосфата (С15) «голова-к-голове» и образование сквалена (С30). Реакция проходит с затратой НАДФН, и высвобождаются две молекулы пирофосфата. Молекулы фарнезилпирофосфата конденсируются концами, несущими пирофосфатные группы. Сначала отщепляется одна пирофосфатная группа и образуется промежуточный прескваленпирофосфат. Он, в свою очередь, восстанавливается с помощью НАДФН. Второй пирофосфат уходит. Образуется сквален.
Начиная со сквалена, продукты пути биосинтеза холестерина нерастворимы в водной среде и участвуют в дальнейших реакциях, будучи связанными со стеринпереносящими белками (СПБ).
Синтез ланостерина[править | править код]
1. Под действием скваленэпоксидазы образуется эпоксид сквалена. 2. Затем эпоксид сквалена циклизуется в ланостерин. При этом метильная группа у С14 переносится на С13, а метильная группа у С8 — на С14.
Синтез холестерина[править | править код]
Ланостерин превращается в мембранах гладкого эндоплазматического ретикулума в холестерин.
- Метильная группа при С14 окисляется, и образуется 14-десметилланостерин.
2. Затем удаляются ещё два метила при С4, и образуется зимостерол. 3. Далее двойная связь C8=С9 перемещается в положение С8=С7 и образуется Δ7,24-холестадиенол. 4. Двойная связь далее перемещается в положение С5=С6,образуется десмостерол. 5. После чего в боковой цепи восстанавливается двойная связь, и образуется холестерин.
(Восстановление двойной связи в боковой цепи может, однако, происходить и на предшествующих стадиях биосинтеза холестерола.)
Другие пути синтеза[править | править код]
У некоторых организмов при синтезе стероидов могут встречаться другие варианты реакций (например, немевалонатный путь образования пятиуглеродных молекул).
Литература[править | править код]
- [www.xumuk.ru/biologhim/169.html Химическая энциклопедия сайта www.humuk.ru. Скан учебника «Биологическая химия», Берёзов Т. Т., Коровкин Б. Ф.]
- Кольман Я., Рём К.-Г., «Наглядная биохимия», пер. с нем., М., «Мир», 2009.
- Марри Р., Греннер Д., Мейес П., Родуэлл В., «Биохимия человека». М., «Мир», 1993.
Промежуточные продукты метаболизма холестерина и стероидов | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Мевалонатный путь |
| ||||||||||||||
| Не-мевалонатный путь |
| ||||||||||||||
| В холестерин |
| ||||||||||||||
| Витамин D С-27: Холестаны |
| ||||||||||||||
| Жёлчные кислоты С-24: Холаны |
| ||||||||||||||
| Стероидные гормоны |
| ||||||||||||||
| Не у человека |
| ||||||||||||||
Примечания Н — нейростероидные гормоны см. также ферменты, заболевания | |||||||||||||||
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист. Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым). Список проблемных ссылок
|
Источник
Как связаны функции печени и холестерин?
Автор Хусаинов Руслан Халилович На чтение 3 мин. Опубликовано 19.06.2018 15:19 Обновлено 19.06.2018 15:19
Большая часть холестерина вырабатывает печень и он необходим для нашего здоровья. Но некоторые формы холестерина могут вызывать проблемы со здоровьем, включая повреждение печени.
Холестерин — жировая молекула, которая содержится в некоторых продуктах, а также в печени. Существуют два основных типа холестерина: липопротеины высокой плотности (ЛПВП) и липопротеины низкой плотности (ЛПНП) .
- ЛПНП должен быть менее 100 мг / дл
- ЛПВП должен составлять более 40 мг / дл
ЛПВП переносится из клеток организма в печень. Печень расщепляет их или выводит из организма в виде отходов.
Эта функция полезна для организма, поэтому ЛПВП иногда называют «хорошим холестерином».
ЛПНП переносятся из печени в клетки. Клетки используют холестерин, но слишком много его остается в артериях. Это может вызвать проблемы со здоровьем, поэтому врачи иногда называют ЛПНП «плохим холестерином».
Холестерин может накапливаться в артериях, в результате чего просвет их сужается, что ограничивает подачу крови и кислорода в органы. Сужение просвета артерий также увеличивает риск образования тромбов. Если кровоток к сердцу ограничен, то это может увеличить риск развития ишемической болезни сердца, сердечных приступов и сердечной недостаточности.
Если ограничен кровоток в головной мозг, то увеличивается риск развития инсульта.
Почему печень вырабатывает много плохого холестерин?
Существует множество различных заболеваний печени. Гепатиты, связанные с алкоголем, а также неалкогольная жировая болезнь печени являются одними из наиболее распространенных заболеваний печени.
Болезнь печени вызывает ее повреждение, и печень не в состоянии адекватно функционировать. Одной из функций печени является расщепление холестерина. Если печень не работает должным образом, это может привести к увеличению холестерина в организме.
Неалкогольная жировая болезнь печени может увеличить риск проблем со здоровьем, таких как инсульт или диабет. Если заболевание обнаружено на ранней стадии, то возможно предотвратить ухудшения.
Повышение холестерина — симптомы
Обычно высокий уровень холестерина не вызывает никаких симптомов. Но простой анализ крови покажет уровень холестерина.
Врач может рекомендовать тест на уровень холестерина, если у человека есть в семейном анамнезе заболевания сердца, диабет и избыточный вес.
Для диагностики заболевания печени обычно используется биопсия печени и тест на функции печени. При биопсии берется крошечный кусок ткани печени, чтобы проверить на наличие болезни. Тест на функцию печени — это анализ крови, который измеряет уровень белка и ферменты в крови. Уровни белков и ферментов могут показать, повреждена ли печень.
Лечение
Человек может изменить образ жизни и принимать препараты для снижения уровня холестерина. Как правило, ему будет предложено сначала изменить диету и выполнять физические упражнения. Если он имеет избыточный вес, то ему может быть рекомендовано снижение веса.
Наиболее распространенными препаратами для снижения уровня холестерина являются статины, которые человек должен принимать всю жизнь. Статины — это препараты, которые блокируют химическое вещество в печени, продуцирующее холестерин.
Лечение печени зависит от типа заболевания. Обычно оно связано с изменением образа жизни, препаратами, иногда прибегают к трансплантации печени, если печень повреждена.
Человеку, страдающему алкогольной болезнью печени, обычно рекомендуют отказ от алкоголя. Употребление достаточного количества белка и углеводов в составе сбалансированной диеты может помочь поддерживать нормальный вес.
Профилактика
- Можно предотвратить проблемы со здоровьем, такие как повреждение печени, путем снижения высокого уровня ЛПНП.
- Изменения диеты и физические упражнения помогут человеку управлять высоким уровнем холестерина.
Источник
Глава 4 Печень и обмен холестерина
Глава 4
Печень и обмен холестерина
Эволюционная роль холестерина заключается в том, что он служит каркасом клеточных мембран человека. Все цитоплазматические мембраны и мембраны органелл клеток млекопитающих и человека в основном состоят из фосфолипидов, гликолипидов и холестерина. Фосфолипиды являются пластичной, жидкой и фунциональной частью мембран, взаимодействуют с включенными в мембрану ферментами и рецепторами (рис. 12). Холестерин образует каркас клеточной мембраны, занимая свободное пространство между нерастворимыми в воде хвостами фосфолипидов и не позволят им изгибаться. Мембраны с низким содержанием холестерина — более гибкие и функционально активные, с высоким содержанием холестерина — более жесткие и инертные. Свободный (не этерифицированный и не связанный с липопротеидами) холестерин может свободно проникать в клеточные мембраны и образовывать эфиры с жирными кислотами, входящими в состав фосфолипидов, нарушая их функциональное состояние. Именно образование этого резервного компартмента холестерина, как и дефицит эссенциальных фосфолипидов, приводит к снижению вязкости и текучести, «старению» клеточных мембран и коррелирует с выраженностью атеросклероза. Таким образом, борьба с излишками холестерина в тканях и циркуляцией свободного холестерина в плазме для человека является эволюционной задачей, которую здоровый и молодой организм успешно решает путем его этерификации, включения в ЛПВП и транспортировки в печень для утилизации.
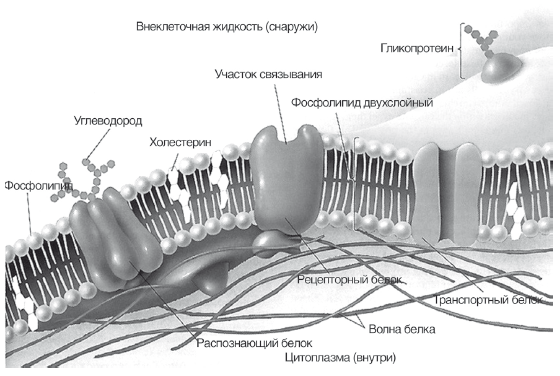
Рис. 12.
Виртуальная модель цитоплазматической мембраны клетки человека
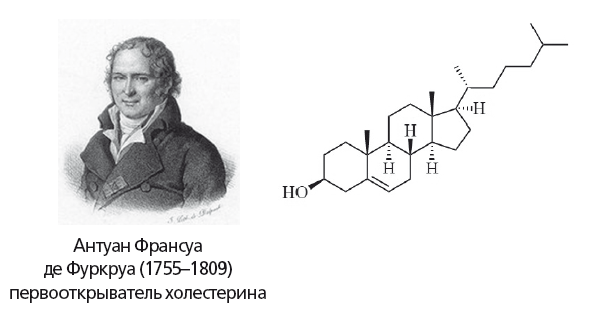
Рис. 13.
Формула холестерина. Холестерин обеспечивает стабильность клеточных мембран в широком интервале температур. Он необходим для выработки витамина D, стероидных и половых гормонов, а также для деятельности синапсов головного мозга и иммунной системы, включая защиту от рака
В 1769 году Пулетье де ла Саль из желчных камней получил плотное белое вещество («жировоск»), обладавшее свойствами жиров. В 1815 году Мишель Шеврёль также выделил это соединение и назвал его холестерином («холе» — желчь, «стерин» — жирный). Однако формулу и химические свойства холестерина установил Антуан Франсуа де Фуркруа. Холестерин и фосфолипиды (98 % их — фосфатидилхолин) составляют липидный комплекс желчи.
В сухом остатке желчи фосфатидилхолин (ФХ) составляет 22 %, а ХС — 4 %. В сутки через каналикулярную мембрану гепатоцита путем активного транспорта переносчиком фосфолипидфлиппазой (MDR3) или в составе фосфолипиднохолестериновых пузырьков и мицелл переносится 1,8-8,2 г ФХ. В кишечнике ФХ желчи расщепляется до лизофосфолипидов и реабсорбируется. Основная функция ФХ заключается в солюбилизации практически нерастворимого в воде ХС путем формирования ядра устойчивых простых (ФХ + холестерин, диаметр до 3 нм) или смешанных мицелл (ФХ + холестерин + желчные кислоты, диаметр 3-6 нм), а также везикул (ФХ + холестерин + желчные кислоты, диаметр 25-130 нм).
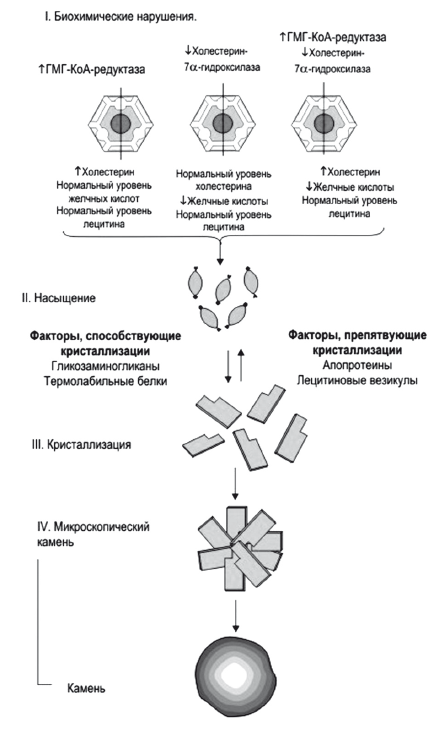
Рис. 14.
Растворимость холестерина в желчи
Потребность в холестерине в организме и печени зависит от активности человека — настройки симпато-адреналовой системы — человеку холестерин жизненно необходим для синтеза прогестерона, стероидных и половых гормонов, деятельности синапсов головного мозга, выработки витамина D. При стрессе и длительном напряжении в организме печень синтезирует много холестерина, который не весь расходуется на синтетические процессы и остается в виде эфиров в цитоплазме гепатоцита. Кроме того, длительное физическое и нервно-психическое напряжение может создать избыток холестерина в тканях преимущественно в форме ЛПНП. Высокое содержание (> 2 %) холестерина в пище также увеличивает фракцию ЛПНП и ЛПВП. При высоком содержании холестерина в пище синтез эндогенного холестерина в печени и других тканях ингибируется по механизму обратной связи.
В норме утилизация избытка холестерина касается только ЛПНП. Захват печенью циркулирующих в плазме ЛПНП — процесс активного транспорта через синусоидальную мембрану гепатоцита. После захвата ЛПНП скавендер-рецепторами гепатоцита они транспортируются в лизосомы, где из них высвобождается свободный холестерин, который используется для синтеза желчных кислот, стероидных гормонов и нейтральных стероидов или секретируется в желчь. Активная экскреция в желчь является основным физиологическим способом выведения избытков холестерина у человека (рис. 15). В сутки у человека образуется 500-1000 мл желчи. При относительно постоянном дебите желчи из организма человека в норме выводится до 1 г продуктов метаболизма холестерина в сутки.
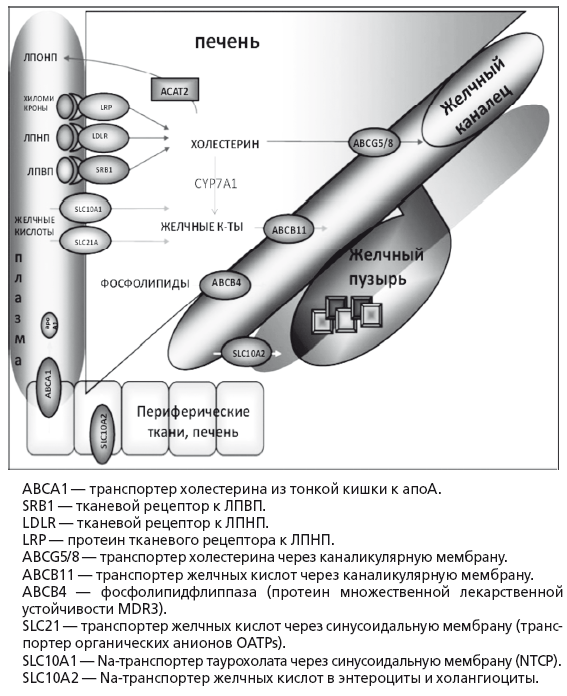
Рис. 15.
Транспорт основных метаболитов в печени (по Marschall HU, Einaon С, 2007)
Приблизительно половина этого количества экскретируется с фекалиями после превращения в желчные кислоты, оставшаяся часть представляет собой нейтральные стероиды. Холестерин секретируется в желчь активно, в желчные канальцы его переносит специальный насос ABCG5/8 (25). Поскольку холестерин не растворим в воде, его удержание в жидкой фракции желчи прямо зависит от концентрации эмульгирующих его желчных кислот и эссенциальных фосфолипидов — преимущественно ФХ, который обеспечивает его растворимость путем образования мицелл. При недостатке желчных кислот образуются более крупные частицы — везикулы, состоящие из лецитина и холестерина. При недостатке ФХ происходит кристаллизация холестерина и образуется желчный камень. Дефицит ФХ в желчи возникает при низком поступлении эссенциальных фосфолипидов или основной функциональной части — незаменимых полиненасыщенных жирных кислот (ПНЖК) в рационе питания. Относительный дефицит эссенциальных фосфолипидов также создается при их высоком потреблении гепатоцитами или другими тканями организма в печени при хронических воспалительных заболеваниях или интоксикациях, в частности, при хронической алкогольной интоксикации. Секреция в желчь холестерина, желчных кислот и ФХ — это энерго- и взаимозависимый, сложный процесс, который может нарушаться при первичном токсическом и аутоиммунном поражении гепатоцитов и холангиоцитов, а также лекарственном или инфекционном холестазе. Увеличение содержания холестерина в желчи форсирует синтез и секрецию в желчь эссенциальных фосфолипидов и базовых желчных кислот, без которых в желчи невозможно поддержание холестерина в растворимой форме и последовательно приводит к увеличению содержания всех этих веществ в тонкой кишке, крови воротной вены и фекалиях.
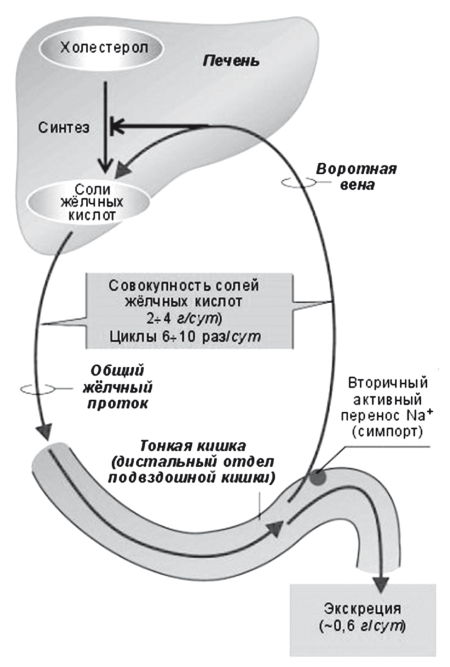
Рис. 16.
Схема энтерогепатической циркуляции желчных кислот
В процессе пассажа химуса по ЖКТ на всем протяжении кишечника всасывается до 90 % «съеденного» холестерина и реабсорбируется около 98 % желчных кислот и около 50 % холестерина, экскретированного с желчью. Оставшееся количество под действием микрофлоры толстой кишки превращается в стеролы, либо выводится с фекалиями, потому что связано с плохо растворимыми желчными кислотами (например, с литохолевой). Энтерогепатическая циркуляция желчных кислот протекает настолько эффективно, что суточная потеря желчных кислот с фекалиями составляет не более 500-1000 мг. Для восполнения потери первичные желчные кислоты — у человека холевая и хенодезоксихолевая кислоты — посредством фермента 7?-гидроксилазы (СУР7А1) постоянно синтезируются из холестерина в эндоплазматическом ретикулуме гепатоцитов, конъюгируются с глицином или таурином и активно секретируются в желчные канальцы (рис. 15). При помощи CYP7a в гепатоцитах из холестерина ежедневно синтезируются около 500 мг новых желчных кислот взамен тех, что были выведены с фекалиями (около 5 % общего пула). Этот метаболический путь является основным не только для синтеза желчных кислот, но и для утилизации избытков холестерина, поскольку приводит к утилизации около 80 % холестерина, циркулирующего в плазме (рис. 17).
Вторичные и третичные желчные кислоты: дезоксихолевая, литохолевая (около 1 % от общего пула желчных кислот) и урсодезоксихо-левая (< 3 % от общего пула желчных кислот) кислоты (УДХК) образуются из первичных желчных кислот под действием бактерий в толстой кишке и также частично реабсорбируются. Этот процесс тонко регулируется по механизму обратной связи — желчные кислоты синтезируются в гепатоците в точном соответствии с их потерей с фекалиями в энтерогепатической циркуляции. Интересно, что синтез желчных кислот более активно протекает в гепатоцитах III зоны печеночной дольки. Напротив, желчные кислоты, реабсорбируемые из кишечника и плазмы, концентрируются в гепатоцитах перипортальной зоны [36].
При увеличении потребности в синтезе нового холестерина в гепатоците активируется ген, кодирующий активность ключевого фермента ГМГ-КоА-редуктазы (рис. 17). Синтез первичных желчных кислот резко уменьшается. Это приводит к уменьшению секреции желчных кислот в желчь и снижению растворимости холестерина в желчи, притом что его концентрация в желчи увеличивается. В общем смысле этот механизм всегда сопутствует прогрессирующему атерогенезу, пожилому возрасту и терапии статинами. Таким образом, неудивительно, что у европейцев с сердечно-сосудистой патологией частота ЖКБ в 1,5 раза превышает среднюю во взрослой популяции, а в возрасте старше 71 года ЖКБ болеют около 14,3 % населения Европы и чаще — мужчины с ССЗ [36]. У представителей некоторых рас и этнических групп возможно также генетически детерминированное увеличение активности ГМГ-КоА-редуктазы: например, известна зависимость частоты ЖКБ от степени экспрессии американо-индейского гена. Накопление холестерина в гепатоцитах также может происходить при DOWN-регуляции CYP7a/
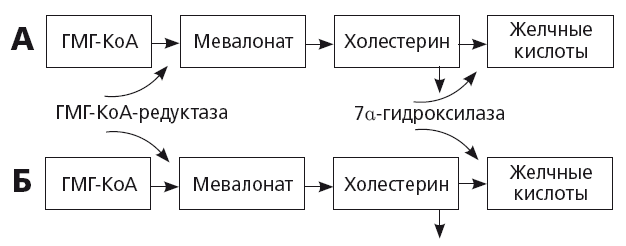
Рис. 17.
Регуляция секреции холестерина и желчных кислот у здоровых людей (А) и пациентов с ожирением и желчнокаменной болезнью (Б) [36]
Установлено, что активность CYP7a увеличивается при уровне холестерина в рационе более 2 %, и происходит это посредством активации ядерных рецепторов LXR, регулирующих экспрессию гена, кодирующего активность этого фермента. Напротив, активная реабсорбция желчных кислот из кишечника тормозит CYP7a и синтез желчных кислот по механизму отрицательной обратной связи и приводит к накоплению холестерина в гепатоцитах. Цель этого тонкого механизма — защита гепатоцитов и холангиоцитов от избыточного накопления желчных кислот, обладающих токсичным детергентным действием.
На первый взгляд, это плохо и тоже должно увеличивать литогенность желчи вследствие снижения секреции желчных кислот. Однако in vivo так не происходит. Изучение молекулярных механизмов ауторегуляции синтеза желчных кислот недавно привело к более тонкому пониманию ключевого регулирующего влияния желчных кислот на метаболизм холестерина, триглицеридов и самих себя. В 1999 году две независимые группы исследователей: в Японии — Makishima М. и соавторы и в Великобритании — Parks D.J. и соавторы почти одновременно опубликовали результаты исследований, впервые показавших, что соли желчных кислот являются прямыми активаторами ядерных рецепторов FXRa (NR1H4), которые регулируют экспрессию генов, участвующих в секреции, транспорте и метаболизме первичных желчных кислот, холестерина и триглицеридов как в гепатоцитах, так и в плазме. Посредством активации FXR желчными кислотами, поступающими из энтерогепатической циркуляции, и происходит подавление синтеза новых желчных кислот в цитозоле гепатоцита (рис. 18).
Активация FXR предотвращает накопление ТГ и ЛПОНП в печени, висцеральной клетчатке и плазме. При этом в печени действительно накапливается холестерин, который в данный момент «не нужен» для синтеза желчных кислот. Однако одновременно стимуляция FXR активирует экскрецию не этерифицированного холестерина в желчь при помощи переносчика ABCG5/8 [60]. Стимуляция FXR также увеличивает скорость захвата желчных кислот из плазмы посредством переносчиков ОАТР (SLC21) и NTCP (SLC10A1) и активирует экскрецию солей желчных кислот в первичные желчные канальцы переносчиком BSEP (АВСВ11). Одновременно стимуляция FXR активирует переносчик MDR3, секретирующий в желчь ФХ.
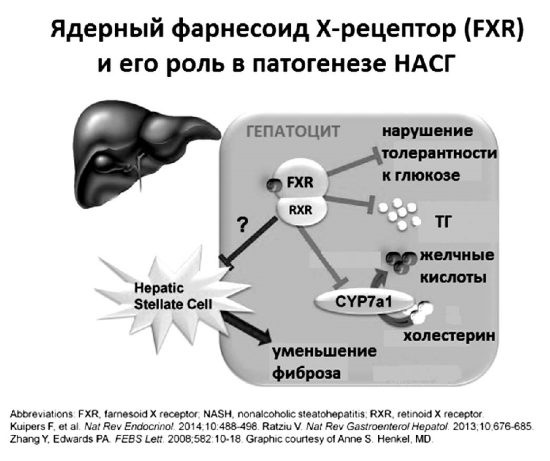
Рис. 18.
Ядерный фарнесоид Х-рецептор (FXR) и его роль в патогенезе НАСГ
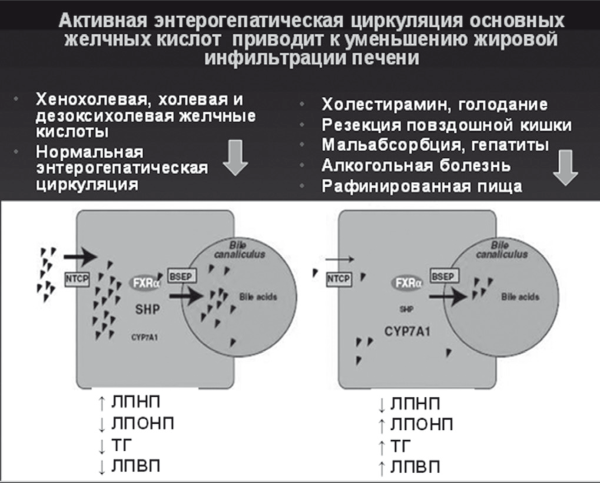
Рис. 19.
Эндокринная функция желчных кислот (модифицировано по S.M. Нouten, М. Watanabe, J. Auwerx, 2006)
Интегрально-активная энтерогепатическая циркуляция обеспечивает включение многокомпонентного механизма защиты гепатоцитов от токсичности желчных кислот при одновременном уменьшении сатурации холестерина в желчи и снижении риска образования желчных камней [60]. Позднее было установлено, что эндогенные желчные кислоты также являются сигнальными молекулами для синергичных FXR рецепторов TGR5 к G-протеину, которые находятся в тонкой кишке и опосредуют секрецию инкретинов. Стимуляция TGR5 желчными кислотами активирует активность щитовидной железы и энергообмен посредством увеличения секреции глюкагонподобных пептидов, которые препятствуют инсулинорезистентности [61]. В эксперименте на мышах оказалось, что добавление холевой кислоты к высококалорийному рациону позволяет предотвратить ожирение и развитие инсулинорезистентности путем увеличения липолиза в бурой жировой клетчатке. Таким образом, высокая реабсорбция желчных кислот при активной физиологической энтерогепатической циркуляции — как это происходит после приема холегенной и богатой жирами пищи — приводит к уменьшению синтеза желчи и накоплению в гепатоците ЛПНП, при одновременном уменьшении содержания ТГ и ЛПВП. Напротив, уменьшение всасывания желчных кислот (например, при голодании, применении секвестрантов, диарее любого происхождения) является сигналом к увеличению синтеза желчных кислот, для чего гепатоцит активно накапливает ТГ, ЛПОНП и ЛПВП. Другими словами, сбалансированный рацион питания, содержащий пищевые жиры и холеретики, служит надежной профилактикой образования желчных камней и развития жировой инфильтрации печени с дислипидемией и инсулинорезистентностью [60, 61].
Источник