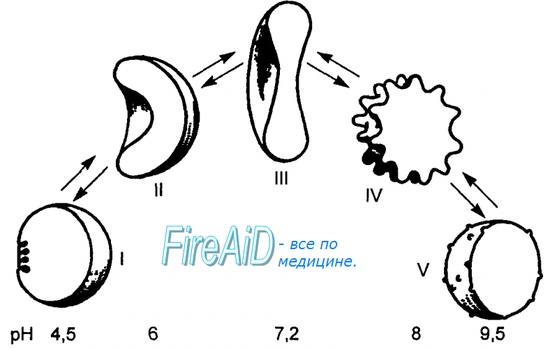
Эффект бора для гемоглобина
Содержание статьи
родство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
Оглавление темы «Вентиляция легких. Перфузия легких кровью.»: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. — Также рекомендуем «Углекислый газ. Транспорт углекислого газа.» |
Источник
иссоциация оксигемоглобина и ее зависимость. Эффект Бора
Диссоциация оксигемоглобина и ее зависимость. Эффект Бора
а) Факторы, сдвигающие кривую диссоциации оксигемоглобина. Их значение для транспорта кислорода. Кривые диссоциации оксигемоглобина (для облегчения понимания просим вас изучить рисунки ниже) справедливы для нормальной крови со средними показателями. Однако существует ряд факторов, которые могут сдвигать эту кривую в одну или другую сторону. На рисунке видно, что при некотором закислении крови со снижением рН от нормального уровня 7,4 до 7,2 кривая диссоциации смещается в среднем на 15% вправо, а повышение уровня рН от нормального уровня 7,4 до 7,6 смещает кривую на такое же расстояние влево.
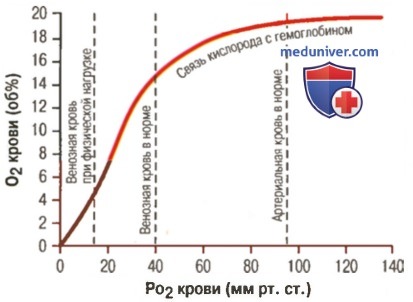
Влияние PO2 крови на количество связанного гемоглобина на 100 мл крови
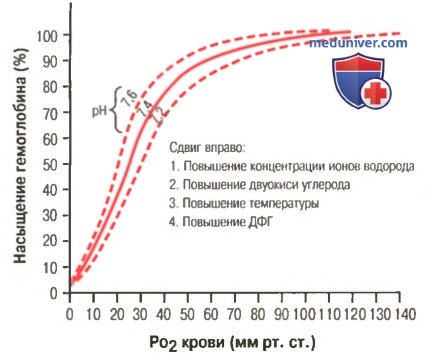
Сдвиг кривой диссоциации оксигемоглобина вправо в результате повышения концентрации ионов водорода (снижения pH). ДФГ — 2,3-дифосфоглицерат
Кроме изменений рН известны и другие факторы, которые могут сдвигать кривую диссоциации. Назовем три, действие которых сдвигает кривую вправо: (1) повышение концентрации двуокиси углерода; (2) повышение температуры крови; (3) повышение концентрации 2,3-дифосфоглицерата — метаболически важного фосфата, который в зависимости от метаболических условий присутствует в крови в разных концентрациях.
б) Повышение снабжения тканей кислородом в случаях, когда двуокись углерода и ионы водорода сдвигают кривую диссоциации оксигемоглобина. Эффект Бора. Сдвиг кривой диссоциации оксигемоглобина в ответ на повышение содержания двуокиси углерода и ионов водорода в крови имеет существенное влияние, выражающееся в ускорении высвобождения кислорода из крови в тканях и увеличении оксигенации крови в легких. Это называют эффектом Бора и объясняют его следующим образом.
При прохождении крови через ткань двуокись углерода диффундирует из клеток ткани в кровь. В результате в крови увеличивается PO2, а затем концентрации угольной кислоты (H2CO3) и ионов водорода. Эти изменения сдвигают кривую диссоциации оксигемоглобина вправо и вниз (для облегчения понимания просим вас изучить рисунок выше), уменьшая сродство кислорода к гемоглобину, и в результате увеличивается выход кислорода в ткани.
При диффузии двуокиси углерода из крови в альвеолы происходят процессы обратного направления — в результате в крови снижаются PCO2 и концентрация ионов водорода, сдвигая кривую диссоциации оксигемоглобина влево и вверх. При этом значительно увеличивается количество кислорода, связывающегося с гемоглобином при любом существующем уровне альвеолярного PO2, что увеличивает транспорт кислорода к тканям.
в) Сдвиг кривой диссоциации оксигемоглобина под влиянием дифосфоглицерата. Нормальное содержание ДФГ в крови вызывает постоянный небольшой сдвиг кривой диссоциации оксигемоглобина вправо. В случае гипоксического состояния, продолжающегося более нескольких часов, концентрация ДФГ в крови значительно возрастает, и кривая диссоциации оксигемоглобина сдвигается вправо еще больше.
В присутствии такой концентрации ДФГ кислород в тканях высвобождается при PO2, превышающем нормальный уровень на 10 мм рт. ст., поэтому в некоторых случаях такой механизм с участием ДФГ может оказаться важным для адаптации к гипоксии, особенно если причиной гипоксии является уменьшение в ткани кровотока.
г) Сдвиг кривой диссоциации во время физической нагрузки. Во время физической нагрузки некоторые факторы вызывают значительный сдвиг кривой диссоциации оксигемоглобина вправо, поэтому активные, выполняющие физическую работу мышечные волокна получают дополнительное количество кислорода. В свою очередь, работающие мышцы высвобождают большое количество двуокиси углерода; это в совокупности с действием некоторых других кислот, высвобождающихся мышцами, повышает концентрацию ионов водорода в крови капилляров мышц.
Кроме того, во время работы температура мышцы часто повышается на 2-3°С, что может еще больше увеличивать доставку кислорода мышечным волокнам. Все эти факторы вызывают значительный сдвиг кривой диссоциации оксигемоглобина в крови капилляров мышц вправо. Сдвиг вправо означает высвобождение кислорода гемоглобином в мышце при достаточно высоком уровне PO2 (40 мм рт. ст.) даже в случаях, когда из него уже высвободилось 70% кислорода. Сдвиг кривой в другую сторону показывает, что в легких присоединилось дополнительное количество кислорода из альвеолярного воздуха.
— Также рекомендуем «Участие кислорода в метаболизме. Метаболическое потребление кислорода»
Оглавление темы «Кислород и его доставка в организме»:
1. Диффузия газов через дыхательную мембрану. Дыхательная мембрана
2. Емкость дыхательной мембраны. Диффузионная емкость для кислорода
3. Вентиляционно-перфузионный коэффициент. Парциальное давление кислорода и двуокиси углерода
4. Концепция физиологического шунта. Концепция физиологического мертвого пространства
5. Обмен кислорода в организме. Транспорт кислорода из легких в ткани
6. Транспорт кислорода артериальной кровью. Диффузия кислорода
7. Гемоглобин. Роль гемоглобина в транспорте кислорода
8. Коэффициент использования кислорода. Сохранение постоянства кислорода в тканях
9. Диссоциация оксигемоглобина и ее зависимость. Эффект Бора
10. Участие кислорода в метаболизме. Метаболическое потребление кислорода
Источник
ВЕРИГО ЭФФЕКТ — Большая Медицинская Энциклопедия
ВЕРИГО ЭФФЕКТ (Б. Ф. Вериго, отечественный физиолог, 1860— 1925), Вериго—Бора эффект, Бора эффект, — зависимость степени диссоциации оксигемоглобина от величины парциального давления углекислоты (pCO2) в крови. При снижении pCO2 в альвеолярном воздухе и крови сродство кислорода к гемоглобину повышается, что затрудняет переход кислорода из капилляров в ткани (см. Газообмен). Этот эффект был отмечен двумя исследователями независимо друг от друга: рус. физиологом Б. Ф. Вериго (1898) и дат. физиологом Бором (Ch. Bohr, 1904), поэтому правильнее называть его эффектом Вериго. В статьях, публикуемых за рубежом, большинство авторов обозначает это явление как эффект Бора, т. к. работа Б. Ф. Вериго мало кому была известна. О ней упоминают только Дж. Холдейн и Пристли (J. Priestley). В дальнейшем В. э. был исследован Дж. Баркрофтом (1910— 1929), который установил определенную зависимость величины сдвигов кривой диссоциации оксигемоглобина от величины pCO2 и pH крови.
Физиол, значение В. э. отмечено многими исследователями. Так, П. М. Альбицкий (1911) выдвинул гипотезу, согласно к-рой pCO2 в крови является важнейшим регулятором интенсивности окислительных процессов в тканях. При снижении pCO2 скорость обменных процессов возрастает, а при увеличении — понижается. Этим, в частности, может быть объяснено наркотическое действие высоких концентраций углекислоты во вдыхаемом воздухе.
В случае развития гипоксии (см.) возникающая гипервентиляция приводит, с одной стороны, к повышению содержания кислорода в крови, а с другой — к снижению поступления его в ткани. Повышенное содержание кислорода в крови уменьшает возникающий при гипоксии цианоз кожи и слизистых оболочек, однако не улучшает состояние организма. При этом необходимо иметь в виду, что гипервентиляция приводит не только к В. э., но и к сужению кровеносных сосудов, преимущественно сосудов головного мозга, что само по себе может быть причиной кислородного голодания.
По мнению Холдейна, терапевтическое действие от добавления углекислоты к вдыхаемой газовой смеси при гипоксии также в определенной степени связано с В. э.
Биохим, механизм, определяющий развитие В. э., долгое время оставался недостаточно изученным. Л. А. Орбели и Баркрофт в 1910 г. установили, что сдвиг кривой диссоциации оксигемоглобина зависит как от изменений pH среды, так и от специфического действия углекислоты. Рерт (М. Rorth, 1968) и Бауэр (Ch. Bauer, 1969) показали, что на кривую диссоциации оксигемоглобина влияет и дифосфоглицериновая к-та. Благодаря присутствию последней кривая диссоциации оксигемоглобина приобретает S-образную форму. Установлено, что дифосфоглицериновая к-та присоединяется между X-концам и бета-цепей дезоксиформы гемоглобина электростатической связью, прочность к-рой зависит от pH и ионной силы среды. При оксигенации расстояние между концами двух (3-цепей гемоглобина увеличивается и происходит разрыв связи между гемоглобином и дифосфоглицериновой к-той. Одновременно два Н-завитка сближаются и выталкивают молекулу дифосфоглицериновой к-ты, что приводит к снижению pH. При появлении повышенного количества углекислоты в крови оксигенация сопровождается отщеплением протона и изменением pH. Совокупность этих процессов выражается в форме В. э.
См. также Газообмен, Гемоглобин.
Библиография: Альбицкий П. Об обратном действии или «последействии» углекислоты и о биологическом значении С02, обычно содержащейся в организме, Изв. Воен.-мед. акад., т. 22, № 2, с. 117, № 3, с. 227, №4, с. 357, №5, с. 601, 1911; Вериго Б. Ф. Основы физиологии человека и высших животных, т. 1—2, Спб., 1905 — 1909: Холден Дж. С. и Пристли Д ж. Г. Дыхание, пер. с англ., М.— Л., 1937, библиогр.: В а г-croft J. The respiratory function of the blood, v. 1, pt 1, Cambridge, 1925: Bauer Ch. Antagonistic influence of C02 and 2,3 diphosphoglycerate on the Bohr effect of human haemoglobin, Life Sci., v. 8, pt 2, p. 1041, 1969, bibliogr.; Bohr C., Hasselbalch K. u. К г о g h A. tiber einen in biologischer Beziehung wichtigen Einfluss, den die Kohlensaurespannung des Blutes auf dessen Sauerstoffbindung ausubt, Skand. Arch. Physiol. ,Bd 16, S. 402, 1904; V e r i go B.F. Quelques remarques relatives en memoire de m.m. A. Rodet et J. Nicolas: Recherches experimentales sur les modifications subies par une masse gaseuse injectee dans les tissues, Arch, Physiol., t. 10, p. 610, 1898.
В. Б. Малкин.
Источник: Большая Медицинская Энциклопедия (БМЭ), под редакцией Петровского Б.В., 3-е издание
Рекомендуемые статьи
Источник
Эффект Вериго — Бора — Википедия Переиздание
Мы немного порассуждали о лёгких и тканях,
и о том, какие же между ними отношения,
когда они пытаются посылать туда-обратно маленькие молекулы
и в это же время отправлять тканям кислород.
Ткань же пытается найти самый эффективный способ отправить обратно углекислый газ.
Это и есть 2 основных процесса, которые происходят между лёгкими и тканями.
Мы уже говорили о том, что есть 2 основных пути получения кислорода.
Первый — самый лёгкий — растворённый кислород.
Растворённый в крови кислород.
Но это не основной путь.
Основной — связывание кислорода с гемоглобином
и образование HbO2, молекулы под названием оксигемоглобин.
Именно так большинство кислорода попадает в ткани.
С другой стороны от тканей в лёгкие переносится
растворённый углекислый газ,
небольшое количество которого переносится прямо в плазме.
Однако, это не основной путь обратной поставки углекислого газа.
Самый эффективный путь доставки углекислого газа в лёгкие —
протонированная форма гемоглобина.
Когда я говорил о протонированной форме гемоглобина,
я упоминал, что плазма содержит бикарбонат.
Суть процесса заключается в том, что
возвращаясь в лёгкие, протон и бикарбонат
снова встречаются и образуют СО2, а также воду,
это происходит благодаря содержащемуся в красных клетках крови ферменту под названием
карбоангидраза.
Это и есть основной путь доставки углекислого газа в лёгкие.
Конечно, есть ещё и 3-ий, заключающийся в том, что гемоглобин
связывается непосредственно с углекислым газом в процессе и
образуется маленький протон,
который участвует здесь.
Он также может связываться с гемоглобином.
Среди такого взаимодействия я бы хотел привлечь ваше внимание к тому,
что гемоглобин может связываться с кислородом
также как и с протонами.
Самое интересное здесь то, что происходит что-то вроде соревнования.
Происходит, так сказать, небольшая игра.
С одной стороны, у вас есть гемоглобин, связывающийся с кислородом
(я нарисую его дважды),
и это, в свою очередь, приводит к взаимодействию с протоном,
который, в свою очередь, пытается выхватить гемоглобин.
Происходит небольшое соревнование за гемоглобин,
в котором кислород не участвует,
а углекислый газ вступает в реакцию, о которой мы уже говорили.
Небольшое количество гемоглобина связывается с углекислым газом, в результате чего образуется протон,
но и в этом процессе кислород не участвует.
Поэтому происходящая реакция напрямую зависит от того,
каких молекул в данный момент больше:
кислорода, протона или углекислого газа.
В зависимости от того, каких молекул больше
в ткани или клетке, происходит соответствующая реакция.
Учитывая это, я мог бы вернуться назад и сказать, что
я думаю, углекислый газ и протон влияют на кислород.
Я мог бы сказать, что и углекислый газ, и протон
действительно влияют
на избирательное стремление гемоглобина к соединению.
Повторю, избирательное стремление гемоглобина к соединению
или на его желание связываться с кислородом.
Это один из выводов, который вы бы могли сделать, наблюдая за таким соревнованием.
Представив это, я думаю, можно сказать,
что кислород (в зависимости от того,
какой точки зрения вы придерживаетесь) влияет на
избирательное стремление гемоглобина к соединению с
углекислым газом или протоном.
Итак, избирательное стремление гемоглобина к соединению с углекислым газом или протоном.
Я хочу подчеркнуть, что независимо от точки зрения,
которой вы придерживаетесь, оба эти утверждения верны.
Мы можем решить, что, возможно, просто повторяем одно и то же дважды.
Но на самом деле это два разных факта, каждый из которых называется по-своему.
Первый случай, когда мы говорим о реакции углекислого газа и протонов,
называется «эффект Бора».
Вы можете встретить это название или описание.
Это эффект Бора.
И второй случай, если мы посмотрим на наш процесс с точки зрения кислорода,
то реакция будет называться «эффект Холдейна».
Что же такое эффект Бора и эффект Холдейна,
кроме того, что это соревнование за гемоглобин?
Давайте я подниму экран,
и посмотрим, смогу ли я их изобразить.
Я считаю, что небольшой рисунок или схема действительно помогают объяснить такие вещи.
Я буду использовать небольшой график. Посмотрим, смогу ли я на нём изобразить эффект Бора.
Это парциальное давление кислорода, то есть то, сколько кислорода растворяется в плазме.
И это содержание кислорода, которое показывает, сколько всего кислорода в крови,
что, конечно, учитывает в основном количество кислорода, связавшегося с гемоглобином.
Что же будет, если я медленно увеличу парциальное давление кислорода?
Вначале лишь несколько молекул кислорода свяжется с гемоглобином,
но как только это произойдёт, возникнет кооперативный эффект,
и потихоньку наклон кривой начнёт увеличиваться и станет более резким.
Такая реакция обусловлена кооперативным эффектом,
так как кислород вступает в реакцию там, где уже произошла реакция с его молекулами.
Затем кривая выравнивается.
Выравнивание происходит в результате насыщения гемоглобина.
Так как остаётся мало свободного места,
необходимо, чтобы в плазме растворилось много кислорода,
который сможет тщательно поискать и найти оставшиеся свободные места на гемоглобине.
Предположим, мы выбрали 2 зоны.
Одна зона богата растворённым в крови кислородом,
а во 2-ой наблюдается недостаток растворённого в крови кислорода.
Это произвольный выбор,
поэтому не следует беспокоиться о точном количестве.
Если вы подумаете, где в организме наблюдается максимальное скопление кислорода, то
естественно, это будут лёгкие, где в крови растворено много кислорода.
И низкое количество кислорода наблюдается в бедренной мышце, например, где много СО2,
но в крови растворено мало кислорода.
И так, это две части тела, и теперь,
глядя на эту кривую, вы можете узнать,
сколько кислорода доставляется в бедро.
Это легко. Я мог бы сказать,
сколько кислорода в лёгких или в кровеносном сосуде, отходящем от лёгких…
Итак.
Вот это — количество кислорода в кровеносных сосудах, идущих от лёгких.
Вот это — количество кислорода в кровеносном сосуде, идущем от бедра.
Разница между этими двумя значениями —
это и есть количество поставляемого кислорода.
Поэтому, если вы хотите вычислить, сколько кислорода поставляется в ткань,
вы должны просто вычесть эти два значения,
это и будет количество поставляемого кислорода.
Глядя на эти два значения, вы можете заинтересоваться тем,
что произойдёт, если вы захотите повысить поставку кислорода.
Предположим, что по какой-то причине необходимо сделать этот процесс более эффективным,
в этом случае всё, что можно сделать, — это
увеличить гипоксию в бедре (на графике вы движетесь влево)
или, другими словами, уменьшить количество имеющегося кислорода.
Итак, при повышении гипоксии в бедре,
(точка на графике станет ниже),
увеличится количество поставляемого кислорода.
Однако это не идеальный вариант, так как нехватка кислорода в бедре
вызывает боль.
Есть ли другой способ увеличения поставки кислорода
без гипоксии или уменьшения количества кислорода в ткани?
Существует ли такой способ поставки кислорода?
Здесь и вступает в игру эффект Бора.
Давайте вспомним: эффект Бора заключается во влиянии СО2 и протона на связь гемоглобина с кислородом.
Дело состоит в том (я буду помечать это зелёным цветом), что
в этой ситуации у нас много углекислого газа и протонов,
это и есть эффект Бора, когда кислороду труднее связаться с гемоглобином.
Если я изображу другую кривую,
изначально она будет менее выраженной, так как ещё меньшее количество кислорода связано с гемоглобином.
Но как только концентрация кислорода достаточно увеличится,
кривая начнёт подниматься и подниматься, и, в конечном счёте, кислород будет связываться с гемоглобином,
то есть, нет такого, что он бы совсем не связывался с ним в присутствии углекислого газа и протонов,
просто это займёт больше времени.
При этом кривая выглядит так, как будто её сместили.
Такие условия с высоким содержанием СО2 и протонов,
которые, по сути, не подходят для лёгких.
Лёгкие, думают: «Кого это волнует? У нас нет таких условий».
Но для бедра, это подходит.
Так как в бедре много СО2 и протонов.
Вспомните, большое количество протонов означает низкий рН.
Это можно рассмотреть с разных точек зрения.
То есть, с бедром — другой случай.
Ему соответствует не зелёная, а синяя кривая.
Поэтому мы сможем изобразить точку на том же самом уровне О2 но ниже.
Каково же содержание О2 в крови, направляющейся из бедра?
Если всё сделать правильно, на кривой это будет отображаться здесь.
Это фактическое количество, при этом доставленное количество О2 становится более впечатляющим.
Посмотрите, из-за эффекта Бора поставка О2 увеличилась.
Если вы захотите узнать, насколько точно она увеличивается,
я покажу — это будет количество отсюда до сюда,
другими словами, — вертикальное расстояние между зелёной и голубой линиями
это и есть дополнительное количество поставленного из-за эффекта Бора кислорода.
Вот почему эффект Бора так важен,
Ведь, по сути, он помогает нам поставлять кислород в ткани.
Итак, теперь давайте по тому же принципу
рассмотрим эффект Холдейна.
Фактически мы должны всё поменять местами, поэтому поменяются и оси, и единицы измерения.
Здесь у нас будет количество углекислого газа,
а здесь — содержание углекислого газа в крови.
Давайте поразмышляем об этом эффекте.
Начнём с медленного, но уверенного увеличения количества углекислого газа
и посмотрим, как увеличивается его концентрация.
С увеличением количества углекислого газа
его концентрация в крови увеличивается прямо пропорционально.
Кривая не имеет S-образной формы, как кривая кислорода,
потому что при связывании с гемоглобином нет кооперативного эффекта.
Содержание углекислого газа просто увеличивается прямо пропорционально его количеству.
Это достаточно легко.
Теперь давайте возьмём два случая, как мы делали ранее.
Здесь будет высокое содержание СО2 в крови,
а здесь низкое содержание СО2 в крови.
В какой же ткани будет низкое содержание СО2 в крови?
Низкое содержание СО2 находится, конечно, в лёгких,
так как здесь мало углекислого газа.
А высокое содержание СО2 возможно в бедре, так как бёдра — это маленькие фабрики по производству СО2.
Поэтому в бёдрах высокое содержание СО2, а в лёгких — низкое.
Если необходимо узнать количество поставленного СО2, то нужно повторить то, что мы делали ранее.
Итак, высокое количество СО2 в бёдрах — это высокое количество СО2 в крови.
А это количество СО2 в крови, направляющейся от бёдер к лёгким.
Поэтому количество поставленного из бёдер в лёгкие СО2 —
это разница этих двух значений. Вот так мы можем рассчитать количество фактически поставленного СО2.
Так же как и поставка О2, наблюдается поставка большого количества СО2.
Теперь давайте перечитаем эффект Холдейна, и посмотрим, что произойдёт,
если мы изобразим ещё одну линию при наличии большого количества кислорода?
Высокая концентрация кислорода меняет
избирательное стремление гемоглобина к связыванию с углекислым газом и протонами.
Поэтому прямо пропорционально количеству гемоглобина снизится количество связанных протонов и углекислого газа.
А это означает снижение содержания СО2
при любом его количестве, растворённом в крови.
Поэтому эта линия всё ещё прямая, но вы можете заметить, что она действительно снижается по наклонной.
И где же это возможно, в каких случаях такое происходит?
Давайте попытаемся определить, где же максимальное количество кислорода?
Это, конечно, не бёдра, так как
в бёдрах мало кислорода.
Но это подходит лёгким.
Даже очень.
Теперь вы скажете: «Давайте посмотрим, что же происходит?
Сколько же поставляется СО2 при высокой концентрации О2?»
Возможно, вы уже заметили, что оно будет больше?
Так как при высокой концентрации О2, количество поставляемого СО2 непрерывно увеличивается.
Это и будет новое количество поставленного СО2.
То есть, вы даже можете узнать точное количество поставленного СО2.
Необходимо узнать разницу этих двух значений,
в чём, по сути, и заключается эффект Холдейна.
Вот так наглядно можно рассмотреть этот эффект.
И так, эффект Бора и эффект Холдейна — две важные стратегии, которых придерживается наш организм
для увеличения количества поставляемого О2 и выводимого СО2
между лёгкими и тканями.
Источник