Ключевые ферменты синтеза холестерина
Содержание статьи
Синтез холестерола должен быть согласован с его выведением
Синтез холестерола в организме составляет примерно 0,5-0,8 г/сут, примерно 50% образуется в печени, около 15% в кишечнике. Все клетки организма способны синтезировать холестерол. Поступление с пищей составляет около 0,4 г/сут.
Единственным реальным способом выведения холестерола является желчь – до 1 г/сут.
Биосинтез холестерола
Биосинтез холестерола происходит в эндоплазматическом ретикулуме. Источником всех атомов углерода в молекуле является ацетил-SКоА, поступающий сюда из митохондрий в составе цитрата, также как при синтезе жирных кислот. При биосинтезе холестерола затрачивается 18 молекул АТФ и 13 молекул НАДФН.
Образование холестерола идет более чем в 30 реакциях, которые можно сгруппировать в несколько этапов.
1. Синтез мевалоновой кислоты.
Первые две реакции синтеза совпадают с реакциями кетогенеза, но после синтеза 3-гидрокси-3-метилглутарил-SКоА вступает в действие фермент гидроксиметил-глутарил-SКоА-редуктаза (ГМГ-SКоА-редуктаза), образующая мевалоновую кислоту.
2. Синтез изопентенилдифосфата. На этом этапе при использовании АТФ мевалоновая кислота трижды фосфорилируется. Затем промежуточный продукт декарбоксилируется и дефосфорилируется с получением изопентенилдифосфата.
3. После объединения трех молекул изопентенилдифосфата (если не считать промежуточных превращений) синтезируется фарнезилдифосфат.
4. Синтез сквалена происходит при связывания двух остатков фарнезилдифосфата.
5. После сложных реакций линейный сквален циклизуется в ланостерол.
6. Удаление лишних метильных групп, восстановление и изомеризация молекулы приводит к появлению холестерола.
Регуляция синтеза
Регуляторным ферментом является гидроксиметилглутарил-SКоА-редуктаза, активность которой может изменяться в 100 и более раз.
1. Метаболическая регуляция – по принципу обратной отрицательной связи фермент аллостерически ингибируется конечным продуктом реакции – холестеролом. Это помогает поддерживать внутриклеточное содержание холестерола постоянным.
2. Регуляция транскрипции гена ГМГ-SКоА-редуктазы (в печени) – холестерол и желчные кислоты подавляют считывание гена и уменьшают количество фермента.
3. Ковалентная модификация при гормональной регуляции:
- Инсулин, активируя протеин-фосфатазу, способствует переходу фермента в активное состояние.
Важным следствием такой регуляции является активация кетогенеза при отсутствии инсулина.
- Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму.
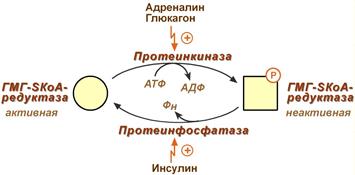
Регуляция активности гидроксиметилглутарил-S-КоА-редуктазы
Кроме указанных гормонов, на ГМГ-SКоА-редуктазу действуют эстрогены и тиреоидные гормоны (повышают активность) и глюкокортикоиды (снижают активность).
Изменение транскрипции гена ГМГ-КоА редуктазы (генетическая регуляция) осуществляется стерол-регулируемым элементом в ДНК (SREBP, sterol regulatory element-binding protein) с которым способны связываться белки — факторы SREBP. Эти факторы при достаточном количестве холестерина в клетке закреплены в мембране ЭПР. Когда уровень холестерина падает, факторы SREBP активируются под действием специфичных протеаз комплекса Гольджи, передвигаются в ядро, взаимодействуют на ДНК с участком SREBP и стимулируют биосинтез холестерина.
Скорость биосинтеза холестерола также зависит от концентрации специфического белка-переносчика, обеспечивающего связывание и транспорт гидрофобных промежуточных метаболитов синтеза.
Источник
Синтез холестерина: нарушения обмена, цикл создания
Постоянный синтез холестерина в организме обеспечивает работа печени. Но, кроме этого, источником соединение выступает кишечник, где обрабатывается и синтезируется липид. Реакция также происходит в коже человека. Важная роль холестерина и его функции значительна. Он позволяет вырабатывать витамин Д и гормоны. Но избыток приводит к накоплению холестерола, что опасно для работы сердца.
Общая характеристика
Холестерин получил название в 1769 году от французского химика Пулетье де ла Саль. Первоначально слово обозначало выработку вещества, которую выделяли желчные камни. В буквальном смысле его стоит переводить как «твердая желчь». Но со временем ученые доказали, что вещество — это природный спирт, поэтому корректнее его называть холестерол. Экзогенный холестерин необходим организму для выработки витамина Д, он обеспечивает энтерогепатический оборот желчных кислот, для создания клеточных мембран и транспортировки эйкозаноидов. Схема создания липида сложная и включает несколько этапов.
Вернуться к оглавлению
Где синтезируется?
Синтез холестерина происходит в таких частях тела:
- кожа;
- кишечник;
- печень.
Биосинтез холестерина — один из важнейших процессов, который происходит в теле человека. Большую часть (выше 50%) экзогенного холестерина синтезирует печень, потому что это регуляторный источник цитозоли и эндоплазматического ретикулюма. В этом же органе начинается производство гликогена. Ресинтез происходит в кишечнике: жирные кислоты соединяются со спиртами и поступают в кровь, что позволяют уменьшить их дегенеративное влияние на мембраны. Активность выработки зависит от наличия в организме сериодов, витамина D и некоторых соединений, которые отвечают за транспортировку веществ. Основные этапы метаболизма и пути использования — это производство мевалоновой кислоты, изопентенилпирофосфата, сквалена, ланостерина, холестерина.
Вернуться к оглавлению
Цикл создания
Последовательность создания и обмена холестерина в организме всегда строго одинакова.
Особенности обмена холестерина в организме человека заключаются в сложности его создания. Последовательность всегда строго одинакова. В этом процессе участвуют ферменты, которые проходят несколько биохимических действий. Нарушение цикла грозит недостатком или избытком липида, что приводит к серьезным заболеваниям.
Вернуться к оглавлению
Синтез мевалоновой кислоты
Обмен холестерина начинается с создания этого соединения с помощью ГМГ-КоА-редуктаза. На первом этапе ключевой фермент ацетил-CoA-ацетилтрасфераза при слиянии двух молекул влияет на производство коэнзима А. В этом процессе превращения также участвует гидроксиметил, который позволяет из ацетила и ацетоацетила получить 3-гидрокси-3-метилглутарил-CoA. После от этого соединения отходит кофермент А, чье молекулярная формула выглядит как HS-CoA. Это приводит к синтезу мевалоната.
Вернуться к оглавлению
Производство изопентенилпирофосфата
На этой стадии синтез протекает в 4 реакции. Сначала мевалонат вместе с мевалоткиназом путем фосфорилирования становится 5-фосфомевалонатом. Затем на второй операции в обмене веществ участвует формула фосфомевалоната, которая превращается в 5-пирофосфомевалонат. После на него влияет гормон кеназ, что позволяет синтезировать 3-фосфо-5-пирофосфомевалонатом. На последнем этапе происходит декарбоксирование и дефосфорилирование, в результате чего синтезируются изопентинилпирофосфат.
Вернуться к оглавлению
Выработка сквалена
Одним из этапов синтеза является формирование и выработка сквалена – углеводорода.
Это коротки этап в формировании спирта. Регуляторным ферментов является гидроксиметилглутарил. Скваленовый путь начинается с того, что на выработанный фермент путем изомеризации влияет диметилаллилпирофосфат. После синтез липидов обеспечивает появление электрной свези между ферментами, что приводит к конденсированию и производству геранилпирофосфата. Но при этом от связи отходит часть пирофосфата, которая появилась при биосинтезе холестерина на втором этапе.
Вернуться к оглавлению
Производство ланостерина
На этом этапе образование эфиров в печени С5 изопентенилпирофосфата соединяется с 10 геранилпирофосфата. Затем происходит конденсация и образуется фарнезилпирофосфат. От него отходит часть, которая называется пирофосфата. На последней стадии этого этапа две молекулы фарнезилпирофосфатных соеднияются и конденсируются, что создает скавален, через распад пирофосфата в клетки.
Вернуться к оглавлению
Синтез липида
Это ключевой и завершающий момент, в котором процесс включает 5 реакций. Метаболизм холестерина начинается с окисления с участием С14 ланостерина. В результате это активирует производство14-десметилланостерина. Из соединения выпадают две С4 и органелла становится зимостеролом. Следующая операция приводит к образованию δ-7,24- холестадиенола. Затем меняются двойные связи и образуется демостерол. На последнем этапе восстанавливается взаимодействие и появляется сам холестерин.
Вернуться к оглавлению
От чего зависит?
По подсчетам ученых, в день производится от 0,5 до 0,8 грамм холестерола.
Биохимические процессы холестерола зависят от микрофлоры кишечника, так как этот орган влияет на всасывание жиров.
Цикл создания эндогенного соединения и обмен эфиров осуществляется при помощи приблизительно 30 реакций. Основные клетки, которые участвуют в этом действии — гепатоциты печени, в которых содержится ретикулин. Эта молекула является группой жиров и углеводов. Холестерин должен контролироваться, так как избыток или недостаток приводит к серьезным заболеваниям. Биохимия и синтез холестерола зависит от микрофлоры организма, в том числе кишечника. Этот орган влияет на всасывание жиров, образования эфиров и трансформации стиролов. Большую роль играет уровень фосфолипидов, которые транспортируют жиры. Важно поддерживать их количество, так как это контролирует содержание холестерола в крови.
Вернуться к оглавлению
Нарушения обмена холестерина
Избыток холестерина
Из-за недостатка физической активности, некачественного питания и переедания появляются проблемы с накоплением пищевого холестерина. Такое нарушение появляется у людей, имеющим вредные привычки. Из-за этого на сосудах начинают скапливаться холестериновые бляшки, которые мешают циркуляции крови. В результате развиваются заболевания сердца.
Нарушение холестеринового обмена происходит из-за таких болезней:
- желчные нарушения;
- патологии печени и почек;
- эндокринные заболевания.
Вернуться к оглавлению
Недостаток метаболитов
Регуляция синтеза холестерина происходит благодаря питанию и спорту. Высокая активность (занятие спортом, танцами) сильно влияет на биосинтез холестерола. Если при этом человек не употребляет алкоголь и не курит, то у него активно снижается количество природного спирта в тканях организма. Врачи рекомендуют для уменьшения уровня молекул соблюдать правильную диету, в которой превалирует углеводная пища. Синтез подавляется также при помощи лекарств. Но люди, у которых нарушен процесс синтеза, страдают от проблем с давлением и рискуют получить сердечный приступ.
Источник
холестериды, всасывание холестерина
Переваривание
холестеридов и всасывание холестерина.
Понятие об экзогенном и эндогенном
холестерине.
Холестерин
в организме человека бывает 2 видов:
1) холестерин,
поступающий с пищей через ЖКТ и называемый
экзогенный
2) холестерин,
синтезируемый из Ац – КоА — эндогенный.
С пищей
ежедневно поступает ≈ 0,2 – 0,5 г,
синтезируется ≈ 1 г (почти все клетки
за исключением эритроцитов синтезируют
холестерин, 80% холестерина синтезируется
в печени.)
Взаимоотношения
экзо и эндогенного холестерина в
определенной степени конкурентные –
холестерин пищи ингибирует его синтез
в печени.
В составе
пищи холестерин находится в основном
в виде эфиров. Гидролиз эфиров холестерола
происходит под действием холестеролэстеразы.
Продукты гидролиза всасываются в составе
смешанных мицелл.

Всасывание
холестерина происходит в основном в
тощей кишке (пищевой холестерин
всасывается почти полностью – если в
пище его не очень много)
Всасывание
холестерина осуществляется только
после эмульгирования эфиров холестерина.
Эмульгаторами являются желчные кислоты,
моно- и диглицериды и лизолецитины.
Холестериды гидролизуются холестеринэстеразой
поджелудочной железы.
Пищевой и
эндогенный холестерин находится в
просвете кишечника в неэстерифицированной
форме в составе сложных мицелл (желчные,
жирные кислоты, лизолецитин), причем
поступают в состав слизистой кишечника
не вся мицелла целиком, а ее отдельные
фракции.
Поглощение
холестерина из мицелл – пассивный
процесс, идущий по градиенту концентрации.
Поступивший в клетки слизистой холестерин
этерифицируется холестеринэстеразой
или АХАТ (у человека это в основном
олеиновая кислота). Из клеток слизистой
кишечника холестерин поступает в лимфу
в составе ХМ, из них он переходит в ЛНП
и ЛВП. В лимфе и крови 60-80% всего холестерина
находится в этерифицированном виде.
Процесс
всасывания холестерина из кишечника
зависит от состава пищи: жиры и углеводы
способствуют его всасыванию, растительные
стероиды (структурные аналоги) блокируют
этот процесс. Большое значение принадлежит
желчным кислотам (все функции активируют
– улучшают эмульгирование, всасывание).
Отсюда значение лекарственных веществ,
блокирующих всасывание желчных кислот.
Основные
этапы синтеза холестерина. Химизм
реакции образования мевалоновой кислоты.
Ключевой фермент синтеза холестерина.
Представьте схематически скваленовый
путь синтеза холестерина
Ключевой
фермент биосинтеза холестерина —
ГМГ-редуктаза
Локализация:печень,кишечник,кожа
Реакции
синтеза холестерола происходят в
цитозоле клеток. Это один из самых
длинных метаболических путей в организме
человека.
Источник-ацетил-КоА
1 этап-Образование
мевалоната
Две молекулы
ацетил-КоА конденсируются ферментом
тиолазой с образованием ацетоацетил-КоА.
Фермент
гидроксиметилглутарил-КоА-синтаза
присоединяет третий ацетильный остаток
с образованием ГМГ-КоА
(3-гидрокси-3-метилглутарил-КоА).
Следующая
реакция, катализируемая ГМГ-КоА-редуктазой,
является регуляторной в метаболическом
пути синтеза холестерола. В этой реакции
происходит восстановление ГМГ-КоА до
мевалоната с использованием 2 молекул
NADPH. Фермент ГМГ-КоА-редуктаза —
гликопротеин, пронизывающий мембрану
ЭР, активный центр которого выступает
в цитозоль.
2 этап —
Образование
сквалена
На втором
этапе синтеза мевалонат превращается
в пятиуглеродную изопреноидную структуру,
содержащую пирофосфат — изопентенилпирофосфат.
Продукт конденсации 2 изопреновых единиц
— геранилпирофосфат. Присоединение ещё
1 изопреновой единицы приводит к
образованию фарнезилпирофосфата —
соединения, состоящего из 15 углеродных
атомов. Две молекулы фарнезилпирофосфата
конденсируются с образованием сквалена
— углеводорода линейной структуры,
состоящего из 30 углеродных атомов.
3 этап —
Образование холестерола
На третьем
этапе синтеза холестерола сквален через
стадию образования эпоксида ферментом
циклазой превращается в молекулу
ланостерола, содержащую 4 конденсированных
цикла и 30 атомов углерода. Далее происходит
20 последовательных реакций, превращающих
ланостерол в холестерол. На последних
этапах синтеза от ланостерола отделяется
3 атома углерода, поэтому холестерол
содержит 27 углеродных атомов.

Биологическая роль холестерина. Пути
использования холестерина в различных
тканях. Биосинтез желчных кислот.
Часть
холестеринового фонда в организме
постоянно окисляется, преобразуясь в
различного рода стероидные соединения.
Основной путь окисления холестерина —
образование желчных кислот. На эти цели
уходит от 60 до 80% ежедневно образующегося
в организме холестерина. Второй путь —
образование стероидных гормонов (половые
гормоны, гормоны коры надпочечников и
др.). На эти цели уходит всего 2-4%
холестерина, образующегося в организме.
Третий путь — образование в коже витамина
ДЗ под действием ультрафиолетовых
лучей.
Еще одним
производным холестерина является
холестанол. Его роль в организме пока
еще не выяснена. Известно лишь, что он
активно накапливается в надпочечниках
и составляет 16% от всех находящихся там
стероидов. С мочой у человека выделяется
около 1 мг холестерина в сутки, а со
слущивающимся эпителием кожи теряется
до 100 мг/сут.
Желчные
кислоты являются основным компонентом
билиарной секреции, они образуются
только в печени. Синтезируются в печени
из холестерина.
В
организме синтезируется за сутки
200-600 мг желчных кислот. Первая реакция
синтеза-образование
7-альфа-гидроксихолестерола-является
регуляторной.Фермент-7-альфа-гидроксилаза,ингибируется
конечным продуктом-желчными
кислотами.7-альфа-гидроксилаза представляет
собой одну из форм цитохрома п450 и
использует атом кислорода как один из
субстратов. Один атом кислорода из О2
включается в гидроксильную группу в 7
положении, а другой восстанавливается
до воды. Последующие реакции синтеза
приводят к формированию 2 видов желчных
кислот:холевой и хондезоксихолевой(первичные
желчные кислоты)

Особенности
обмена холестерина в организме человека.
Роль липопротеинлипазы, печеночной
липазы, липопротеинов, ЛХАТ, апопротеинов
в транспорте холестерина в крови: альфа-
и бета-холестерин, коэффициент
атерогенности, АХАТ, накопление
холестерина в тканях. Пути распада и
выведения холестерина
В организме
человека содержится 140-190 г холестерина
и около 2 г образуется ежедневно из
жиров,углеводов, белков. Чрезмерное
поступление холестерина с пищей приводит
к отложению его в сосудах и может
способствовать развитию атеросклероза,
а также нарушению функции печени и
развитию желчно-каменной болезни.
Ненасыщенные жирные кислоты ( линолевая,
линоленовая) затрудняют всасывание
холестерина в кишечнике, тем самым
способствуя уменьшению его содержания
в организме. Насыщенные жирные кислоты
(пальмитиновая, стеариновая) являются
источником образования холестерина.
Липопротеинлипаза
(ЛПЛ) — фермент, относящийся к классу
липаз. ЛПЛ расщепляет триглицериды
самых крупных по размеру и богатых
липидами липопротеинов плазмы крови —
хиломикронов и липопротеинов очень
низкой плотности (ЛПОНП или ЛОНП)). ЛПЛ
регулирует уровень липидов в крови, что
определяет её важное значение в
атеросклерозе.
Печёночная
липаза — один из ферментов липидного
метаболизма. Эта липаза по ферментативному
действию похожа на панкреатическую
липазу. Однако в отличие от панкреатической
липазы ПЛ синтезируется в печени и
секретируется в кровь. Печёночная липаза
после секреции связывается со стенкой
сосуда (почти исключительно в печени)
и расщепляет липиды липопротеинов.
Печёночная
липаза работает в кровотоке в тандеме
с липопротеинлипазой. Липопротеинлипаза
расщепляет липопротеины, богатые
триглицеридами (липопротеины очень
низкой плотности и хиломикроны), до их
остатков. Остатки липопротеинов являются
в свою очередь субстратом для печёночной
липазы. Таким образом, в результате
действия печёночной липазы образуются
атерогенные липопротеины низкой
плотности, которые поглощаются печенью.
(ЛВП) — Транспорт
холестерина от периферийных тканей к
печени
(ЛНП) —
Транспорт холестерина, триацилглицеридов
и фосфолипидов от печени к периферийным
тканям
ЛПП (ЛСП) —
Транспорт холестерина, триацилглицеридов
и фосфолипидов от печени к периферийным
тканям
(ЛОНП)-Транспорт
холестерина, триацилглицеридов и
фосфолипидов от печени к периферийным
тканям
Хиломикроны -Транспорт
холестерина и жирных кислот, поступающих
с пищей, из кишечника в периферические
ткани и печень
Лецитинхолестеринацилтрансфераза
(ЛХАТ)- является ферментом метаболизма
липопротеинов. ЛХАТ связан с поверхностью
липопротеинов высокой плотности, которые
содержат аполипопротеин A1 — активатор
этого фермента. Холестерин, превращённый
в эфиры холестерина, благодаря высокой
гидрофобности перемещается с поверхности
липопротеина в ядро, освобождая место
на поверхности частицы для захвата
нового свободного холестерина. Таким
образом, эта реакция является исключительно
важной для процесса очищения периферических
тканей от холестерина (обратный транспорт
холестерина). Частица ЛПВП в результате
увеличивается в диаметре или в случае
насцентных ЛПВП превращается из
дисковидной в сферическую.
Апопротеины
формируют структуру липоппротеинов,взаимодействуют
с рецепторами на поверхности клеток и
таким образом определяют какими тканями
будет захватываться данный тип
липопротеидов, служат ферментами или
активаторами ферментов, действующих
на липопротеины.
АХАТ
катализирует эстерификацию холестерола
. Свободный холестерол выходит в
цитоплазму , где ингибирует ГМГ-CoA-редуктазу
и de novo синтез холестерола и активирует
АХАТ . У человека, однако, из-за низкой
активности АХАТ в печени холестерол
поступает в плазму в составе ЛПОНП
преимущественно в свободном виде.
Нарушение
обмена холестерола и холестеридов
проявляется прежде всего накоплением
их в тканях (кумулятивные холестерозы),
особенно в стенке артерий и в коже.
Основной причиной накопления холестерола
в тканях является недостаточность
механизма его обратного транспорта.
Ключевым фактором системы обратного
транспорта холестерола (с периферии в
печень, откуда его излишки удаляются
из организма с желчью) являются
липопротеины высокой плотности, точнее
входящий в их состав белок апопротеин
А. Частицы липопротеинов высокой
плотности собирают холестерол не только
в интерстициальном секторе, но и внутри
клеток. У человека (а также высших обезьян
и свиней) существует видовая (характерная
для всех представителей вида)
недостаточность апопротеина А и,
соответственно, липопротеинов высокой
плотности. Животные с высоким содержанием
этих липопротеинов не страдают
холестериновым диатезом, даже при
постоянном употреблении богатой
холестеролом пищи. Некоторые люди также
отличаются довольно высокой концентрацией
апопротеина А («синдром долголетия»).
Из организма
человека ежедневно выводится около 1 г
холестерола. Приблизительно половина
этого количества экскретируется с
фекалиями после превращения в желчные
кислоты . Оставшаяся часть выводится в
виде нейтральных стероидов. Большая
часть холестерола, поступившего в желчь,
реабсорбируется; считается, что по
крайней мере часть холестерола,
являющегося предшественником фекальных
стеролов , поступает из слизистой
оболочки кишечника . Основным фекальным
стеролом является копростанол , который
образуется из холестерола в нижнем
отделе кишечник а под действием
присутствующей в нем микрофлоры .
Значительная доля солей желчных кислот
, поступающих с желчью, всасывается в
кишечнике и через воротную вену
возвращается в печень , где снова
поступает в желчь. Этот путь транспорта
солей желчных кислот получил название
кишечно-печеночной циркуляции . Оставшаяся
часть солей желчных кислот, а также их
производные выводятся с фекалиями. Под
действием кишечных бактерий первичные
желчные кислоты превращаются во
вторичные.
Соседние файлы в предмете Биохимия
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник