Кто открыл гемоглобин крови
Содержание статьи
обин — Доказательная медицина для всех
Гемоглобин (Hb) — сложный белок, обеспечивающий транспорт кислорода из легких к тканям. Гемоглобин состоит из белковых цепей и гема — порфиринового кольца, которое содержит железо.
Физиологически, основной функцией гемоглобина является перенос кислорода из легких к органам и тканям, но не меньшей важностью является перенос гемоглобином оксида азота (NO) и регуляция тонуса сосудов (вазомоторного тонуса).
Низкий уровень гемоглобина является одним из проявлений анемии, повышенный уровень гемоглобина также является признаком ряда заболеваний и патологических состояний.
Гемоглобин. Цифры и факты
- Одна молекула гемоглобина переносит четыре молекулы кислорода
- Во всем гемоглобине в организме содержит 2,5 грамма железа у мужчин и 1,9 грамма у женщин
- Паразит, вызывающий малярию, малярийный плазмодий, питается гемоглобином. Подробнее о малярии
ЭТО ИНТЕРЕСНО: физиологический процесс распада гемоглобина в организме называется гемоглобинолизом
Виды гемоглобинов
В организме здорового взрослого человека присутствует несколько типов гемоглобина:
- Гемоглобин А (HbA)
- Гемоглобин A2 (HbA2)
- Фетальный гемоглобин (HbF)
- Гликированный гемоглобин (HbA1C)
Гликированный гемоглобин имеет важнейшее значение в диагностике и лечении сахарного диабета
Нормы гемоглобина
Казалось бы, все знают, что норма гемоглобина для женщин составляет 120-140 г/л (грамм на литр), а для мужчин 140-160 г/л. Но как и с нормальными показателями уровня сывороточного железа, с нормами гемоглобина не все так просто.
ЭТО ИНТЕРЕСНО: Методы определения концентрации гемоглобин в крови называются гемоглобинометрией
Сначала интересные факты о том, откуда взялись вышеуказанные нормы. Эти нормы разработаны ВОЗ, но разработаны они не для оценки нормального уровня гемоглобина как такового, а для оценки питания. Т.е. проще говоря, эти уровни гемоглобина соответствующие указанному диапазону, с точки зрения экспертов ВОЗ, говорят о том, что человек, в общем то, неплохо питается, не более того.
Ассоциация гематологов США предлагает рассматривать нижнюю границу нормы гемоглобина, на следующем уровне:
Популяция* | Нижняя граница нормы гемоглобина |
Мужчины в возрасте от 20 до 59 лет | 137 г/л |
Мужчины в возрасте старше 60 лет | 132 г/л |
Женщины 20 лет и старше | 122 г/л |
* Нормы гемоглобин для представителей европеоидной расы
Как следует из приведенной таблицы, на уровень гемоглобина влияют пол и возраст, другие факторы, влияющие на уровень гемоглобина:
- Проживание на большой высоте
- Занятия спортом
- Курение
- Раса
- Сопутствующие заболевания
У курящих, живущих на большой высоте, спортсменов — уровень гемоглобина будет выше, т.е. то, что для других норма, для других будет уже анемией. Как и наоборот, то, что для людей живущих примерно на уровне моря будет повышенным уровнем гемоглобина, для курящих, спортсменов и живущих на большой высоте будет нормой.
Норма гемоглобина у беременных женщин*
Первый триместр | Второй триместр | Третий триместр | |
Гемоглобин (г/л) | 116-139 | 97-148 | 9.5-150 |
Гематокрит (в процентах) | 31.0-41.0 | 30.0-39.0 | 28.0-40.0 |
*Данные показатели получены в результате клинических исследований, но не являются нормативными. Подробнее о некоторых лабораторных нормах у беременных женщин.
Итак, после того, как мы рассказали о сложностях в оценке того, какой уровень является нормальным для гемоглобина, а какой нет, мы расскажем на какие нормативные показатели обычно ориентируются врачи.
Показатель | Мужчины | Женщины |
Гемоглобин г/л | 157 ± 17 | 138 ± 15 |
Гематокрит % | 46.0 ± 4.0 | 40.0 ± 4.0 |
Эритроцитов в мкл | 5.2 ± 0.7 | 4.6 ± 0.5 |
Ретикулоциты % | 1.6 ± 0.5 | 1.4 ± 0.5 |
Средний объем эритроцита, fL | 88.0 ± 8.0 | |
Среднее содержание гемоглобина в эритроците | 30.4 ± 2.8 | |
Средняя концентрация гемоглобина в эритроците | 34.4 ± 1.1 | |
Ширина распределения эритроцитов | 13.1 ± 1.4 | |
Напомним, что нормальные показатели гемоглобина у взрослых отличаются от показателей у детей.
Гемоглобин у детей
Возраст | Гемоглобин, г/л | Гематокрит, % | Средний эритроцитарный объем, мкм3 |
Новорожденные | 165 ± 30 | 51 ± 9 | 108 ± 10 |
1 мес | 140 ± 40 | 43 ± 12 | 104 ± 19 |
6 мес | 115 ± 20 | 35 ± 6 | 91 ± 17 |
1 год | 120 ± 15 | 36 ± 3 | 78 ± 8 |
2—6 лет | 125 ± 10 | 37 ± 3 | 81 ± 6 |
6—12 лет | 135 ± 20 | 40 ± 5 | 86 ± 9 |
12—18 лет | 140 ± 20 | 42 ± 6 | 89 ± 11 |
Подготовка к анализу на гемоглобин
Подготовка к анализу на гемоглобин обычно не требуется. Перед анализом необходимо пить достаточное количество жидкости, чтобы не допустить обезвоживания. Анализ на гемоглобин может быть сдан отдельно, но чаще всего, исследование гемоглобина проводится в рамках проведения общего анализа крови. В некоторых случаях общий анализ крови может потребовать подготовки в виде 12 часового голодания.
Симптомы пониженного гемоглобина
Пониженный гемоглобин приводит к недостаточному обеспечению органов и тканей кислородом. ОБычно симптомы низкого гемоглобина включают:
- слабость
- одышку
- головокружение
- учащенное сердцебиение
- шум в ушах
- головную боль
- похолодание конечностей
- побледнение или желтизну кожи
- боль в груди
Подробно симптомы связанные с пониженным гемоглобином обсуждаются в статье об анемиях.
Источник
Тайна крови: эволюцию гемоглобина воссоздали в пробирке
Биологи выяснили происхождение гемоглобина и синтезировали белки, которые были его предками. Оказалось, что поразительная эффективность этого вещества, сделавшая позвоночных господами планеты, возникла благодаря всего двум ключевым мутациям.
Достижение описано в научной статье, опубликованной в журнале Nature.
Великолепная четвёрка
Все современные наземные позвоночные и почти все морские, за исключением жалкой сотни видов, относятся к группе челюстных. Но выделяются они не только челюстями, но и строением гемоглобина. Он невероятно эффективно справляется с переносом кислорода. Несомненно, это стало одним из главных эволюционных козырей челюстных, позволивших им оккупировать верхние уровни всех пищевых цепей на суше и в море.
Гемоглобин челюстных – белок с характером. Его молекула – это комплекс из четырёх субъединиц, каждая из которых, в общем-то, и сама представляет собой полноценную молекулу белка. Таким образом, наш гемоглобин – это белок, состоящий из других белков.
Таких белков два, и обозначаются они греческими буквами α и β. Каждая молекула гемоглобина в нашей крови состоит из двух молекул α-белка (α-субъединиц) и двух молекул β-белка (β-субъединиц).
При этом все четыре субъединицы связывают или высвобождают кислород одновременно. Так что молекула гемоглобина транспортирует живительный газ по принципу «четыре грузовика по цене одного». Ничего удивительного, что организмы с такой щедрой кислородной логистикой добились господствующего положения на земном шаре.
Удивительная эффективность гемоглобина позволяет нам иметь быстрый обмен веществ.
Потомки индивидуалистов
При этом и α-, и β-белок входят в обширное семейство глобинов. Удивительно, но их ближайшие известные «сородичи» по этому семейству совсем не склонны объединятся в комплексы и брать на себя скромную роль субъединиц. Они предпочитают гордое одиночество. В таком случае когда и как они обрели способность к объединению (за что им огромное спасибо от имени всех челюстных)? До сих пор ответа не было.
Между прочим, эта загадка касается не только гемоглобина. Большинство белков представляют собой комплексы из нескольких субъединиц и только благодаря этому могут выполнять свои биологические функции. И совершенно неизвестно, как и когда молекулы-субъединицы научились подобной кооперации.
И, пожалуй, именно с гемоглобина удобнее всего было начать распутывать эту головоломку.
«Структура и функция гемоглобина изучены лучше, чем, возможно, любой другой молекулы. Но ничего не было известно о том, как они возникли в ходе эволюции, – рассказывает первый автор статьи Арвид Пиллаи (Arvind Pillai) из Чикагского университета. – Это отличная модель [для изучения эволюции белков], потому что компоненты гемоглобина являются частью обширного семейства белков, и их самые близкие «родственники» не образуют комплексов, а функционируют в одиночку».
Отзвуки прошлого
Проанализировав структуру разных глобинов, исследователи восстановили их эволюционное древо. Они исходили из того, что все глобины происходят от общего белка-предка. При этом чем больше похожи друг на друга последовательности аминокислот в двух белках, тем позже разошлись их эволюционные пути. А зная, насколько часто происходят мутации, можно установить и когда произошло это ветвление.
Биологи не просто вычислили структуру белков-предков. Они синтезировали эти вещества и изучили их в эксперименте. Здесь авторам опять-таки помог тот факт, что человечество десятилетиями пристально изучало гемоглобин и накопило целый арсенал методов для этого занятия. Он подошёл и для исследования «воскрешенных» молекул.
«Есть отличные лабораторные инструменты для анализа их свойств», – отмечает Пиллаи.
Эволюционное дерево гемоглобина челюстных согласно новому исследованию.
Захватывающая история из жизни белков
У авторов получилась следующая история из жизни белков. Это быль, но, чтобы облегчить участь читателя, расскажем её в тоне сказки.
Жил-был на свете белок, последний общий предок гемоглобина и миоглобина (исследователи назвали его AncMH). И никаких комплексов ни с кем он образовывать не умел и не хотел.
Но однажды он мутировал, и получился из него белок Ancα/β – последний общий предок α- и β-белков гемоглобина. Две молекулы Ancα/β уже умели образовывать пару друг с другом.
Долго ли, коротко ли, но Ancα/β тоже мутировал. И возникло два новых белка: Ancα и Ancβ. И оказалось, что молекула Ancα так нравится молекуле Ancβ, а та настолько отвечает ей взаимностью, что две эти молекулы могут образовать пару.
До гемоглобина остался лишь один шаг. Ancα и Ancβ снова претерпели каждый свою мутацию. После чего из Ancα получился уже α-белок собственной персоной, а из Ancβ – β-белок. А пара, состоящая из одной молекулы α-белка и одной молекулы β-белка, обрела способность объединиться с другой такой же парой.
Так и получилась молекула-четвёрка, поныне снабжающая каждого из нас кислородом (в этом месте все челюстные дружно поаплодировали руками, лапами и плавниками).
Три революции в одной
Удивительно, но две мутации, научившие пары Ancα+Ancβ объединяться в четвёрки, привели к ещё одному животворному изменению.
Молекулы всех предшественников нашего современного гемоглобина, включая Ancα и Ancβ, слишком уж страстно сливались в объятиях с молекулой кислорода и неохотно расставались с ней. Поэтому они плохо выполняли свою функцию по снабжению этим веществом клеток.
Мутации, собравшие четыре белка в один, не заменили ни одной аминокислоты в участке молекулы, который соединяется с кислородом. Но когда четыре молекулы объединились, аминокислотная нить буквально натянулась как верёвка. Участок, связывающий кислород, изменил свою форму. В результате белок умерил свой пыл в отношении O2.
Более того, при этом возникла и та самая склонность всех субъединиц присоединять или отдавать кислород одновременно (очень удачно для каждого из нас).
Происходит этот процесс так. Когда одна субъединица соединяется с молекулой кислорода, натяжение аминокислотной нити ослабевает. «Кислородосвязывающий» участок соседней субъединицы возвращает себе исходную форму. Примерно ту самую, которую он имел в жадной до O2 молекуле Ancα или Ancβ. Поэтому эта субъединица тоже сразу же хватает пролетающий мимо кислород. Потом приходит черёд третьей субъединицы, а затем и четвёртой.
Когда приходит время расставаться с добычей, всё происходит в обратном порядке. Достаточно одной субъединице отдать свою молекулу газа, как аминокислотная нить снова натягивается. Форма связывающего кислород участка ближайшей субъединицы меняется, и она уже не настолько крепко держит молекулу O2. Потом та же участь постигает третью и четвёртую субъединицу.
Так и получается наш замечательный гемоглобин. Его молекула состоит из четырёх субъединиц, присоединяющих или отдающих кислород одновременно. И чувство родства с кислородом у него ровно такое, какое выгодно организму. Он охотно забирает этот газ из лёгких или жабр, но при этом послушно отдаёт его нуждающимся клеткам. И всё благодаря двум простым мутациям, научившим пары молекулы объединяться в четвёрку.
Кстати, произошли они более 400 миллионов лет назад, ещё до того, как разделились эволюционные линии человека и акулы.
Эффективный гемоглобин стал эволюционным козырем челюстных позвоночных.
Всемогущая случайность
«Мы были поражены, когда увидели, что такой простой механизм может породить такие сложные свойства, – признаётся глава исследовательской группы Джозеф Торнтон (Joseph Thornton) из Чикагского университета. – Это говорит о том, что во время эволюции скачки в сложности могут происходить внезапно и даже случайно, создавая новые молекулярные объекты, которые в конечном итоге становятся необходимыми для нашей биологии».
Традиционный взгляд на эволюцию, восходящий ещё к Дарвину, заключается в том, что новое не возникает сразу. Мутации, ведущие к кардинальным изменениям в организме, конечно, случаются, но они могут быть только вредными. Получится урод, монстр, который не сможет выжить и размножиться.
Живой организм настолько сложен, говорят сторонники этой позиции, что любое крупное изменение нарушит какой-нибудь важный процесс. Изменить живое и при этом оставить его живым можно только в мелочах. Конечно, мелкие изменения постепенно накапливаются, рано или поздно меняя организм до неузнаваемости. Но нужны целые эпохи, чтобы потомок перестал походить на предка.
Между тем восстановленная авторами история гемоглобина убедительно демонстрирует, что иногда ключевые изменения происходят скачком, за одну-две мутации. Кстати, это далеко не единственный пример того, как изменения в небольшом числе генов обеспечивают эволюционные прорывы. Так что, хотя эволюция действительно чаще всего работает через накопление небольших изменений, иногда случаются стремительные революции.
Другой урок этого исследования, пожалуй, в том, насколько нынешний облик всей биосферы определяется произошедшими когда-то случайностями.
«Представьте себе, если эти две мутации никогда не произошли <…>, – фантазирует Торнтон. – Гемоглобин в том виде, в котором мы его знаем, не эволюционировал. А вместе с ним многие последующие инновации, которые требуют эффективного транспорта кислорода, такие как быстрый обмен веществ и способность достигать гораздо больших размеров и двигаться гораздо быстрее, чем наши древние морские предки».
Впрочем, как ни удивительно, ключевые эволюционные прорывы нередко происходят независимо в разных эволюционных линиях. Например, животные и растения стали многоклеточными независимо друг от друга. Так что было бы слишком опрометчиво утверждать, что без этих двух мутаций позвоночные так и остались бы мелкими и медлительными морскими созданиями с неэффективным дыханием. Возможно, случились бы какие-то другие изменения в белках, решившие проблему доставки кислорода. Но, вероятно, жизнь в этом случае была бы совсем не похожа на ту, частью которой мы являемся.
К слову, ранее «Вести.Наука» (nauka.vesti.ru) рассказывали об эволюционной истории другого ключевого изобретения живых организмов – фотосинтеза.
Источник
емоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.
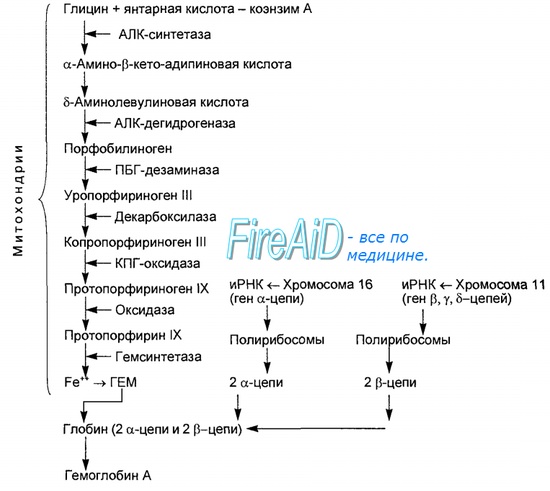
Оглавление темы «Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.»: Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.Гемоглобин — это гемопротеин, с молекулярной массой около 60 тыс., окрашивающий эритроцит в красный цвет после связывания молекулы O2 с ионом железа (Fe++). У мужчин в 1 л крови содержится 157 (140—175) г гемоглобина, у женщин — 138 (123—153) г. Молекула гемоглобина состоит из четырех субъединиц гема, связанных с белковой частью молекулы — глобином, сформированной из полипептидных цепей.
Синтез гема протекает в митохондриях эритробластов. Синтез цепей глобина осуществляется на полирибосомах и контролируется генами 11-й и 16-й хромосом. Схема синтеза гемоглобина у человека представлена на рис. 7.2. Гемоглобин, содержащий две а- и две В-цепи, называется А-тип (от adult — взрослый). 1 г гемоглобина А-типа связывает 1,34 мл O2. В первые три месяца жизни плода человека в крови содержатся эмбриональные гемоглобины типа Gower I (4 эпсилон цепи) и Gower II (2а и 25 цепи). Затем формируется гемоглобин F (от faetus — плод). Его глобин представлен двумя цепями а и двумя В. Гемоглобин F обладает на 20—30 % большим сродством к O2, чем гемоглобин А, что способствует лучшему снабжению плода кислородом. При рождении ребенка до 50—80 % гемоглобина у него представлены гемоглобином F и 15—40 % — типом А, а к 3 годам уровень гемоглобина F снижается до 2 %. Соединение гемоглобина с молекулой 02 называется оксигемоглобином. Сродство гемоглобина к кислороду и диссоциация оксигемоглобина (отсоединения молекул кислорода от оксигемоглобина) зависят от напряжения кислорода (Р02), углекислого газа (РС02) в крови, рН крови, ее температуры и концентрации 2,3-ДФГ в эритроцитах. Так, сродство повышают увеличение Р02 или снижение РС02 в крови, нарушение образования 2,3-ДФГ в эритроцитах. Напротив, повышение концентрации 2,3-ДФГ, снижение Р02 крови, сдвиг рН в кислую сторону, повышение РС02 и температуры крови — уменьшают сродство гемоглобина к кислороду, тем самым облегчая ее отдачу тканям. 2,3-ДФГ связывается с р-цепями гемоглобина, облегчая отсоединение 02 от молекулы гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах. Оксигемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. В состоянии физиологического покоя у человека гемоглобин в артериальной крови на 97 % насыщен кислородом, в венозной — на 70 %. Чем выраженней потребление кислорода тканями, тем ниже насыщение венозной крови кислородом. Например, при интенсивной физической работе потребление кислорода мышечной тканью увеличивается в несколько десятков раз и насыщение кислородом оттекающей от мышц венозной крови снижается до 15 %. Содержание гемоглобина в отдельном эритроците составляет 27,5—33,2 пикограмма. Снижение этой величины свидетельствует о гипохромном (т. е. пониженном), увеличение — о гиперхромном (т. е. повышенном) содержании гемоглобина в эритроцитах. Этот показатель имеет диагностическое значение. Например, гиперхромия эритроцитов характерна для В|2-дефицитной анемии, гипохромия — для железодефицитной анемии. — Также рекомендуем «Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты.» |
Источник