Механизм связывания кислорода гемоглобином
Содержание статьи
Эффективность связывания кислорода с гемоглобином регулируется
Кооперативное взаимодействие
Взаимовлияние протомеров олигомерного белка друг на друга называется кооперативное взаимодействие.
В легких такое взаимодействие субъединиц гемоглобина повышает его сродство к кислороду и ускоряет присоединение кислорода в 300 раз. В тканях идет обратный процесс, сродство снижается и ускорение отдачи кислорода также 300-кратное.
Схема кооперативного взаимодействия субъединиц гемоглобина
Объясняется такой феномен тем, что в легких при присоединении первой молекулы кислорода к железу (за счет 6-й координационной связи) атом железа втягивается в плоскость гема, кислород остается вне плоскости. Это вызывает перемещение участка белковой цепи и изменение конформации первого протомера. Такой измененный протомер влияет на другие субъединицы и облегчает связывание кислорода со второй субъединицей. Это меняет конформацию второй субъединицы, облегчая присоединение последующих молекул кислорода и изменение других протомеров.
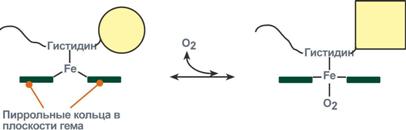
Изменение формы субъединиц гемоглобина
при присоединении и отщеплении кислорода
Дезоксиформа гемоглобина обозначается как Т-форма, напряженная (англ. tense), она обладает существенно более низким сродством к кислороду. Оксигенированная форма, или R-форма (англ. relaxed), обладает высоким сродством к кислороду.
Изменение рН среды
Влияние рН на сродство гемоглобина к кислороду носит название эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
При повышении концентрации протонов (закисление среды) в тканях возрастает освобождение кислорода из оксигемоглобина. В легких после удаления угольной кислоты (в виде СО2) из крови и одновременном увеличении концентрации кислорода высвобождаются ионы Н+ из гемоглобина.
Реакция взаимодействия кислорода с гемоглобином упрощенно имеет вид:
Изменение сродства гемоглобина к кислороду в тканях и в легких при изменении концентрации ионов H+ и О2 обусловлено конформационными перестройками глобиновой части молекулы. В тканях молекула О2 отрывается от железа и ионы водорода присоединяются к остаткам гистидина (глобиновой части), образуя восстановленный гемоглобин (H-Hb) с низким сродством к кислороду. В легких поступающий в больших количествах кислород «вытесняет» ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
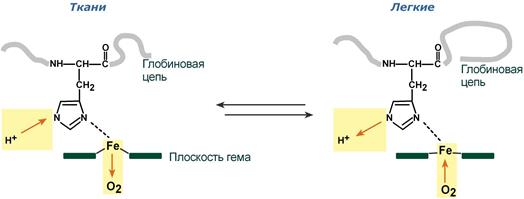
Механизм эффекта Бора
Роль 2,3-дифосфоглицерата
2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
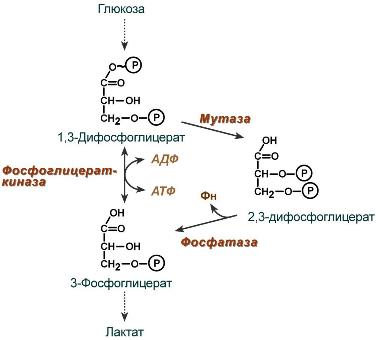
Реакции шунта Раппопорта
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
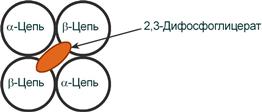
Расположение 2,3-дифосфоглицерата в гемоглобине
Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду, что имеет особенное значение при подъеме на высоту и при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
Источник
Гемоглобин: роль в газообмене и процессе дыхания
Одним из самых сложных процессов, что происходят в организме человека, несомненно, является дыхание. И сложность эта не только в танце легких, благодаря которому человек получает кислород, но и в процессах, с помощью которых этот кислород проникает дальше, в ткани, где превращается в углекислый газ, что отправляется в обратное путешествие. О данных процессах и пойдет речь далее.
Итак, приступим. Человек делает вдох, иии… Далеко не весь кислород поступает в легкие, а затем и в кровь. Часть вдыхаемого воздуха остается в так называемом мертвом пространстве. Мертвое пространство, в свою очередь, делится на анатомическое (дыхательные пути), в котором остается около 30 % вдыхаемого воздуха, и функциональное (вентилируемые, но по каким-то причинам не перфузируемые альвеолы).
Ухудшение альвеолярного газообмена может происходить при неглубоком и частом дыхании (причиной может стать перелом ребер, паралич дыхательной мускулатуры различного генеза и др.), а также при увеличении мертвого пространства, вызванном разнообразными причинами (нарушение перфузии альвеол в результате воспалительных заболеваний легких, удаление доли или целого легкого и др.), при снижении скорости кровотока по альвеолярным капиллярам (ТЭЛА, инфаркт легкого), при наличии диффузионного барьера (отек легких) и в результате ослабления альвеолярной вентиляции при обтурации просвета бронха. Газообмен между легкими и кровью происходит путем диффузии в соответствии с законом Фика. В легочных капиллярах она происходит за счет разности парциальных давлений в альвеолах и эритроцитах.
В альвеолах парциальное давление кислорода значительно превышает таковое для углекислого газа и составляет примерно 13,3 кПа (100 мм рт. ст.) и 5,3 кПа (40 мм рт. ст.) соответственно. Альвеолы омываются приносимой легочными артериями венозной кровью, в которой соотношение парциальных давлений этих двух газов обратно пропорционально и составляет приблизительно 5,3 кПа (40 мм рт. ст.) для кислорода и 6,1 кПа (46 мм рт. ст.) для углекислого газа. В среднем разница парциальных давлений составляет около 8 кПа (60 мм рт. ст.) для кислорода и около 0,8 кПа для углекислого газа.
Как уже было сказано выше, кислород путем диффузии проникает в кровь легочных капилляров. Диффузионное расстояние для кислорода при этом составляет 1–2 мкм, то есть именно на такое расстояние он проникает внутрь капилляра. Обмен крови в легочном капилляре происходит примерно за 0,75 секунды, но этого времени хватает на то, чтобы парциальные давления в альвеолах и в крови пришли в равновесие.
Кровь, в которой показатели парциального давления для кислорода и углекислого газа примерно равны таковым в альвеолах, называется артериализированной. Однако за счет наличия в легких артериовенозных шунтов и притока венозной крови из бронхиальных вен такой она остается недолго. В результате парциальное давление кислорода в аорте составляет примерно 12,0 кПа (как уже было сказано выше, парциальное давление в артериализированной крови равно таковому в альвеолах и составляет 13,3 кПа), а давление углекислого газа меняется незначительно и не приводит к затруднению его диффузии из крови в альвеолы.
Но кислород непосредственно в ткани попадает лишь в крайне незначительных количествах: для свободного перемещения по организму ему необходим транспортер. Эту функцию выполняет содержащийся в эритроцитах белок — гемоглобин. Гемоглобин существует в оксигенированной и неоксигенированной формах. В дезокси-гемоглобине железо находится на уровне порфиринового кольца и стабилизируется электростатическими силами, что обеспечивает поддержание всей структуры. Появившись, кислород начинает «тянуть» за железо, которое переносится на проксимальный гистидин на другом конце полипептидной цепи и меняет структуру всего протеина.
В результате гемоглобин переходит в оксигенированную форму, альфа- и бета-цепи при этом поворачиваются относительно друг друга на 15 градусов, облегчая присоединение остальных молекул кислорода. В итоге каждый из четырех содержащихся в нем атомов двухвалентного железа обратимо связывается с молекулой кислорода, что превращает молекулу гемоглобина в оксигемоглобин. По сравнению с миоглобином гемоглобин имеет низкое сродство к кислороду, однако оно не статично. Так, миоглобин может связывать кислород только одним участком, поэтому кривая его связывания — гипербола. Кривая связывания гемоглобина с кислородом имеет S-образную форму, демонстрируя, что при его связывании с первой молекулой кислорода гемоглобин имеет очень низкое сродство к кислороду, но при связывании последующих молекул кислорода сродство остальных его субъединиц к нему значительно увеличивается и в конечном счете повышается примерно в 500 раз.
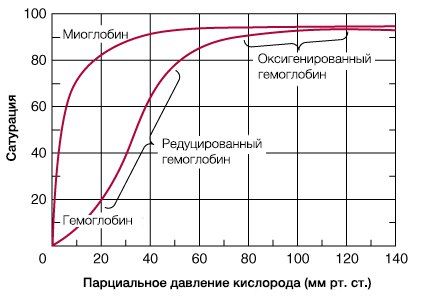
При этом альфа-цепи связывают кислород легче, чем бета-цепи. Этот процесс назван кооперативным взаимодействием. По мере снижения парциального давления кислорода в крови происходит его высвобождение из гемоглобина и поступление в ткани. Например, парциальное давление кислорода в работающих мышцах составляет всего 26 мм рт. ст, и при прохождении эритроцитов через капилляры, кровоснабжающие мышцы, происходит высвобождение и поступление в мышечные клетки примерно ⅓ всего переносимого гемоглобином кислорода. При повышении температуры тела также возрастает потребность в кислороде, что, в свою очередь, стимулирует высвобождение и поступление его в ткани. При снижении температуры, напротив, развивается гипоксия тканей, способствующая компенсаторному увеличению сродства гемоглобина к кислороду.
Гемоглобин также осуществляет перенос от тканей к легким продуктов тканевого дыхания — углекислого газа и ионов водорода. В ходе окислительных процессов в клетке выделяется углекислый газ, в результате гидратации которого образуются ионы водорода, что, в свою очередь, приводит к снижению рН. Давно известно, что снижение рН и повышение концентрации углекислого газа в крови оказывает сильное влияние на способность гемоглобина связывать кислород.
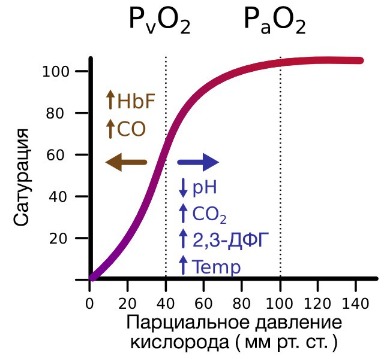
В периферических сосудах показатели рН низкие, и по мере связывания гемоглобина с ионами водорода и углекислым газом происходит снижение его сродства к кислороду. Это влияние величины рН и концентрации углекислого газа на способность гемоглобина связывать кислород называют эффектом Бора.
Обратная ситуация имеет место в альвеолярных капиллярах, где присоединение кислорода к гемоглобину превращает тот в более сильную кислоту.
При этом сродство гемоглобина к углекислому газу снижается, а повышение кислотности гемоглобина приводит к высвобождению излишка ионов водорода и образованию в крови из бикарбоната угольной кислоты, которая затем распадается на воду и углекислый газ. В обоих случаях углекислый газ из крови поступает в альвеолы, а затем в атмосферу. Данный процесс назван эффектом Холдейна. Стоит отметить, что важную роль в образовании углекислого газа в эритроцитах играет ион хлора, поступающий в плазму крови в обмен на бикарбонат при участии белка-переносчика АЕ1. Данный процесс в англоязычной литературе получил название «Chloride shift» или «перенос Хамбургера».
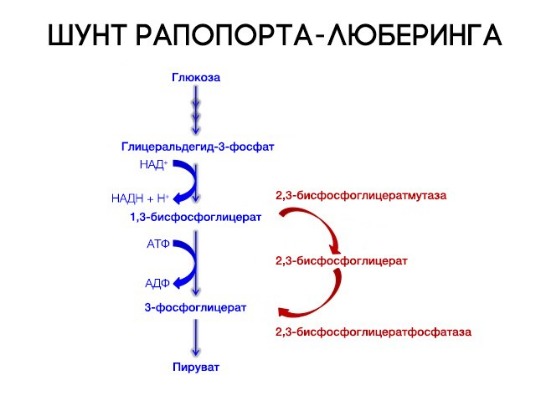
На сродство гемоглобина к кислороду оказывает влияние и присутствующее в эритроцитах вещество, получившее название 2,3-бисфосфоглицерат (БФГ). Его образование — своего рода побочная реакция анаэробного гликолиза, происходящего в эритроцитах в ходе ферментативного превращения глюкозы в пируват под действием фермента бифосфоглицератмутазы. БФГ способен самостоятельно связываться с неоксигенированной формой гемоглобина, образуя солевой мостик между двумя его бета-субъединицами и снижая сродство к кислороду.
При этом гемоглобин способен связать только одну молекулу БФГ, а при присоединении кислорода БФГ вытесняется из полости. В обычных условиях в эритроцитах крови содержится достаточно большое количество БФГ, которое может увеличиваться в условиях гипоксии (например, у дайверов при погружении на глубину), а также при восхождении на большую высоту. В первые часы подъема концентрация БФГ в эритроцитах будет возрастать, а сродство кислороду снижаться. Но на большой высоте парциальное давление будет значительно ниже такового на уровне моря, а значит, оно снизится и в тканях. При этом БФГ будет облегчать передачу кислорода от гемоглобина к тканям.
Некоторые вещества способны прочно связываться с гемоглобином или же вовсе менять его структуру. Одним из них является угарный газ, чье сродство к гемоглобину в 200 раз превышает таковое для кислорода. Отравления угарным газом часто происходят в помещениях с печным отоплением, при пожарах и авариях на производстве. Со временем кислород вытесняет угарный газ из гемоглобина, и в легких случаях пациенты помещаются под наблюдение и получают ингаляции с увлажненным кислородом. Необходимой мерой при тяжелых отравлениях угарным газом является переливание эритроцитарной массы.
К веществам, способным изменять структуру гемоглобина, относятся метгемоглобинобразователи — соединения, способные окислять двухвалентное железо в геме до трехвалентного. К ним относятся нитриты, нитраты, некоторые местные анестетики, аминофенолы, хлораты, примахин и некоторые сульфаниламиды. Состояние, характеризующееся появлением в крови окисленного гемоглобина, называют метгемоглобинемией. При высокой метгемоглобинемии капля крови, помещенная на фильтровальную бумагу, имеет характерный коричневый цвет, а при пропускании кислорода через пробирку с такой кровью ее цвет не меняется. Метгемоглобинемия выше 70 % от общего содержания гемоглобина часто приводит к гибели пациента еще до момента постановки диагноза.
Источники:
- Harrison’s hematology and oncology Longo, Dan L (Dan Louis), Third edition. New York : McGraw-Hill Education Medical, 2017.
- Наглядная физиология, С. Зильбернагль, А. Деспопулос, 2013.
- Ленинджер А. Основы биохимии: В 3-х т. Т. 1. /Д. Нельсон, М. Кокс ; Пер. с англ.-М.: БИНОМ: Лаборатория знаний, 2011.- 694 с.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
Эффект Вериго — Бора
Мы немного порассуждали о лёгких и тканях,
и о том, какие же между ними отношения,
когда они пытаются посылать туда-обратно маленькие молекулы
и в это же время отправлять тканям кислород.
Ткань же пытается найти самый эффективный способ отправить обратно углекислый газ.
Это и есть 2 основных процесса, которые происходят между лёгкими и тканями.
Мы уже говорили о том, что есть 2 основных пути получения кислорода.
Первый — самый лёгкий — растворённый кислород.
Растворённый в крови кислород.
Но это не основной путь.
Основной — связывание кислорода с гемоглобином
и образование HbO2, молекулы под названием оксигемоглобин.
Именно так большинство кислорода попадает в ткани.
С другой стороны от тканей в лёгкие переносится
растворённый углекислый газ,
небольшое количество которого переносится прямо в плазме.
Однако, это не основной путь обратной поставки углекислого газа.
Самый эффективный путь доставки углекислого газа в лёгкие —
протонированная форма гемоглобина.
Когда я говорил о протонированной форме гемоглобина,
я упоминал, что плазма содержит бикарбонат.
Суть процесса заключается в том, что
возвращаясь в лёгкие, протон и бикарбонат
снова встречаются и образуют СО2, а также воду,
это происходит благодаря содержащемуся в красных клетках крови ферменту под названием
карбоангидраза.
Это и есть основной путь доставки углекислого газа в лёгкие.
Конечно, есть ещё и 3-ий, заключающийся в том, что гемоглобин
связывается непосредственно с углекислым газом в процессе и
образуется маленький протон,
который участвует здесь.
Он также может связываться с гемоглобином.
Среди такого взаимодействия я бы хотел привлечь ваше внимание к тому,
что гемоглобин может связываться с кислородом
также как и с протонами.
Самое интересное здесь то, что происходит что-то вроде соревнования.
Происходит, так сказать, небольшая игра.
С одной стороны, у вас есть гемоглобин, связывающийся с кислородом
(я нарисую его дважды),
и это, в свою очередь, приводит к взаимодействию с протоном,
который, в свою очередь, пытается выхватить гемоглобин.
Происходит небольшое соревнование за гемоглобин,
в котором кислород не участвует,
а углекислый газ вступает в реакцию, о которой мы уже говорили.
Небольшое количество гемоглобина связывается с углекислым газом, в результате чего образуется протон,
но и в этом процессе кислород не участвует.
Поэтому происходящая реакция напрямую зависит от того,
каких молекул в данный момент больше:
кислорода, протона или углекислого газа.
В зависимости от того, каких молекул больше
в ткани или клетке, происходит соответствующая реакция.
Учитывая это, я мог бы вернуться назад и сказать, что
я думаю, углекислый газ и протон влияют на кислород.
Я мог бы сказать, что и углекислый газ, и протон
действительно влияют
на избирательное стремление гемоглобина к соединению.
Повторю, избирательное стремление гемоглобина к соединению
или на его желание связываться с кислородом.
Это один из выводов, который вы бы могли сделать, наблюдая за таким соревнованием.
Представив это, я думаю, можно сказать,
что кислород (в зависимости от того,
какой точки зрения вы придерживаетесь) влияет на
избирательное стремление гемоглобина к соединению с
углекислым газом или протоном.
Итак, избирательное стремление гемоглобина к соединению с углекислым газом или протоном.
Я хочу подчеркнуть, что независимо от точки зрения,
которой вы придерживаетесь, оба эти утверждения верны.
Мы можем решить, что, возможно, просто повторяем одно и то же дважды.
Но на самом деле это два разных факта, каждый из которых называется по-своему.
Первый случай, когда мы говорим о реакции углекислого газа и протонов,
называется «эффект Бора».
Вы можете встретить это название или описание.
Это эффект Бора.
И второй случай, если мы посмотрим на наш процесс с точки зрения кислорода,
то реакция будет называться «эффект Холдейна».
Что же такое эффект Бора и эффект Холдейна,
кроме того, что это соревнование за гемоглобин?
Давайте я подниму экран,
и посмотрим, смогу ли я их изобразить.
Я считаю, что небольшой рисунок или схема действительно помогают объяснить такие вещи.
Я буду использовать небольшой график. Посмотрим, смогу ли я на нём изобразить эффект Бора.
Это парциальное давление кислорода, то есть то, сколько кислорода растворяется в плазме.
И это содержание кислорода, которое показывает, сколько всего кислорода в крови,
что, конечно, учитывает в основном количество кислорода, связавшегося с гемоглобином.
Что же будет, если я медленно увеличу парциальное давление кислорода?
Вначале лишь несколько молекул кислорода свяжется с гемоглобином,
но как только это произойдёт, возникнет кооперативный эффект,
и потихоньку наклон кривой начнёт увеличиваться и станет более резким.
Такая реакция обусловлена кооперативным эффектом,
так как кислород вступает в реакцию там, где уже произошла реакция с его молекулами.
Затем кривая выравнивается.
Выравнивание происходит в результате насыщения гемоглобина.
Так как остаётся мало свободного места,
необходимо, чтобы в плазме растворилось много кислорода,
который сможет тщательно поискать и найти оставшиеся свободные места на гемоглобине.
Предположим, мы выбрали 2 зоны.
Одна зона богата растворённым в крови кислородом,
а во 2-ой наблюдается недостаток растворённого в крови кислорода.
Это произвольный выбор,
поэтому не следует беспокоиться о точном количестве.
Если вы подумаете, где в организме наблюдается максимальное скопление кислорода, то
естественно, это будут лёгкие, где в крови растворено много кислорода.
И низкое количество кислорода наблюдается в бедренной мышце, например, где много СО2,
но в крови растворено мало кислорода.
И так, это две части тела, и теперь,
глядя на эту кривую, вы можете узнать,
сколько кислорода доставляется в бедро.
Это легко. Я мог бы сказать,
сколько кислорода в лёгких или в кровеносном сосуде, отходящем от лёгких…
Итак.
Вот это — количество кислорода в кровеносных сосудах, идущих от лёгких.
Вот это — количество кислорода в кровеносном сосуде, идущем от бедра.
Разница между этими двумя значениями —
это и есть количество поставляемого кислорода.
Поэтому, если вы хотите вычислить, сколько кислорода поставляется в ткань,
вы должны просто вычесть эти два значения,
это и будет количество поставляемого кислорода.
Глядя на эти два значения, вы можете заинтересоваться тем,
что произойдёт, если вы захотите повысить поставку кислорода.
Предположим, что по какой-то причине необходимо сделать этот процесс более эффективным,
в этом случае всё, что можно сделать, — это
увеличить гипоксию в бедре (на графике вы движетесь влево)
или, другими словами, уменьшить количество имеющегося кислорода.
Итак, при повышении гипоксии в бедре,
(точка на графике станет ниже),
увеличится количество поставляемого кислорода.
Однако это не идеальный вариант, так как нехватка кислорода в бедре
вызывает боль.
Есть ли другой способ увеличения поставки кислорода
без гипоксии или уменьшения количества кислорода в ткани?
Существует ли такой способ поставки кислорода?
Здесь и вступает в игру эффект Бора.
Давайте вспомним: эффект Бора заключается во влиянии СО2 и протона на связь гемоглобина с кислородом.
Дело состоит в том (я буду помечать это зелёным цветом), что
в этой ситуации у нас много углекислого газа и протонов,
это и есть эффект Бора, когда кислороду труднее связаться с гемоглобином.
Если я изображу другую кривую,
изначально она будет менее выраженной, так как ещё меньшее количество кислорода связано с гемоглобином.
Но как только концентрация кислорода достаточно увеличится,
кривая начнёт подниматься и подниматься, и, в конечном счёте, кислород будет связываться с гемоглобином,
то есть, нет такого, что он бы совсем не связывался с ним в присутствии углекислого газа и протонов,
просто это займёт больше времени.
При этом кривая выглядит так, как будто её сместили.
Такие условия с высоким содержанием СО2 и протонов,
которые, по сути, не подходят для лёгких.
Лёгкие, думают: «Кого это волнует? У нас нет таких условий».
Но для бедра, это подходит.
Так как в бедре много СО2 и протонов.
Вспомните, большое количество протонов означает низкий рН.
Это можно рассмотреть с разных точек зрения.
То есть, с бедром — другой случай.
Ему соответствует не зелёная, а синяя кривая.
Поэтому мы сможем изобразить точку на том же самом уровне О2 но ниже.
Каково же содержание О2 в крови, направляющейся из бедра?
Если всё сделать правильно, на кривой это будет отображаться здесь.
Это фактическое количество, при этом доставленное количество О2 становится более впечатляющим.
Посмотрите, из-за эффекта Бора поставка О2 увеличилась.
Если вы захотите узнать, насколько точно она увеличивается,
я покажу — это будет количество отсюда до сюда,
другими словами, — вертикальное расстояние между зелёной и голубой линиями
это и есть дополнительное количество поставленного из-за эффекта Бора кислорода.
Вот почему эффект Бора так важен,
Ведь, по сути, он помогает нам поставлять кислород в ткани.
Итак, теперь давайте по тому же принципу
рассмотрим эффект Холдейна.
Фактически мы должны всё поменять местами, поэтому поменяются и оси, и единицы измерения.
Здесь у нас будет количество углекислого газа,
а здесь — содержание углекислого газа в крови.
Давайте поразмышляем об этом эффекте.
Начнём с медленного, но уверенного увеличения количества углекислого газа
и посмотрим, как увеличивается его концентрация.
С увеличением количества углекислого газа
его концентрация в крови увеличивается прямо пропорционально.
Кривая не имеет S-образной формы, как кривая кислорода,
потому что при связывании с гемоглобином нет кооперативного эффекта.
Содержание углекислого газа просто увеличивается прямо пропорционально его количеству.
Это достаточно легко.
Теперь давайте возьмём два случая, как мы делали ранее.
Здесь будет высокое содержание СО2 в крови,
а здесь низкое содержание СО2 в крови.
В какой же ткани будет низкое содержание СО2 в крови?
Низкое содержание СО2 находится, конечно, в лёгких,
так как здесь мало углекислого газа.
А высокое содержание СО2 возможно в бедре, так как бёдра — это маленькие фабрики по производству СО2.
Поэтому в бёдрах высокое содержание СО2, а в лёгких — низкое.
Если необходимо узнать количество поставленного СО2, то нужно повторить то, что мы делали ранее.
Итак, высокое количество СО2 в бёдрах — это высокое количество СО2 в крови.
А это количество СО2 в крови, направляющейся от бёдер к лёгким.
Поэтому количество поставленного из бёдер в лёгкие СО2 —
это разница этих двух значений. Вот так мы можем рассчитать количество фактически поставленного СО2.
Так же как и поставка О2, наблюдается поставка большого количества СО2.
Теперь давайте перечитаем эффект Холдейна, и посмотрим, что произойдёт,
если мы изобразим ещё одну линию при наличии большого количества кислорода?
Высокая концентрация кислорода меняет
избирательное стремление гемоглобина к связыванию с углекислым газом и протонами.
Поэтому прямо пропорционально количеству гемоглобина снизится количество связанных протонов и углекислого газа.
А это означает снижение содержания СО2
при любом его количестве, растворённом в крови.
Поэтому эта линия всё ещё прямая, но вы можете заметить, что она действительно снижается по наклонной.
И где же это возможно, в каких случаях такое происходит?
Давайте попытаемся определить, где же максимальное количество кислорода?
Это, конечно, не бёдра, так как
в бёдрах мало кислорода.
Но это подходит лёгким.
Даже очень.
Теперь вы скажете: «Давайте посмотрим, что же происходит?
Сколько же поставляется СО2 при высокой концентрации О2?»
Возможно, вы уже заметили, что оно будет больше?
Так как при высокой концентрации О2, количество поставляемого СО2 непрерывно увеличивается.
Это и будет новое количество поставленного СО2.
То есть, вы даже можете узнать точное количество поставленного СО2.
Необходимо узнать разницу этих двух значений,
в чём, по сути, и заключается эффект Холдейна.
Вот так наглядно можно рассмотреть этот эффект.
И так, эффект Бора и эффект Холдейна — две важные стратегии, которых придерживается наш организм
для увеличения количества поставляемого О2 и выводимого СО2
между лёгкими и тканями.
Источник