Метгемоглобин образуется при взаимодействии гемоглобина с
Содержание статьи
Метгемоглобин
Молекула гемоглобина: 4 субъединицы глобина окрашены в разные цвета
Гемоглоби́н (от др.-греч. αἷμα — кровь и лат. globus — шар) — сложный железосодержащий белок эритроцитов животных и человека, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани.
Главная функция гемоглобина состоит в транспорте дыхательных газов. В капиллярах лёгких в условиях избытка кислорода последний соединяется с гемоглобином. Током крови эритроциты, содержащие молекулы гемоглобина со связанным кислородом, доставляются к органам и тканям, где кислорода мало, здесь необходимый для протекания окислительных процессов кислород освобождается из связи с гемоглобином. Кроме того, гемоглобин способен связывать в тканях небольшое количество диоксида углерода (CO2) и освобождать его в лёгких. Монооксид углерода (CO) связывается с гемоглобином крови прочнее, чем кислород, образуя карбоксигемоглобин (HbCO). Некоторые процессы приводят к окислению иона железа в геме до степени окисления +3. В результате образуется форма гемоглобина, известная как метгемоглобин (HbOH) (metHb, от мета… и гемоглобин, иначе гемиглобин или ферригемоглобин, см. Метгемоглобинемия). В обоих случаях блокируются процессы транспортировки кислорода. Впрочем, монооксид углерода может быть частично вытеснен из гема при повышении парциального давления кислорода в легких.
Нормальным содержанием гемоглобина в крови человека считается: у мужчин 130-170 г/л, у женщин 120-150 г/л; у детей — 120-140 г/л.
Строение
Гемоглобин является сложным белком класса хромопротеинов, то есть в качестве простетической группы здесь выступает особая пигментная группа, содержащая химический элемент железо — гем. Гемоглобин является тетрамером, то есть состоит из четырёх субъединиц. У взрослого человека они представлены полипептидными цепями α1, α2, β1 и β2. Субъединицы соединены друг с другом по принципу изологического тетраэдра. Основной вклад во взаимодействие субъединиц вносят гидрофобные взаимодействия. И α, и β-цепи относятся к α-спиральному структурному классу, так как содержат исключительно α-спирали. Каждая цепь содержит восемь спиральных участков, обозначаемых буквами A-H (От N-конца к C-концу).
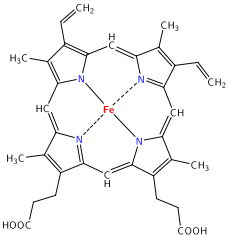
Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа(II). Эта простетическая группа нековалентно связана с гидрофобной впадиной молекул гемоглобина и миоглобина. Железо(II) характеризуется октаэдрической координацией, то есть связывается с шестью лигандами. Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. Две других координационных позиции лежат на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93 положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается заключённой между атомом железа и азотом ещё одного остатка гистидина, располагающегося в 64 положении цепи (участок E). Всего в гемоглобине четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может связываться четыре молекулы. Гемоглобин в легких при высоком парциальном давлении кислорода соединяется с ним, образуя оксигемоглобин. При этом кислород соединяется с гемом, присоединяясь к железу гема на 6-ю координационную связь.На эту же связь присоединяется и моноксид углерода, вступая с кислородом в конкурентную борьбу за связь с гемоглобином,образуя карбоксигемоглобин.Связь моноксида углерода с гемоглобином более прочная, чем с кислородом.Поэтому часть гемоглобина,образующая комплекс с моноксидом углерода не участвует в транспорте кислорода.В норме у человека образуется 1,2% карбоксигемоглобина. Повышение его уровня характерно для гемолитических процессов, в связи с этим уровень карбоксигемоглобина является показателем гемолиза.
Физиология
Гемоглобин является одним из основных белков, которыми питаются плазмодии малярии, и в эндемичных по малярии районах земного шара весьма распространены наследственные аномалии строения гемоглобина, затрудняющие малярийным плазмодиям питание этим белком и проникновение в эритроцит. В частности, к таким имеющим эволюционно-приспособительное значение аномалиям относится серповидно-клеточная анемия. Однако, к несчастью, эти аномалии, как и аномалии строения гемоглобина не имеющие явно приспособительного значения, сопровождаются нарушением кислород-транспортирующей функции гемоглобина, снижением устойчивости эритроцитов к разрушению, анемией и другими негативными последствиями. Аномалии строения гемоглобина называются гемоглобинопатиями.
Гемоглобин высоко токсичен при попадании значительного его количества из эритроцитов в плазму крови (что происходит при массивном внутрисосудистом гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях). Токсичность гемоглобина, находящегося вне эритроцитов, в свободном состоянии в плазме крови, проявляется тканевой гипоксией — ухудшением кислородного снабжения тканей, перегрузкой организма продуктами разрушения гемоглобина — железом, билирубином, порфиринами с развитием желтухи или острой порфирии, закупоркой почечных канальцев крупными молекулами гемоглобина с развитием некроза почечных канальцев и острой почечной недостаточности.
Ввиду высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. В частности, одним из компонентов системы обезвреживания гемоглобина является особый плазменный белок гаптоглобин, специфически связывающий свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина (или гемоглобина) затем захватывается селезенкой и макрофагами тканевой ретикуло-эндотелиальной системы и обезвреживается.
Другой частью гемоглобинообезвреживающей системы является белок гемопексин, специфически связывающий свободный гем и гем в составе гемоглобина. Комплекс гема (или гемоглобина) и гемопексина затем захватывается печенью, гем отщепляется и используется для синтеза билирубина и других желчных пигментов, или выпускается в рециркуляцию в комплексе с трансферрином для повторного использования костным мозгом в процессе эритропоэза.
Смотри также
- Гемоглобин С (мутантная форма)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (эмбриональный гемоглобин)
Литература
- Mathews, CK; KE van Holde & KG Ahern (2000), Biochemistry (3rd ed.), Addison Wesley Longman, ISBN 0-8053-3066-6.
- Levitt, M & C Chothia (June 17, 1976), «Structural patterns in globular proteins», Nature. doi 10.1038/261552a0.
Ссылки
- Гемоглобин в мясе и изменения цвета под воздействием окисления
- Интерактивные модели гемоглобина
Wiki Foundation. 2010.
Источник
1.2. Метгемоглобинобразователи.
Железо, входящее в структуру гемоглобина — двухвалентно, независимо от того, связан пигмент крови с кислородом (HbO) или нет (Hb). Более того, только находясь в двухвалентном состоянии, Fe+2 обладает необходимым для осуществления транспортных функций сродством к кислороду.
В нормальных условиях спонтанно и под влиянием различных патогенных факторов, в том числе химической природы, двухвалентное железо гемоглобина окисляется, переходя в трёхвалентную форму. Образуется так называемый метгемоглобин (MetHb). Метгемоглобин не участвует в переносе кислорода от лёгких к тканям, поэтому значительное повышение его содержания в крови представляет опасность в связи с развитием гипоксии гемического типа.
Основной причиной массивного образования метгемоглобина в крови является действие на организм химических веществ, объединяемых в группу метгемоглобинобразователей. Все они являются органическими или неорганическими соединениями, содержащими азот. Наиболее токсичные метгемоглобинобразователи входят в одну из следующих групп:
Соли азатистой кислоты (нитрит натрия);
Алифатические нитриты (амилнитрит, изопропилнитрит, бутилнитрит и т.д.);
Ароматические амины (анилин, аминофенол);
Ароматические нитраты (динитробензол, хлорнитробензол);
Производные гидроксиламина (фенилгидраксиламин);
Производные гидразина (фенилгидразин).
Некоторые из указанных веществ могут представлять интерес для военной медицины либо как возможные диверсионные агенты (нитрит натрия), либо как промышленные агенты весьма опасные при авариях и катастрофах. Последнее обстоятельство связано с тем, что амино- и нитросоединения бензольного ряда — анилин, метиланилин, диметиланилин (ксилидин), нитроанилин, нитробензол, динитробензол, нитротолуол, динитротолуол, тринитротолуол, их хлор-производные продукты и изомеры, а также ряд других нитросоединений широко используются в текстильной, пищевой, фармацевтической промышленности, производстве синтетических красителей, пластических масс и взрывчатых веществ.
Попав в организм, эти вещества либо непосредсредственно активируют процессы, приводящие к окислению гемоглобина, либо первоначально метаболизируются в организме с образованием реактивных продуктов, которые обладают этим свойством. Тяжесть развивающейся при этом патологии определяется дозой и скоростью поступления токсиканта в организм, а затем в эритроциты, их окислительно-восстановительным потенциалом, скоростью элиминации. Если действующим веществом является не исходное вещество, а продукт его метаболизма, то глубина патологического процесса зависит также от интенсивности биоактивации ксенобиотика в организме.
В организме человека с большой скоростью вызывают метгемоглобинобразование соли азотистой кислоты (нитриты), алкиламинофенолы (диэтил-, диметиламинофенол). Медленно нарастает содержание MetHb при отравлении анилином, нитробензолом.
Проявления метгемоглобинемии.
Поскольку образующийся метгемоглобин не способен переносить кислород, у пораженных развивается гемическая форма гипоксии со всеми характерными клиническими признаками, выраженность которых будет зависеть от количества образовавшегося метгемоглобина. Если содержание метгемоглобина не превышает 15%, то клинические проявления гемической гипоксии, как правило, отсутствуют. При содержании метгемоглобина 15 — 20% у пострадавшего отмечается головная боль, возбуждение, возникает состояние, напоминающее алкогольное опьянение. Образование метгемоглобина порядка 20 -45% сопровождается беспокойством, тахикардией, одышкой при физической нагрузке, слабостью, утомляемостью, возникновением состояния оглушенности. При содержании 45 — 55% метгемоглобина возникает угнетение сознания, ступор; 55 — 70% — судороги, кома, брадикардия, аритмии. При содержании метгемоглобина более 70% развивается сердечная недостаточность и может наступить смерть. Кроме того, при действии больших доз этих веществ, гемоглобин может окисляться до сульфгемоглобина и вертгемоглобина, которые в дальнейшем не восстанавливаются и приводят к гемолизу эритроцитов, с присоединением гемолитической анемии, которая, в свою очередь, может привести к развитию острой почечной, а иногда и печёночной недостаточности.
Характерной особенностью клинической картины поражения является развитие выраженного цианоза, от фиолетового оттенка при легкой степени интоксикации до аспидно-серого или сине-черного цвета при средних и тяжелых поражениях. Наличие сульфгемоглобина резко усиливает цианоз, поскольку он в три раза темнее MetHb (артериальная кровь приобретает коричневатый оттенок). Цианоз развивается при содержании в крови метгемоглобина около 10%, а сульфгемоглобина уже около 3%. Поэтому даже при достаточно выраженном цианозе может не отмечаться сколько-нибудь значительных признаков гипоксии. При этом цианоз носит разлитой («центральный») характер, то есть практически сразу происходит относительно равномерное синюшное окрашивание всех участков кожных покровов и видимых слизистых, поскольку вся циркулирующая в организме кровь изменяет свой цвет.
Нитро- и аминосоединения ароматического ряда.
Нитро- и аминосоединения ароматического ряда по физико-химическим свойствам, путям поступления, механизму действия и картине острого отравления весьма сходны. Наиболее распространенными представителями этой группы СДЯВ являются нитробензол и анилин.
Эти вещества представляют собой жидкости с довольно высокой температурой кипения (нитробензол+210, анилин+184 град.), неприятным специфическим запахом и относительной плотностью паров по воздуху больше 1. Эти вещества способны вызывать поражение при любом пути поступления, но наиболее часто встречается ингаляционный и перкутанный варианты поражения. Острое отравление развивается при концентрации паров анилина >0,6 г/м3, нитробензола — ≥0,5 г/м3. При пероральном поступлении смертельная доза для анилина составляет порядка 1 грамма, для нитробензола данные отсутствуют. Есть материалы, согласно которым несколько капель вещества, принятых через рот, могут привести к смертельному отравлению. Очаги, образуемые этими токсическими соединениями, относятся к стойким замедленного действия. Эти вещества объединяет механизм токсческого действия — выраженное метгемоглобинобразование.
Механизм действия и патогенез интоксикации нитро- и аминосоединениями ароматического ряда.
Попав в организм человека, нитробензол и анилин проникают во все органы и ткани, накапливаясь преимущественно в печени и жировой ткани, где могут образовываться депо этих СДЯВ, за счет чего, в последующем, возможны рецидивы интоксикации. Биотрансформация осуществляется в основном в печени, а также в почках, слизистой ЖКТ. Конечными продуктами метаболизма являются о- и п-аминофенолы, которые вступают в реакции конъюгации с глюкуроновой, серной кислотами и глутатионом, а также в реакцию N-ацетилирования. Конъюгаты — высоко полярные, нетоксичные соединения, выводятся из организма с мочой. В процессе метаболизма образуются промежуточные продукты, представляющие собой свободные радикалы, которые могут активировать молекулярный кислород, который в свою очередь взаимодействуя с водой приводит к образованию перекиси водорода. Действие супероксидного радикала и перекиси водорода на железо гемоглобина приводит к его окислению (метгемоглобинобразование). Наряду с другими компонентами противорадикальной защиты в эритроцитах отравленных снижается уровень восстановленного глутатиона, который выполняет функцию стабилизатора эритроцитарных мембран. Истощение пула этого трипептида сопровождается развитием гемолиза. Кроме метгемглобинобразующих свойств метаболиты анилина и нитробензола обладают мутагенными, тератогенными и канцерогенными свойствами.
Из особенностей клинической картины следует также отметить возможность повторного развития метгемоглобинобразования с усилением симптомов интоксикации, что связано с выходом в кровь депонированного в жировой ткани яда. Повторное метгемоглобинобразование является прогностически неблагоприятным признаком, довольно часто провоцируется тепловыми процедурами (горячая ванна, душ) или приемом алкоголя и может развиться даже на 12-14 день после первичного отравления.
Выделяются вещества частично в неизмененном виде через легкие (запах горького миндаля в выдыхаемом воздухе у отравленных нитробензолом) и почки (болезненное мочеиспускание у отравленных анилином). Метаболиты выводятся в виде конъюгатов через почки.
Нитриты.
Нитриты — это производные азотистой кислоты: либо её соли (неорганические производные: азотистокислый натрий), либо простые эфиры спиртов, содержащие одну или несколько нитритных групп (органические производные: изопропилнитрит, бутирилнитрит). По механизму действия и картине острого отравления различные представители группы во многом сходны. Однако неорганические производные обладают более выраженной метгемоглобинобразующей активностью, а органические — более сильным действием на стенки кровеносных сосудов.
Азотистокислый натрий. Кристаллическое вещество хорошо растворимое в воде, солоноватое на вкус. Основной путь поступления — пероральный с зараженной пищей и водой. В организме часть вещества окисляется до нитратов (затем вновь восстанавливается до NO2-), часть восстанавливается до оксида азота, часть превращается в нитрозоамины, значительная часть выводится в неизменённом виде. Пероральное поступление около 3 граммов вещества вызывает тяжёлое отравление.
Изопропилнитрит. Желтоватая жидкость с резким запахом, температура кипения около 400, плохо растворяется в воде, хорошо — в спирте. Водный раствор быстро гидролизуется с выделением оксидов азота. Поражения могут возникнуть при ингаляционном либо пероральном (со спиртными напитками) поступлении. В организме разрушается с отщеплением оксида азота или нитритной группы. Расчётная смертельная доза при приёме через рот для человека составляет около 9 мг/кг.
Помимо способности вызывать быстрое, но умеренное образование в крови метгемоглобина, связанное с высвобождением нитрит-иона, для нитритов характерно возбуждающее действие на ЦНС и специфическое расслабляющее действие на гладкую мускулатуру кровеносных сосудов, за счёт образующегося оксида азота. При этом вены более чувствительны к веществам, чем артерии. При интоксикациях, в результате расслабления прежде всего больших вен, значительно увеличивается ёмкость сосудистого русла, что приводит к снижению системного артериального давления. Развивается головная боль, появляется чувство пульсации в висках, головокружение, тошнота, двигательные расстройства. Кожа лица краснеет. Нарушается зрение, слух. Острая реакция на умеренные дозы веществ быстро проходит. При высоких дозах и продолжительном воздействии давление резко падает, сознание утрачивается, постепенно появляется цианоз, как следствие метгемоглобинобразования. Таким образом, для отравления нитритами характерен смешанный тип развивающейся гипоксии: гемический (за счёт метгемоглобинобразования) и циркуляторный (за счёт расслабления сосудов).
Оказание помощи при поражении метгемоглобинобразователями.
При оказании помощи пораженным проводятся, прежде всего мероприятия, направленные на удаление всосавшегося яда и его метаболитов (форсированный диурез, гемодиализ и гемосорбция в первые 4-5 часов, в дальнейшем — перитонеальный диализ), а также на деметгемоглобинобразование. С этой целью внутривенно вводятся хромосмон до 30мл, или метиленовый синий — 1% раствор из расчёта 1 — 2 мг/кг, тиосульфат натрия 30% — 60-100мл, аскорбиновая кислота 5%- 60мл на глюкозе; внутримышечно витамин В12 — 600мкг. При очень тяжелых формах интоксикации в ранние сроки показана операция замещения крови. Для устранения гемической гипоксии проводится ГБО.
Кроме того, проводится симптоматическая терапия, мероприятия, направленные на защиту печени и профилактику инфекционных осложнений.
Соседние файлы в папке Лекции
- #
- #
- #
- #
- #
- #
- #
Источник