Молекулярная масса молекулы гемоглобина
Содержание статьи
емоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.
Оглавление темы «Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.»: Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.Гемоглобин — это гемопротеин, с молекулярной массой около 60 тыс., окрашивающий эритроцит в красный цвет после связывания молекулы O2 с ионом железа (Fe++). У мужчин в 1 л крови содержится 157 (140—175) г гемоглобина, у женщин — 138 (123—153) г. Молекула гемоглобина состоит из четырех субъединиц гема, связанных с белковой частью молекулы — глобином, сформированной из полипептидных цепей.
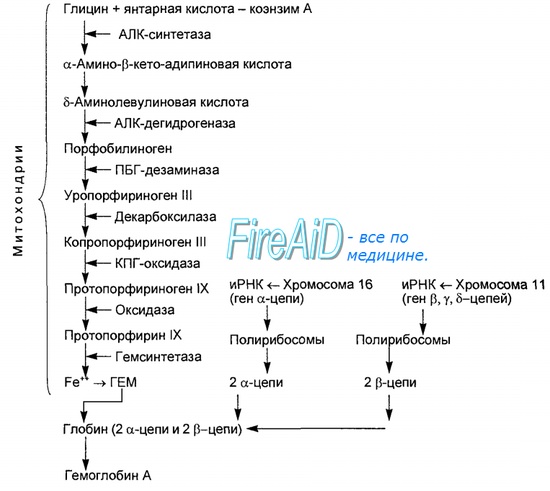
Синтез гема протекает в митохондриях эритробластов. Синтез цепей глобина осуществляется на полирибосомах и контролируется генами 11-й и 16-й хромосом. Схема синтеза гемоглобина у человека представлена на рис. 7.2. Гемоглобин, содержащий две а- и две В-цепи, называется А-тип (от adult — взрослый). 1 г гемоглобина А-типа связывает 1,34 мл O2. В первые три месяца жизни плода человека в крови содержатся эмбриональные гемоглобины типа Gower I (4 эпсилон цепи) и Gower II (2а и 25 цепи). Затем формируется гемоглобин F (от faetus — плод). Его глобин представлен двумя цепями а и двумя В. Гемоглобин F обладает на 20—30 % большим сродством к O2, чем гемоглобин А, что способствует лучшему снабжению плода кислородом. При рождении ребенка до 50—80 % гемоглобина у него представлены гемоглобином F и 15—40 % — типом А, а к 3 годам уровень гемоглобина F снижается до 2 %. Соединение гемоглобина с молекулой 02 называется оксигемоглобином. Сродство гемоглобина к кислороду и диссоциация оксигемоглобина (отсоединения молекул кислорода от оксигемоглобина) зависят от напряжения кислорода (Р02), углекислого газа (РС02) в крови, рН крови, ее температуры и концентрации 2,3-ДФГ в эритроцитах. Так, сродство повышают увеличение Р02 или снижение РС02 в крови, нарушение образования 2,3-ДФГ в эритроцитах. Напротив, повышение концентрации 2,3-ДФГ, снижение Р02 крови, сдвиг рН в кислую сторону, повышение РС02 и температуры крови — уменьшают сродство гемоглобина к кислороду, тем самым облегчая ее отдачу тканям. 2,3-ДФГ связывается с р-цепями гемоглобина, облегчая отсоединение 02 от молекулы гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах. Оксигемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. В состоянии физиологического покоя у человека гемоглобин в артериальной крови на 97 % насыщен кислородом, в венозной — на 70 %. Чем выраженней потребление кислорода тканями, тем ниже насыщение венозной крови кислородом. Например, при интенсивной физической работе потребление кислорода мышечной тканью увеличивается в несколько десятков раз и насыщение кислородом оттекающей от мышц венозной крови снижается до 15 %. Содержание гемоглобина в отдельном эритроците составляет 27,5—33,2 пикограмма. Снижение этой величины свидетельствует о гипохромном (т. е. пониженном), увеличение — о гиперхромном (т. е. повышенном) содержании гемоглобина в эритроцитах. Этот показатель имеет диагностическое значение. Например, гиперхромия эритроцитов характерна для В|2-дефицитной анемии, гипохромия — для железодефицитной анемии. — Также рекомендуем «Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты.» |
Источник
имический каталог >> ГЕМОГЛОБИН
ГЕМОГЛОБИН
Автор Химическая энциклопедия г.р. И.Л.Кнунянц
ГЕМОГЛОБИН (от греческого haima- кровь и лат. globus-шар), основные белок
дыхат. цикла, участвующий в переносе О2 от органов дыхания к
тканям, а в обратном направлении — СО2. Содержится в эритроцитах
крови почти всех позвоночных и гемолимфе большинства беспозвоночных животных.
Г. позвоночных (молекулярная масса 6,4*104-6,6*104) состоят
из четырех попарно идентичных субъединиц (их обозначают греческого буквами;
теми же буквами обозначают входящие в состав субъединиц полипептидные цепи,
а также гены, кодирующие эти цепи). Каждая субъединица имеет белковую глобиновую
часть, состоящую из 140-160 аминокислотных остатков, с которой нековалентно
связан гем-ферропрото-порфирин (см. формулу).

Функцию переноса О2 у некоторых видов беспозвоночных выполняют
крупные гемсодержащие белки-эритрокруорины (молекулярная масса 0,4*106-6,7*106),
состоящие из 30-400 субъединиц, и хлоркруорины (молекулярная масса 3,4*106),
состоящие из 190 субъединиц. Эти белки способны обратимо связывать одну
молекулу О2 на группу тема, т.е. на субъединицу. Переносчиком
О2 у др. видов беспозвоночных служат негемовые белки, состоящие
из 8-10 субъединиц,— медьсодержащие гемоцианины (молекулярная масса 0,05*107*107)
и железосодержащие гемэритрины (молекулярная масса 1*105). Каждая субъединица
таких белков содержит два атома металла (соответственно Сu + и Fe2+), способных связать одну молекулу О2.
ГЕМОГЛОБИН взрослого человека (НbА) имеет молекулярная масса 6,49*104 и принадлежит
к числу наиболее изученных белков. Его форма в растворе близка к эллипсоиду с
осями 6,4, 5,5 и 5,0 нм; изоэлектрич. точка 6,9. Тетрамер НЬА состоит из
двух и двухсубъединиц,
их полипептидные цепи содержат соответственно 141 и 146 аминокислотных остатков.
Известны первичная структура обеих цепей, а также пространств. структура
оксигенированной, дезоксигенированной, ряда лигандированных, а также окисленной
формы (содержит Fe3+) НbА. Пространств. структура
субъединиц (рис. 1) характеризуется наличием восьмиспиральных
участков, включающих около 80% аминокислотных остатков, и внутр. полости
-гемового кармана. Фиксирование тема в субъединице осуществляется в результате
гидрофобных взаимодействие пиррольных и винильных групп тема с алифатич. и ароматические
боковыми радикалами аминокислот, выстилающими полость кармана, а также
благодаря координационной связи (направлена перпендикулярно к плоскости
кольца тема) Fe2+ с аксиальным лигандом-имидазольной группой
гистидина (так называемой проксимальный гистидин). При оксигенации молекула О2
занимает шестое вакантное место в координационной сфере Fe2+.
Связывание происходит обратимо, без окисления железа, с образованием стабильного
оксигенированного комплекса НbО2. Одна молекула ГЕМОГЛОБИН способна
присоединить 4 молекулы О2-по одной на группу тема.

Рис. 1. Схема упаковки поли-пептидной цеписубъединицы
гемоглобина. Точками обозначены положенияС
атомов аминокислотных остатков; 1 -гем; 2-проксимальный остаток гистидина.
Субъединицы
и прочно
удерживаются в составе тетрамера ГЕМОГЛОБИН множественными ван-дер-ваальсовыми
взаимодействие и водородными связями; дезоксигенированная форма НbА стабилизирована
кроме того несколько ионными связями внутри и между субъединицами. Теграмер
Г.-кооперативная структура, в которой существует взаимодействие пространственно
разобщенных между собой групп (так называемой гем-гем взаимодействие). Это проявляется
в облегчении присоединения к тетрамеру последующих молекул О2
по мере протекания оксигенирования, что значительно увеличивает эффективность
переноса О2 при физиол. условиях по сравнению с мономерными
Г. и миоглобином (белок, депонирующий О2 в мышцах). Присоединение
О2 к молекуле ГЕМОГЛОБИН сопровождается значительной конформационными перестройками
пространств. структуры субъединиц и тетрамера в целом.
Сродство ГЕМОГЛОБИН к О2 является основным физических-химический показателем
функциональных свойств ГЕМОГЛОБИН; его принято характеризовать зависимостью степени
оксигенирования ГЕМОГЛОБИН от парциального давления кислорода
(кислородно-диссоционная кривая, или КДК, рис. 2), а также величиной,
при которой достигается оксигенирование 50% ГЕМОГЛОБИН (р50)- Нормальная
величина р50 НbА в крови при физиол. условиях [37 °С, парциальное
давление СО2
40 мм рт. ст., рН 7,4] составляет 26-28 мм рт. ст. Сигмоидный характер
КДК отражает кооперативный характер оксигенирования. При существующем у
человека различии артериальной и венозной крови (соответственно 90 ± 10 и 40 ±
2 мм рт. ст.) 1 л крови, насыщенной в легких кислородом (92-98% ГЕМОГЛОБИН находится
в форме НbО2), отдает в тканях ок. 45 мл О2, при
этом содержание НbО2 в венозной крови составляет 70-75%.

Рис. 2. Зависимость содержания оксигемоглобина от парциального давления
О2.
Из клеток тканей СО2 диффундирует через плазму крови в эритроциты,
где гидратируется в реакции, катализируемой ферментом карбоангидразой:
Гидрокарбонат-ионы в эритроцитах замещаются далее на ионы Cl-
из плазмы, сами переходят в плазму и переносятся ею к легким. Определенная
часть СО2 связывается в эритроцитах с N-концевымиаминогруппами
Г. с образованием остатка карбаминовой кислоты, уменьшая сродство ГЕМОГЛОБИН к О2.
Увеличение РСО2 температуры, ионной силы раствора и уменьшение рН снижают
сродство ГЕМОГЛОБИН к О2. Важнейший внутриэритроцитарный регулятор сродства
— анионы 2,3-дифосфоглицериновой кислоты. Увеличение их концентрации также
уменьшает сродство ГЕМОГЛОБИН к О2. Снижение сродства при уменьшении
рН в интервале 9-6 называют щелочным эффектом Бора, который обусловлен существованием
равновесия:
Этот эффект
вносит значительной вклад в поддержание постоянного значения рН крови и освобождение
О2 в тканях соответственно уровню обмена веществ [увеличение концентрации
СО2 сдвигает равновесие реакций (1) и (2) вправо]. В легких, где
рСО2 составляет 40 мм рт. ст., процессы, описываемые реакциями
(1) и (2), идут в обратном направлении, в результате чего СО2,
находящийся в растворенном и связанном с ГЕМОГЛОБИН состоянии, освобождается, ГЕМОГЛОБИН
оксигенируется и дыхат. цикл завершается.
У человека на разных этапах развития организма обнаружено несколько
Г., различающихся составляющими их субъединицами. На ранних стадиях эмбрионального
развития у зародыша обнаруживаются ГЕМОГЛОБИН строения,,
. На более поздних стадиях появляется и доминирует к моменту рождения HbF
(; так называемой
фетальный ГЕМОГЛОБИН). Св-ва эмбриональных ГЕМОГЛОБИН обеспечивают выполнение кисло-родтранспортной
функции в специфический условиях внутриутробной жизни. В эритроцитах взрослого
человека содержится в норме 95-97% НЬА
, начинающего преобладать через 2-3 месяца после рождения, и 2-3% НbА2
Первичные структуры
иполипептидных
цепей ГЕМОГЛОБИН человека, а также многие др. глобиновых цепей различные происхождения
известны. Гены, кодирующиеглобиновые
цепи ГЕМОГЛОБИН человека, сцеплены и расположены в последовательности
на хромосоме 16 (цифры-номера дуплицированных генов); группа генов, кодирующих
др. полипептидные цепи, также непосредственно примыкающие один к другому,
локализована на хромосоме 11. Первичная структураи
неглобиновых
генов человека известна. Для каждого из них установлено наличие двух нитронов
(отрезков ДНК, прерывающих кодирующие участки,-экзоны) и больших некодирующих
участков, находящихся на флангах генов. Биосинтез тема,
иглобиновых
цепей, а также сборка тетрамерных молекул НbА осуществляется в клетках
эритроцитарного ряда и практически завершается к моменту выхода зрелых
эритроцитов (их продолжительность жизни у человека составляет 120-130 дней)
из костного мозга в кровяное русло.
Точковые мутации в экзонах глобиновых генов могут вести к появлению
мутантных ГЕМОГЛОБИН с единичной аминокислотной заменой. Это может быть причиной молекулярных
болезней — наследств. гемоглобинопатий. наиболее известный пример мутантного
Г.- HbS, в котором шестой от N-концаглобиновой
цепи остаток глутаминовой кислоты заменен на остаток валина. Такой ГЕМОГЛОБИН содержится
в эритроцитах больных серповидноклеточной анемией. Точечная мутация, делеция
(выпадение участка ДНК) или другой дефект глобинового гена, локализованный
вне экзонов, может уменьшить продукцию глобиновых цепей в эритроцитах,
нарушить сбалансированный биосинтезицепей
и привести к др. распространенной разновидности гемоглобинопатий-талассемии.
Химическая энциклопедия. Том 1 >> К списку статей
Введение в химию окружающей среды.
Книга известных английских ученых раскрывает основные принципы химии окружающей
среды и их действие в локальных и глобальных масштабах. Важный аспект книги
заключается в раскрытии механизма действия природных геохимических процессов в
разных масштабах времени и влияния на них человеческой деятельности.
Показываются химический состав, происхождение и эволюция земной коры, океанов и
атмосферы. Детально рассматриваются процессы выветривания и их влияние на
химический состав осадочных образований, почв и поверхностных вод на континентах.
Для студентов и преподавателей факультетов биологии, географии и химии
университетов и преподавателей средних школ, а также для широкого круга
читателей.
Химия и технология редких и рассеянных элементов.
Книга представляет собой учебное пособие по специальным курсам для студентов
химико-технологических вузов. В первой части изложены основы химии и технологии
лития, рубидия, цезия, бериллия, галлия, индия, таллия. Во
второй
части книги изложены основы химии и технологии скандия, натрия, лантана,
лантаноидов, германия, титана, циркония, гафния. В
третьей части книги изложены основы химии и технологии ванадия, ниобия,
тантала, селена, теллура, молибдена, вольфрама, рения. Наибольшее внимание
уделено свойствам соединений элементов, имеющих значение в технологии. В
технологии каждого элемента описаны важнейшие области применения, характеристика
рудного сырья и его обогащение, получение соединений из концентратов и отходов
производства, современные методы разделения и очистки элементов. Пособие
составлено по материалам, опубликованным из советской и зарубежной печати по
1972 год включительно.
Источник