Насыщение гемоглобина кислородом происходит в
Содержание статьи
Строение и общие закономерности функционирования органов дыхания. Часть 3.
- Предыдущая
- 1 of 3
- Следующая
В этой части речь идет о переносе газов кровью: о значении физических факторов для переноса газов кровью, о роли давления газов в их переносе кровью, о кислородной емкости крови, о содержании газов в крови, о связывании кислорода кровью, о связывании углекислого газа кровью.
Перенос газов кровью.
Значение физических факторов для переноса газов кровью.
Растворение газов в жидкостях зависит от ряда факторов: от свойств самого газа, от свойств жидкости (концентрации в ней солей, ее температуры), от объема и давления газа над жидкостью.
Показателем растворимости газов служит коэффициент растворимости (или абсорбционный коэффициент). Его величина показывает тот объем газа, который растворяется в 1 см3 жидкости при температуре 0 градусов Цельсия и давлении 760 мм рт.ст.
Коэффициент растворимости газа тем больше, чем ниже температура; он уменьшается с повышением температуры и при температуре кипения равен нулю (газ из раствора весь испаряется). Коэффициент растворимости в крови для кислорода равен 0,022, для азота — 0,011, для углекислоты — 0,511.
В состоянии растворения в артериальной крови содержится 0,25 мл О2, 2,69 мл СО2 и 1,04 мл N.
Физическое растворение газов очень мало, а поэтому оно не имеет большого значения для их переноса кровью. Важным фактором переноса газов кровью является образование химических соединений с веществами плазмы крови и эритроцитов. Для установления химических связей и физического растворения газов важна величина давления газа над жидкостью.
Роль давления газов в их переносе кровью.
Поступление газа в жидкость зависит от его давления. Если над жидкостью находится смесь газов, то движение и растворение каждого из них зависят от его парциального давления. Парциальное давление можно рассчитать исходя из общего давления смеси газов и их процентного содержания.
Всю газовую смесь атмосферного воздуха принимают за 100%, он обладает давлением 760 мм рт.ст., а часть газа (О2 — 20,95%) принимают за X. Отсюда: X=(760х20,95):100=159,22 мм рт.ст. При расчете парциального давления газов в альвеолярном воздухе необходимо учитывать, что он насыщен водяными парами, давление которых составляет 47 мм рт.ст. Следовательно, на долю газовой смеси, входящей в состав альвеолярного воздуха приходится давления не 760 мм рт.ст., а 760-47=713 мм рт.ст. Это давление принимается за 100%.
Отсюда легко вычислить, что парциальное давление О2, который содержится в альвеолярном воздухе в количестве 14,3%, будет равно: (713х14,3):100=102 мм рт.ст.
Соответственный расчет парциального давления СО2 показывает, что оно равно 40 мм рт.ст.
Альвеолярный воздух контактирует с тонкими стенками легочных капилляров, по которым приходит к легким венозная кровь. Интенсивность обмена газов и направление их движения (из легких в кровь или из крови в легкие) зависят от парциального давления кислорода и углекислоты в газовой смеси в легких и в крови (давление газов в жидкостях называют их напряжением).
Напряжение кислорода в венозной крови равно 40 мм рт.ст., углекислоты — 46 мм рт.ст. Движение газов осуществляется от большего давления к меньшему. Следовательно. кислород будет поступать из легких (его парциальное давление в них равно 102 мм рт.ст.) в кровь (его напряжение в крови 400 мм рт.ст.) в альвеолярный воздух (давление 40 мм рт.ст.)
Кислородная емкость крови. Содержание газов в крови.
В крови кислород соединяется с гемоглобином и образует непрочное соединение — оксигемоглобин. Насыщение крови кислородом зависит от количества гемоглобина в крови. Максимальное количество кислорода, которое может поглотить 100 мл крови, называют кислородной емкостью крови. Известно, что в 100 г крови человека содержится 14% гемоглобина. Каждый грамм гемоглобина может связать 1,34 мл О2. Значит, 100 мл крови могут перенести 1,34х14%=19 мл (или 19 объемных процентов). Это и есть кислородная емкость крови.
Можно рассчитать степень насыщения крови кислородом. Для этого нужно разделить содержание кислорода исследуемой крови на ее кислородную емкость.
Связывание кислорода кровью.
В артериальной крови 0,25 объемного процента О2 находится в состоянии физического растворения в плазме, а остальные 18,75 объемного процента — в эритроцитах в связанном состоянии с гемоглобином в виде оксигемоглобина. Связь гемоглобина с кислородом зависит от величины напряжения газов: если оно увеличивается, гемоглобин присоединяет кислород и образуется оксигемоглобин (НВО2). При уменьшении напряжения кислорода оксигемоглобин распадается и отдает кислород. Кривую, отражающую зависимость насыщения гемоглобина кислородом от напряжения последнего, называют кривой диссоциации оксигемоглобина. Даже при небольшом парциальном давлении кислорода (40 мм рт.ст.) с ним связываются 75-80% гемоглобина. При давлении 80-90 мм рт.ст. гемоглобин почти полностью насыщается кислородом. В альвеолярном воздухе парциальное давление кислорода равно 120 мм рт.ст., поэтому кровь в легких будет полностью насыщена кислородом.
При рассмотрении кривой диссоциации оксигемоглобина можно заметить, что при уменьшении парциального давления кислорода оксигемоглобин подвергается диссоциации и отдает кислород. При нулевом давлении кислорода оксигемоглобин может отдать весь соединенный с ним кислород.
Свойство гемоглобина — легко насыщаться кислородом, даже при небольших давлениях, и легко его отдавать — очень важно.
Благодаря легкой отдаче гемоглобином кислорода при снижении парциального давления обеспечивается бесперебойное снабжение тканей кислородом, в которых вследствие постоянного потребления кислорода его парциальное давление равно нулю.
Распад оксигемоглобина на гемоглобин и кислород увеличивается с повышением температуры тела.
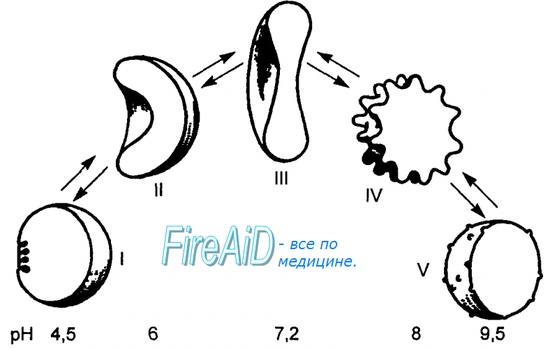
Диссоциация оксигемоглобина зависит от реакции среды плазмы крови. С увеличением кислотности крови возрастает диссоциация оксигемоглобина.
Связывание гемоглобина с кислородом в воде осуществляется быстро, но полного его насыщения не достигается, так же как не происходит полной отдачи кислорода при снижении его парциального давления. Более полное насыщение гемоглобина кислородом и полная его отдача при понижении напряжения кислорода происходят в растворах солей и в плазме крови.
Особое значение в связывании гемоглобина с кислородом имеет содержание СО2 в крови. Чем больше содержится углекислоты в крови, тем меньше связывается гемоглобин с кислородом и тем быстрее происходит диссоциация оксигемоглобина. Особенно резко понижается способность гемоглобина соединяться с кислородом при давлении СО2, равном 46 мм рт.ст. в венозной крови. Влияние СО2 на диссоциацию оксигемоглобина очень важно для переноса газов в легких и тканях.
В тканях содержится большое количество СО2 и других кислых продуктов распада, образующихся в результате обмена веществ. Переходя в артериальную кровь тканевых капилляров, они способствуют более быстрому распаду оксигемоглобина и отдаче кислорода тканям.
В легких же, по мере выделения СО2 из венозной крови в альвеолярный воздух. с уменьшением содержания СО2 в крови увеличивается способность гемоглобина соединяться с кислородом. Тем самым обеспечивается превращение венозной крови в артериальную.
Связывание углекислого газа кровью.
В артериальной крови содержится 50-52% СО2, а в венозной на 5-6% больше — 55-58%. из них 2,5-2,7 объемного процента в состоянии физического растворения, а остальная часть СО2 переносится в виде солей угольной кислоты: бикарбоната натрия (NaHCO3) в плазме и бикарбоната калия (KHCO3) — в эритроцитах. Часть углекислого газа (от 10 до 20 объемных процентов) может транспортироваться в виде соединений с аминогруппой гемоглобина — карбгемоглобина.
Из всего количества СО2 большая его часть (2/3) переносится плазмой крови.
Одной из важнейших реакций, обеспечивающих транспорт СО2, является образование угольной кислоты из СО2 и Н2О:
H2O+CO2↔H2CO3
Такая реакция в крови ускоряется приблизительно в 20 000 раз. Большая скорость этой реакции обеспечивается ферментом карбоангидразой. При увеличении содержания СО2 в крови (что бывает в тканях) фермент способствует гидратации СО2 и реакция идет в сторону образования Н2СО3. При уменьшении парциального напряжения СО2 в крови (что имеет место в легких) фермент карбоангидраза способствует дегидратации Н2СО3 и реакция идет в сторону образования СО2 иН2О. Это обеспечивает наиболее быструю отдачу СО2 в альвеолярный воздух.
Связывание СО2 кровью, так же как и кислорода, зависит от парциального давления. Можно построить кривые диссоциации углекислоты, отложив на оси абсцисс парциальное давление СО2, а на оси ординат — количество связанного углекислого газа в объемных процентах. Кривая показывает, что связывание СО2 кровью увеличивается по мере возрастания его парциального давления.
При парциальном напряжении СО2, равном 40 мм рт.ст. (что соответствует его напряжению в артериальной крови), в крови содержится 52% углекислоты. При напряжении СО2, равном 46 мм рт.ст. (что соответствует напряжению в венозной крови), содержание СО2 возрастает до 58%.
На связывание СО2 кровью влияет присутствие оксигемоглобина в крови. Эту зависимость можно проследить при переходе артериальной крови в венозную. Сравнение нижней кривой и верхней НА РИСУНКЕ
показывает, что при превращении артериальной крови в венозную солями гемоглобина отдается кислород и тем самым облегчается ее насыщение углекислым газом. При этом содержание СО2 в ней увеличивается на 6%: с 52% до 58%.
В сосудах легких образование оксигемоглобина способствует отдаче СО2, содержание которого при превращении венозной крови в артериальную уменьшается с 58 до 52 объемных процентов. В присутствии кислорода из крови удаляется весь СО2 при его нулевом напряжении в окружающей среде. В присутствии азота, даже при нулевом напряжении СО2 в окружающей среде, часть его остается связанным с кровью.
Источник
родство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
Оглавление темы «Вентиляция легких. Перфузия легких кровью.»: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. — Также рекомендуем «Углекислый газ. Транспорт углекислого газа.» |
Источник
ранспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
Оглавление темы «Вентиляция легких. Перфузия легких кровью.»:
1. Вентиляция легких. Вентиляция кровью легких. Физиологическое мертвое пространство. Альвеолярная вентиляция.
2. Перфузия легких кровью. Влияние гравитации на вентиляцию легких. Влияние гравитации на перфузию легких кровью.
3. Коэффициент вентиляционно-перфузионных отношений в легких. Газообмен в легких.
4. Состав альвеолярного воздуха. Газовый состав альвеолярного воздуха.
5. Напряжение газов в крови капилляров легких. Скорость диффузии кислорода и углекислого газа в легких. Уравнение Фика.
6. Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
7. Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
8. Углекислый газ. Транспорт углекислого газа.
9. Роль эритроцитов в транспорте углекислого газа. Эффект Холдена..
10. Регуляция дыхания. Регуляция вентиляции легких.
Транспорт газов кровью. Транспорт кислорода. Кислородная емкость гемоглобина.
Кровообращение выполняет одну из важнейших функций переноса кислорода от легких к тканям, а углекислого газа — от тканей к легким. Потребление кислорода клетками тканей может изменяться в значительных пределах, например при переходе от состояния покоя к физической нагрузке и наоборот. В связи с этим кровь должна обладать большими резервами, необходимыми для увеличения ее способности переносить кислород от легких к тканям, а углекислый газ в обратном направлении.
Транспорт кислорода.
При 37 С растворимость 02 в жидкости составляет 0,225 мл • л-1 • кПа-1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т. е. 13,3 кПа или 100 мм рт.ст., 1 л плазмы крови может переносить только 3 мл 02, что недостаточно для жизнедеятельности организма в целом. В покое в организме человека за минуту потребляется примерно 250 мл кислорода. Чтобы тканям получить такое количество кислорода в физически растворенном состоянии, сердце должно перекачивать за минуту огромное количество крови. В эволюции живых существ проблема транспорта кислорода была более эффективно решена за счет обратимой химической реакции с гемоглобином эритроцитов. Кислород переносится кровью от легких к тканям организма молекулами гемоглобина, которые содержатся в эритроцитах.
Гемоглобин способен захватывать кислород из альвеолярного воздуха (соединение называется ок-сигемоглобином) и освобождать необходимое количество кислорода в тканях. Особенностью химической реакции кислорода с гемоглобином является то, что количество связанного кислорода ограничено количеством молекул гемоглобина в эритроцитах крови. Молекула гемоглобина имеет 4 места связывания с кислородом, которые взаимодействуют таким образом, что зависимость между парциальным давлением кислорода и количеством переносимого кислорода с кровью имеет S-образную форму, которая носит название кривой насыщения или диссоциации оксигемоглобина (рис. 10.18). При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10 %, а при Р02 30 мм рт. ст. — 50—60 %. При дальнейшем увеличении парциального давления кислорода от 40 мм рт. ст. до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина и процент его насыщения кислородом возрастает в диапазоне от 70—75 до 90 % соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6 %. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. В результате кривая диссоциации оксигемоглобина переходит в горизонтальную линию и процент насыщения гемоглобина кислородом достигает предела, т. е. 100. Насыщение гемоглобина кислородом под влиянием Р02 характеризует своеобразный молекулярный «аппетит» этого соединения к кислороду.
Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне парциального давления от 20 до 40 мм рт. ст. способствует тому, что в ткани организма значительное количество кислорода может диффундировать из крови в условиях фадиента его парциального давления между кровью и клетками тканей (не менее 20 мм рт. ст.). Незначительный процент насыщения гемоглобина кислородом в диапазоне его парциального давления от 80 до 100 мм рт. ст. способствует тому, что человек без риска снижения насыщения артериальной крови кислородом может перемещаться в диапазоне высот над уровнем моря до 2000 м.
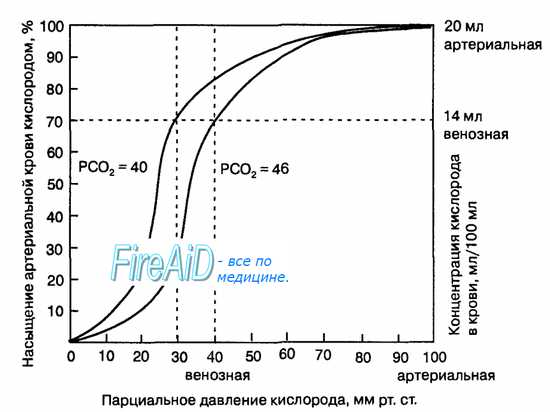
Рис. 10.18. Кривая диссоциации оксигемоглобина. Пределы колебания кривой при РС02 = 40 мм рт. ст. (артериальная кровь) и РС02 = 46 мм рт. ст. (венозная кровь) показывают изменение сродства гемоглобина к кислороду (эффект Ходена).
Общие запасы кислорода в организме обусловлены его количеством, находящимся в связанном состоянии с ионами Fe2+ в составе органических молекул гемоглобина эритроцитов и миоглобина мышечных клеток.
Один грамм гемоглобина связывает 1,34 мл 02. Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл 02.
Количество 02, которое может связаться с гемоглобином эритроцитов крови при насыщении 100 % его количества, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание 02 в крови (кислородная емкость крови), которое отражает его истинное количество, как связанного с гемоглобином, так и физически растворенного в плазме. Поскольку в норме артериальная кровь насыщена кислородом на 97 %, то в 100 мл артериальной крови содержится примерно 19,4 мл 02.
— Также рекомендуем «Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.»
Источник