Низкий гемоглобин при хобл
Содержание статьи
Анемии при хронической обструктивной болезни легких
АПФ — ангиотензинпревращающий фермент
АХЗ — анемия хронических заболеваний
ИЛ — интерлейкин
ОФВ1 — объем форсированного выдоха за 1-ю секунду
РААС — ренин-ангиотензин-альдостероновая система
СН — сердечная недостаточность
СРБ — С-реактивный белок
ХОБЛ — хроническая обструктивная болезнь легких
ЭПО — эритропоэтин
MCV (mean cell volume) — средний объем эритроцита
α-ФНО — α-фактор некроза опухоли
Хроническая обструктивная болезнь легких (ХОБЛ) в настоящее время является четвертой по частоте причиной смертности по всему миру, и по прогнозам к 2020 г. может выйти на третье место. Среди известных факторов риска развития ХОБЛ особое значение придается курению (активному и пассивному), общему старению населения, воздействию профессиональных вредных факторов и промышленных поллютантов [1, 2]. Несвоевременное выявление заболевания, недостаточная эффективность терапии значительно повышают риск обострения ХОБЛ [3—7]. В структуре легочных заболеваний экономические затраты, связанные с лечением обострений ХОБЛ, занимают значительное место и уступают лишь раку легких [1—4]. Системные проявления и сопутствующие хронические заболевания, среди которых наиболее изучены сердечно-сосудистые, остеопороз и рак легких, ухудшают состояние пациентов с ХОБЛ и прогноз в целом, поэтому профилактика ХОБЛ и ее обострений являются социально значимыми и экономическими обоснованными мероприятиями [2]. ХОБЛ на протяжении многих лет ассоциирована с эритроцитозом, однако в последнее время стали появляться сообщения об относительно часто встречающейся анемии, возможно, влияющей на прогноз, качество жизни и выживаемость больных ХОБЛ.
Распространенность анемии при ХОБЛ. Распространенность анемии у больных ХОБЛ колеблется от 10 до 30% и чаще встречается у пациентов с тяжелой формой заболевания и частыми обострениями, при которых требуется госпитализация, в то время как истинная полицитемия (эритроцитоз) наблюдается достаточно редко [7]. Всемирная организация здравоохранения рекомендует диагностировать анемии при снижении концентрации гемоглобина менее 130 г/л у мужчин и менее 120 г/л у женщин [8]. В то же время, используя в качестве диагностического критерия анемии только уровень гемоглобина, следует учитывать следующие аспекты: 1) с увеличением возраста распространенность анемии в популяции увеличивается; 2) пороговый уровень гемоглобина у пожилых женщин в постменопаузе остается спорным [9]; 3) «относительная анемия» у больных ХОБЛ — термин, используемый для описания случаев, в которых нормальный уровень гемоглобина не коррелирует с тяжестью гипоксии. Опубликованы данные о распространенности впервые выявленной анемии у больных со стабильным течением ХОБЛ. Из 100 пациентов с тяжелым течением ХОБЛ (объем форсированного выдоха за 1-ю секунду — ОФВ1 37±2% от должного) 13 страдали анемией [10]. Результаты исследования ANTADIR (Association National pour le Traitement a Dominicile de I’Insuffiance Respiratory) показали сходную распространенность анемии среди 2524 больных ХОБЛ, находившихся на длительной кислородной терапии, у 12,6% мужчин и 8,2% женщин [11]. Среди 683 больных ХОБЛ, наблюдавшихся в амбулаторных условиях, анемия выявлена у 17%, а полицитемия — у 6%, у госпитализированных больных распространенность анемии оказалась выше — до 33% [9]. M. John и соавт. [12] сравнили распространенность анемии у больных, госпитализированных по поводу ХОБЛ, и у пациентов с другими хроническими заболеваниями (бронхиальная астма, хроническая сердечная недостаточность — СН, хроническая почечная недостаточность). Среди 7337 обследованных больных анемия выявлена у 23%. Сходные результаты обнаружились у пациентов с С.Н. Распространенность анемии у больных ХОБЛ оказалась выше, чем в группе больных бронхиальной астмой, но ниже, чем у пациентов с хронической почечной недостаточностью. В другом исследовании среди 177 больных с обострением ХОБЛ анемия диагностирована у 31%, из них наиболее часто встречалась нормоцитарная нормохромная анемия (у 58%), в то время как полицитемия выявлена только у 8 (4,5%) [13]. Стоит отметить, что частота развития анемии у больных с ХОБЛ остается актуальным вопросом, и до сих пор нет данных о ее истинной распространенности [14, 15].
Патогенез анемии при ХОБЛ. В последнее время все больше данных свидетельствует о системном характере ХОБЛ. У многих пациентов заболевание ассоциировано с внелегочными проявлениями, которые отражают системный воспалительный процесс. Помимо возможной роли воспаления в этиологии анемии при ХОБЛ не следует забывать, что процесс старения увеличивает распространенность анемии в популяции [7].
Так называемая анемия хронических заболеваний (АХЗ), как прежде всего иммунное расстройство, встречается при многих хронических воспалительных состояниях. Воспалительные цитокины с разных сторон влияют на патогенез анемии и в конечном счете нарушают нормальный эритропоэз. Основные механизмы достаточно сложны и включают дисрегуляцию обмена железа и продукции эритропоэтина (ЭПО), нарушение пролиферации эритроидных клеток-предшественников и снижение продолжительности жизни эритроцитов [15]. Кроме того, активация воспалительных медиаторов может стимулировать выработку гепсидина — полипептида, который является главным регулятором внеклеточного гомеостаза железа и, как полагают, играет ключевую роль в развитии АХЗ. Как правило, АХЗ является нормоцитарной нормохромной, однако при прогрессировании болезни может трансформироваться в микроцитарную и гипохромную. Характерные изменения системного распределения железа проявляются снижением концентрации железа в сыворотке крови и насыщения трансферрина, в то время как макрофагальные запасы железа остаются на высоком уровне [16]. В одном из исследований процент воспалительных маркеров в периферической крови и мокроте у больных ХОБЛ в сочетании с анемией оказался значительно выше, чем в контрольной группе [17].
Считается, что наиболее важными медиаторами, участвующими в патогенезе АХЗ, являются С-реактивный белок (СРБ), фибриноген, некоторые интерлейкины (ИЛ), такие как ИЛ-6, ИЛ-8, а также α-фактор некроза опухоли (α-ФНО). У больных ХОБЛ также обнаружено увеличение выраженности окислительного стресса, особенно во время обострений заболевании [18]. S. Tassiopoulos и соавт. [19] одни из первых оценили связь АХЗ с ХОБЛ. Первоначальная цель состояла в сравнении компенсаторных механизмов эритропоэза у пациентов с идиопатическим фиброзом легких и ХОБЛ. Предполагалось, что гематологические механизмы проявят себя по-разному при этих двух заболеваниях и что явления вторичного эритроцитоза будут выявлены у больных ХОБЛ с хронической гипоксией. Однако результаты оказались противоречивыми. У пациентов с ХОБЛ уровень гемоглобина был нормальным или сниженным, несмотря на высокие концентрации ЭПО в плазме [19]. Эти данные подтверждены результатами другого исследования, в котором также обнаружены более высокие уровни СРБ и ИЛ-6 у больных ХОБЛ [10]. Уровень СРБ оказался значительно выше в подгруппе больных с анемией, как и уровень ЭПО в сыворотке крови. Кроме того, ученые продемонстрировали обратную корреляцию между уровнем гемоглобина и ЭПО, что свидетельствует об устойчивости к его влиянию на эритропоэз у этих больных [10]. Таким образом, в отсутствие данных о другом генезе анемии (хронический дефицит железа и др.) можно предположить, что анемия, ассоциированная с ХОБЛ, соответствует критериям АХЗ.
Анемии и обострения ХОБЛ. Считается, что при обострении ХОБЛ усиленная локальная и системная воспалительная реакция усугубляет внелегочные проявления болезни, включая анемию [13, 20]. В двух недавних исследованиях изучены уровни ЭПО и СРБ в плазме в следующих группах пациентов: 1-я госпитализированные по поводу обострения ХОБЛ (n=26; ОФВ1 48±15% от должного); 2-я пациенты с клинически стабильным течением ХОБЛ (n=31; ОФВ1 49±17% от должного); 3-я курильщики с нормальной функцией легких (n=9); 4-я здоровые лица, которые никогда не курили (n=9). По результатам исследования выяснилось, что уровень ЭПО в плазме во время обострения ХОБЛ значительно ниже, чем в других группах. Во 2-й группе уровень ЭПО зависел от концентрации СРБ (r=–0,55; р<0,0001) и циркулирующих нейтрофилов (r=–0,48; р<0,0001). У 8 больных со стабильным течением ХОБЛ уровень ЭПО был значительно выше, чем у представителей других групп (р<0,0001). Эти наблюдения демонстрируют подавление выработки ЭПО во время обострения ХОБЛ, что может быть обусловлено выраженностью системного воспаления [21]. В другом исследовании, в котором приняли участие 93 пациента, уровень гемоглобина, ЭПО и сывороточных маркеров системного воспаления (СРБ, α-ФНО, фибриноген и ИЛ-6) оценивались при госпитализации больных с обострением ХОБЛ, после купирования симптомов дыхательной недостаточности и после стабилизации состояния. Уровень гемоглобина при поступлении был значительно ниже, чем на последующих двух этапах (p=0,002), в то время как в отношении ЭПО прослеживалась обратная зависимость [22].
Макроцитоз. А. Tsantes и соавт. [23] обнаружили увеличение среднего объема эритроцитов (MCV — mean cell volume) у пациентов с ХОБЛ, однако причины этого явления недостаточно изучены. Данный феномен исследовался у 32 больных ХОБЛ с гипоксемией и 34 здоровых добровольцев. Оценивались общий анализ крови, процент F-клеток (эритроциты, содержащие фетальный гемоглобин), газовый состав артериальной крови, и уровень ЭПО. Макроцитоз (MCV >94 фл) выявлялся у 43,75% больных ХОБЛ, эритроцитоз — у 37%. При этом уровень ЭПО часто не зависел от степени гипоксемии, эритроцитоза или макроцитоза. Процент F-клеток оказался значительно выше у пациентов с ХОБЛ, и этот параметр коррелировал с MCV. Основываясь на полученных результатах, авторы предположили, что эритропоэтиновый стресс при ХОБЛ является результатом обострения заболевания, ночных или ассоциированных с нагрузкой эпизодов гипоксемии [23]. Следствием роста уровня ЭПО может быть активация компенсаторных механизмов в виде увеличения продукции незрелых клеток в костном мозге с целью оптимизации кислородной емкости крови. Несмотря на выраженную гипоксемию, уровень ЭПО может оставаться в пределах нормы даже при сниженной концентрации гемоглобина [23]. Известно о 17 (29%) случаях макроцитоза у 58 больных ХОБЛ без признаков дыхательной недостаточности. Клинически значимой находкой оказалась корреляция между макроцитозом, степенью выраженности одышки и ОФВ1 в подгруппе из 9 (36%) больных ХОБЛ, что, по-видимому, доказывает связь макроцитоза с ухудшением клинических показателей [24].
Ренин-ангиотензин-альдостероновая система (РААС). В нескольких клинических и экспериментальных исследованиях показана роль активации нейрогуморальных механизмов у больных ХОБЛ, которые предположительно вносят вклад в патогенез системных эффектов заболевания [25]. Увеличение секреции ЭПО наблюдалось у экспериментальных животных после введения ренина или ангиотензина II. Использование ингибиторов ангиотензинпревращающего фермента (АПФ) сопровождалось снижением уровня ЭПО. Связь активации РААС с развитием компенсаторного эритроцитоза у лиц с ХОБЛ продемонстрирована в исследовании D. Vlahakos и соавт. [26]. Уровни ренина и альдостерона у пациентов с эритроцитозом оказались в 3 раза выше, чем в контрольной группе. Таким образом, предполагается, что различная степень активации РААС позволяет частично объяснить разные уровни гемоглобина у больных ХОБЛ с одной и той же степенью гипоксемии.
Другие аспекты анемии при ХОБЛ. ЭПО синтезируется прежде всего в почках и любое ухудшение гемодинамики, сопутствующее ХОБЛ, часто приводит к снижению почечного кровотока, вызывая дисбаланс в потребности и доставке кислорода, что влияет на синтез ЭПО [27].
Андрогены также могут стимулировать эритропоэз, оказывая непосредственное стимулирующее влияние на предшественники эритроцитов, или косвенно, путем активации РААС. Анемия нередко встречается у мужчин с гипогонадизмом или у лиц, получающих препараты, которые подавляют синтез андрогенов. Существуют доказательства, что у мужчин с ХОБЛ концентрация тестостерона ниже нормы; кроме того, его уровень снижается с возрастом [28]. Предполагается, что снижению уровня андрогенов в плазме крови способствуют хроническая гипоксия и лечение глюкокортикостероидами. В исследовании с участием 905 мужчин старше 65 лет показан высокий риск развития анемии у пациентов с низким уровнем тестостерона [29].
Считается, что ингибиторы АПФ снижают гематокрит. Теофиллин угнетает синтез эритроцитов, причем механизм этого является сложным и может быть результатом прямого ингибирования эритропоэза путем апоптоза, индуцированного данным препаратом, а не какого-либо эффекта, связанного с ЭПО [30].
Хорошо известно, что анемия сама служит причиной одышки и способствует ограничению функциональных возможностей. Повышенная утомляемость также частое явление как у больных ХОБЛ, так и у пациентов с анемией. Существует мнение, что анемия служит одной из наиболее легко устранимых причин усталости в целом. В исследовании с использованием шкалы для оценки выраженности одышки (Medical Research Council — MRC) выявлено, что у больных ХОБЛ с анемией одышка значительно более выражена и снижена переносимость физической нагрузки, оцененная с применением теста с 6-минутной ходьбой [9].
Существуют доказательства снижения продолжительности жизни больных ХОБЛ с анемией. Длительное наблюдение за больными со стабильным течением ХОБЛ показало, что у пациентов с меньшей продолжительностью жизни уровни гематокрита значительно ниже, чем в отсутствие анемии [31]. Результаты исследования ANTADIR свидетельствуют, что гематокрит является важным предиктором выживаемости больных ХОБЛ, получавших длительную кислородную терапию. Трехлетняя выживаемость составила 24% у пациентов с гематокритом менее 35% и 70% у пациентов с гематокритом более 55% [11]. Множественный регрессионный анализ показал, что основными факторами риска смерти больных после 3 лет наблюдения были мужской пол, низкие уровни гемоглобина, гематокрита, гипоксемия и одышка. Высокая летальность характерна для больных с уровнем гемоглобина ≤110 г/л (чувствительность 95%, специфичность 85%) и гематокритом ≤33% (чувствительность 97%, специфичность 89%) [32].
Лечение анемии при ХОБЛ. В предыдущих разделах мы попытались объяснить некоторые клинические и патофизиологические аспекты, которые могли бы повысить значение анемии у больных ХОБЛ, соответственно, обосновать необходимость ее коррекции у пациентов этого контингента. Тем не менее доказательств в пользу улучшения выживаемости больных с ХОБЛ после лечения анемии недостаточно [33]. Опубликованы результаты двух противоречивых исследований о пользе лечения анемии у больных ХОБЛ. Снижение минутного дыхательного объема зафиксировано практически у всех пациентов с тяжелым течением ХОБЛ после переливания крови с целью лечения анемии [33]. Раннее исследование, проведенное этой же группой ученых, показало невозможность перевода с искусственной вентиляции легких на самостоятельное дыхание без коррекции анемии [34]. Варианты лечения анемии (препараты железа, комбинированная терапия), используемые при других хронических заболеваниях, таких как застойная СН, хроническая болезнь почек, еще недостаточно изучены у больных ХОБЛ. Неизвестно также, может ли лечение самой ХОБЛ, а именно коррекция хронического воспаления, оказать положительное влияние на показатели крови.
Учитывая изложенное, можно прийти к выводу, что анемия нередко встречается у больных ХОБЛ, однако ее реальная распространенность у этого контингента пациентов остается неопределенной, а механизмы, способствующие ее возникновению, плохо изучены. Для решения этих вопросов, а также для определения тактики лечения больных ХОБЛ с анемией требуется проведение дополнительных исследований.
Конфликт интересов отсутствует.
Источник
причины, симптомы и лечение в статье врача УЗИ Никитина И. Л.
Дата публикации 29 марта 2018Обновлено 19 июля 2019
Определение болезни. Причины заболевания
Хроническая обструктивная болезнь лёгких (ХОБЛ) — заболевание, которое набирает обороты, продвигаясь в рейтинге причин смерти людей старше 45 лет. На сегодняшний день болезнь стоит на 6-м месте среди ведущих причин смертности в мире, по прогнозам ВОЗ в 2020 г. ХОБЛ займёт уже 3-е место.
Данная болезнь коварна тем, что основные симптомы болезни, в частности, при табакокурении проявляются лишь через 20 лет после начала курения. Оно долгое время не даёт клинических проявлений и может протекать бессимптомно, однако, в отсутствии лечения незаметно прогрессирует обструкция дыхательных путей, которая становится необратимой и ведёт к ранней нетрудоспособности и сокращению продолжительности жизни в целом. Поэтому тема ХОБЛ представляется в наши дни особенно актуальной.
Важно знать, что ХОБЛ — это первично хроническое заболевание, при котором важна ранняя диагностика на начальных стадиях, так как болезнь имеет тенденцию к прогрессированию.
Если врач поставил диагноз «Хроническая обструктивная болезнь лёгких (ХОБЛ)», у пациента возникает ряд вопросов: что это значит, насколько это опасно, что изменить в образе жизни, какой прогноз течения болезни?
Итак, хроническая обструктивная болезнь лёгких или ХОБЛ – это хроническое воспалительное заболевание с поражением мелких бронхов (воздухоносных путей), которое приводит к нарушению дыхания за счёт сужения просвета бронхов.[1] С течением времени в лёгких развивается эмфизема. Так называется состояние, при котором снижается эластичность лёгких, то есть их способность сжиматься и расширяться в процессе дыхания. Лёгкие при этом находятся постоянно как будто в состоянии вдоха, в них всегда, даже во время выдоха, остается много воздуха, что нарушает нормальный газообмен и приводит к развитию дыхательной недостаточности.
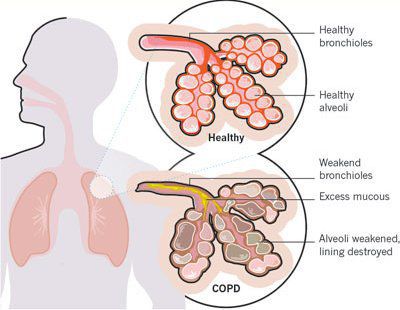
Причинами заболевания ХОБЛ являются:
- воздействие вредных факторов окружающей среды;
- табакокурение;
- факторы профессиональной вредности (пыль содержащая кадмий, кремний);
- общее загрязнение окружающей среды (выхлопные газы автомобилей, SO2, NO2);
- частые инфекции дыхательных путей;
- наследственность;
- дефицит α1-антитрипсина.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы хронической обструктивной болезни легких
ХОБЛ — болезнь второй половины жизни, чаще развивается после 40 лет. Развитие болезни — постепенный длительный процесс, чаще незаметный для пациента.
Обратиться к врачу заставляют появившиеся одышка и кашель — самые распространённые симптомы заболевания (одышка почти постоянная; кашель частый и ежедневный, с выделениями мокроты по утрам).[2]
Типичный пациент с ХОБЛ — курящий человек 45-50 лет, жалующийся на частую одышку при физической нагрузке.
Кашель — один из самых ранних симптомов болезни. Он часто недооценивается пациентами. На начальных стадиях болезни кашель носит эпизодический характер, но позже становится ежедневным.
Мокрота также относительно ранний симптом заболевания. На первых стадиях она выделяется в небольших количествах, в основном по утрам. Характер слизистый. Гнойная обильная мокрота появляется во время обострения заболевания.
Одышка возникает на более поздних стадиях заболевания и отмечается вначале только при значительной и интенсивной физической нагрузке, усиливается при респираторных заболеваниях. В дальнейшем одышка модифицируется: ощущение недостатка кислорода во время обычных физических нагрузкок сменяется тяжёлой дыхательной недостаточностью и через время усиливается. Именно одышка становится частой причиной для того, чтобы обратиться к врачу.
Когда можно заподозрить наличие ХОБЛ?
Вот несколько вопросов алгоритма ранней диагностики ХОБЛ:[1]
- Кашляете ли Вы каждый день по нескольку раз? Беспокоит ли это Вас?
- Возникает ли при откашливании мокрота или слизь (часто/ежедневно)?
- У Вас быстрее/чаще появляется одышка, в сравнении со сверстниками?
- Вы старше 40 лет?
- Курите ли Вы и приходилось ли курить раньше?
При положительно ответе более чем на 2 вопроса необходимо проведение спирометрии с бронходилятационным тестом. При показателе теста ОФВ1/ФЖЕЛ ≤ 70 определяется подозрение на ХОБЛ.
Патогенез хронической обструктивной болезни легких
При ХОБЛ страдают как дыхательные пути, так и ткань самого лёгкого — лёгочная паренхима.
Начинается заболевание в мелких дыхательных путях с закупорки их слизью, сопровождающейся воспалением с формированием перибронхиального фиброза (уплотнение соединительной ткани) и облитерации (зарастание полости).
При сформировавшейся патологии бронхитический компонент включает:
- гиперплазию слизистых желёз (избыточное новообразование клеток)[4];
- слизистое воспаление и отёк;
- бронхоспазм и закупорку дыхательных путей секретом, что приводит к сужению дыхательных путей и увеличению их сопротивления.
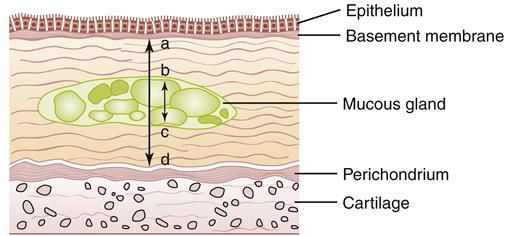
Эмфизематозный компонент приводит к разрушению конечных отделов дыхательных путей — альвеолярных стенок и поддерживающих структур с образованием значительно расширенных воздушных пространств. Отсутствие тканевого каркаса дыхательных путей приводит к их сужению вследствие тенденции к динамическому спадению во время выдоха, что становится причиной экспираторного коллапса бронхов.[4]
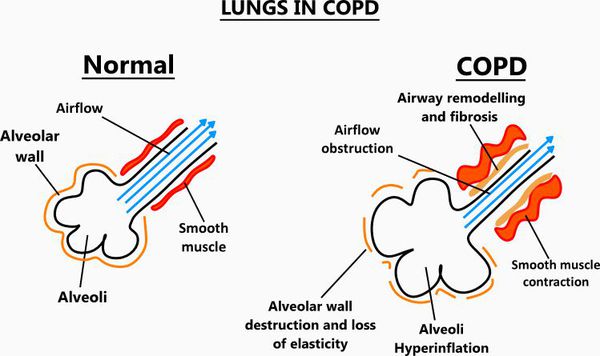
Ко всему прочему, разрушение альвеолярно-капиллярной мембраны влияет на газообменные процессы в лёгких, снижая их диффузную способность. В результате этого возникают уменьшение оксигенации (кислородное насыщения крови) и альвеолярной вентиляции. Происходит избыточная вентиляция недостаточно перфузируемых зон, приводящая к росту вентиляции мёртвого пространства и нарушению выведения углекислого газа СО2. Площадь альвеолярно-капиллярной поверхности уменьшена, но может быть достаточной для газообмена в состоянии покоя, когда эти аномалии могут не проявляться. Однако при физической нагрузке, когда потребность в кислороде возрастает, если дополнительных резервов газообменивающихся единиц нет, то возникает гипоксемия — недостаток содержания кислорода в крови.
Появившаяся гипоксемия при длительном существовании у пациентов с ХОБЛ включает ряд адаптивных реакций. Повреждение альвеолярно-капиллярных единиц вызывает подъём давления в лёгочной артерии. Поскольку правый желудочек сердца в таких условиях должен развивать большее давление для преодоления возросшего давления в лёгочной артерии, он гипертрофируется и расширяется (с развитием сердечной недостаточности правого желудочка). Кроме того, хроническая гипоксемия способна вызывать увеличение эритропоэза, который впоследствии увеличивает вязкость крови и усиливает правожелудочковую недостаточность.
Классификация и стадии развития хронической обструктивной болезни легких
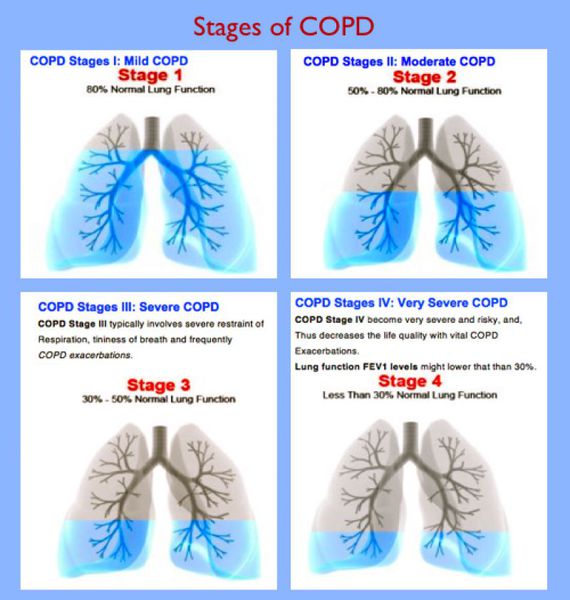
| Стадия течения ХОБЛ | Характеристика | Наименование и частота надлежащих исследований |
|---|---|---|
| I. легкая | Хронический кашель и продукция мокроты обычно, но не всегда. ОФВ1/ФЖЕЛ ≤ 70% ОФВ1 ≥ 80% должных величин | Клинический осмотр, спирометрия с бронходилятационным тестом 1 раз в год. В период ХОБЛ — общий анализ крови и рентгенография органов грудной клетки. |
| II. среднетяжёлая | Хронический кашель и продукция мокроты обычно, но не всегда. ОФВ1/ФЖЕЛ ≤ 50% ОФВ1 | Объём и частота исследований те же |
| III.тяжёлая | Хронический кашель и продукция мокроты обычно, но не всегда. ОФВ1/ФЖЕЛ ≤ 30% ≤ОФВ1 | Клинический осмотр 2 раза в год, спирометрия с бронходилятационным тестом и ЭКГ 1 раз в год. В период обострения ХОБЛ — общий анализ крови и рентгенография органов грудной клетки. |
| IV. крайне тяжёлая | ОФВ1/ФЖЕЛ ≤ 70 ОФВ1 ОФВ1 в сочетании с хронической дыхательной недостаточностью или правожелудочковой недостаточностью | Объём и частота исследований те же. Сатурация кислородом (SatO2) – 1-2 раза в год |
Осложнения хронической обструктивной болезни легких
Осложнениями ХОБЛ являются инфекции, дыхательная недостаточность и хроническое лёгочное сердце. Также у пациентов с ХОБЛ с большей частотой встречается бронхогенная карцинома (рак лёгкого), хотя она не является непосредственным осложнением болезни.

Дыхательная недостаточность — состояние аппарата внешнего дыхания, при котором либо не обеспечивается поддержание напряжения О2 и СО2 в артериальной крови на нормальном уровне, либо оно достигается за счёт повышенной работы системы внешнего дыхания. Проявляется, главным образом, одышкой.
Хроническое лёгочное сердце — увеличение и расширение правых отделов сердца, которое происходит при повышении артериального давления в малом круге кровообращения, развившееся, в свою очередь, в результате лёгочных заболеваний. Основной жалобой пациентов также является одышка.
Диагностика хронической обструктивной болезни легких
Если у пациентов кашель, выделение мокроты, одышки, а также были выявлены факторы риска развития хронической обструктивной болезни лёгких, то у них у всех должен предполагаться диагноз ХОБЛ.
Для того, чтобы установить диагноз, учитываются данные клинического обследования (жалобы, анамнез, физикальное обследование).
При физикальном обследовании могут выявляться симптомы, характерные для длительно протекающего бронхита: «часовых стекол» и/или «барабанных палочек» (деформация пальцев), тахипноэ (учащённое дыхание) и одышка, изменение формы грудной клетки (для эмфиземы характерна бочкообразная форма), малая подвижность её во время дыхания, западение межреберных промежутков при развитии дыхательной недостаточности, опущение границ лёгких, изменение перкуторного звука на коробочный, ослабленное везикулярное дыхание или сухие свистящие хрипы, которые усиливаются при форсированном выдохе (то есть быстром выдохе после глубокого вдоха). Тоны сердца могут прослушиваться с трудом. На поздних стадиях может иметь место диффузный цианоз, выраженная одышка, появляются периферические отёки. Для удобства заболевание подразделяют на две клинические формы: эмфизематозную и бронхитическую. Хотя в практической медицине чаще встречаются случаи смешанной формы заболевания.
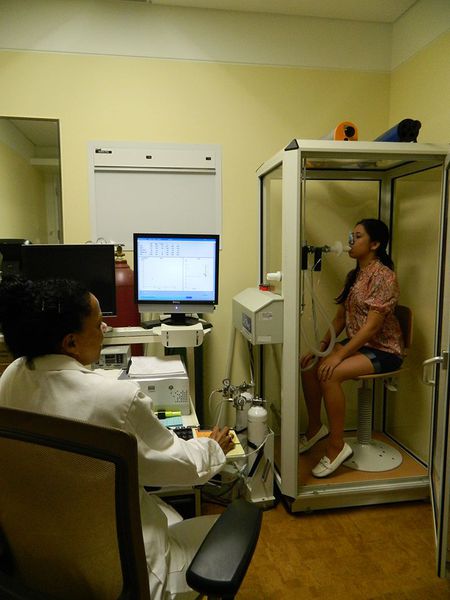
Самый важный этап диагностики ХОБЛ — анализ функции внешнего дыхания (ФВД). Он необходим не только для определения диагноза, но и для установления степени тяжести заболевания, составления индивидуального плана лечения, определения эффективности терапии, уточнения прогноза протекания болезни и оценки трудоспособности. Установление процентного соотношения ОФВ1/ФЖЕЛ чаще всего применяется в лечебной практике. Уменьшение объема форсированного выдоха в первую секунду к форсированной жизненной ёмкости лёгких ОФВ1/ФЖЕЛ до 70 % — начальный признак ограничения воздушного потока даже при сохранённой ОФВ1>80% должной величины. Низкая пиковая скорость потока воздуха на выдохе, незначительно меняющаяся при применении бронходилятаторов также говорит в пользу ХОБЛ. При впервые диагностируемых жалобах и изменениях показателей ФВД спирометрия повторяется на протяжении года. Обструкция определяется как хроническая, если она фиксируется не менее 3-х раз за год (невзирая на проводимое лечение), и диагностируется ХОБЛ.
Мониторирование ОФВ1 — важный метод подтверждения диагноза. Спиреометрическое измерение показателя ОФВ1 осуществляется многократно на протяжении нескольких лет. Норма ежегодного падения ОФВ1 для людей зрелого возраста находится в пределах 30 мл в год. Для пациентов с ХОБЛ характерным показателем такого падения является 50 мл в год и более.
Бронхолитический тест — первичное обследование, при котором определяется максимальный показатель ОФВ1, устанавливаются стадия и степень тяжести ХОБЛ, а также исключается бронхиальная астма (при положительном результате), избирается тактика и объём лечения, оценивается эффективность терапии и прогнозируется течение заболевания. Очень важно отличить ХОБЛ от бронхиальной астмы, так как у этих часто встречаемых заболеваний одинаковое клиническое проявление — бронхообструктивный синдром. Однако подход к лечению одного заболевания отличается от другого. Главный отличительный признак при диагностике — обратимость бронхиальной обструкции, которая является характерной особенностью бронхиальной астмы. Установлено, что у людей с диагнозом ХОБЛ после приёма бронхолитика процент увеличения ОФВ1 — менее 12% от исходного (или ≤200 мл), а у пациентов с бронхиальной астмой он, как правило, превышает 15%.
Рентгенография грудной клетки имеет вспомогательное значение, так как изменения появляются лишь на поздних стадиях заболевания.
ЭКГ может выявлять изменения, которые характерны для лёгочного сердца.
ЭхоКГ необходима для выявления симптомов лёгочной гипертензии и изменений правых отделов сердца.
Общий анализ крови — с его помощью можно оценить показатели гемоглобина и гематокрита (могут быть повышены из-за эритроцитоза).
Определение уровня кислорода в крови (SpO2) – пульсоксиметрия, неинвазивное исследование для уточнения выраженности дыхательной недостаточности, как правило, у больных с тяжёлой бронхиальной обструкцией. Кислородная насыщенность крови менее 88%, определяемая в покое, указывает на выраженную гипоксемию и необходимость назначения оксигенотерапии.
Лечение хронической обструктивной болезни легких
Лечение ХОБЛ способствует:
- уменьшению клинических проявлений;
- повышению толерантности к физической нагрузке;
- профилактике прогрессирования болезни;
- профилактике и лечению осложнений и обострений;
- повышению качества жизни;
- снижению смертности.
К основным направлениям лечения относятся:
- ослабление степени влияния факторов риска;
- образовательные программы;
- медикаментозное лечение.
Ослабление степени влияния факторов риска
Отказ от курения обязателен. Именно это является наиболее эффективным способом, который снижает риск развития ХОБЛ.
Производственные вредности также следует контролировать и снижать их влияние, применяя адекватную вентиляцию и воздухоочистители.
Образовательные программы
Образовательные программы при ХОБЛ включают в себя:
- базовые знания о заболевании и общих подходах к лечению с побуждением пациентов к прекращению курения;
- обучение тому, как правильно использовать индивидуальные ингаляторы, спейсеры, небулайзеры;
- практику самоконтроля с применением пикфлоуметров, изучение мер неотложной самопомощи.
Обучение пациентов занимает значимое место в лечении пациентов и влияет на последующий прогноз (уровень доказательности А).
Метод пикфлоуметрии даёт возможность пациенту ежедневно самостоятельно контролировать пиковый объём форсированного выдоха — показатель, тесно коррелирующий с величиной ОФВ1.
Пациентам с ХОБЛ на каждой стадии показаны физические тренирующие программы с целью увеличения переносимости физических нагрузок.
Медикаментозное лечение
Фармакотерапия при ХОБЛ зависит от стадии заболевания, тяжести симптомов, выраженности бронхиальной обструкции, наличия дыхательной или правожелудочковой недостаточности, сопутствующих заболеваний. Препараты, которые борются с ХОБЛ, делятся на средства для снятия приступа и для профилактики развития приступа. Предпочтение отдают ингаляционным формам препаратов.

Для купирования редких приступов бронхоспазма назначают ингаляции β-адреностимуляторов короткого действия: сальбутамол, фенотерол.
Препараты для профилактики приступов:
- формотерол;
- тиотропия бромид;
- комбинированные препараты (беротек, беровент).
Если применение ингаляции невозможно или их эффективность недостаточна, то возможно необходимо применение теофиллина.
При бактериальном обострении ХОБЛ требуется подключение антибиотиков. Могут быть применены: амоксициллин 0,5-1 г 3 раза в сутки, азитромицин по 500 мг трое суток, кларитромицин СР 1000 мг 1 раз сутки, кларитромицин 500 мг 2 раза в сутки, амоксициллин + клавулановая кислота 625 мг 2 раза в сутки, цефуроксим 750 мг 2 раза в сутки.
Снятию симптомов ХОБЛ также помогают глюкокортикостероиды, которые также вводят ингаляционно (беклометазона дипропионат, флутиказона пропионат). Если ХОБЛ протекает стабильно, то назначение системных глюкокортикостероидов не показано.
Традиционные отхаркивающие и муколитические средства дают слабый положительный эффект у пациентов с ХОБЛ.
У тяжёлых пациентов с парциальным давлением кислорода (рО2) 55 мм рт. ст. и менее в покое показана кислородотерапия.
Прогноз. Профилактика
На прогноз заболевания влияет стадия ХОБЛ и число повторных обострений. При этом любое обострение негативно сказывается на общем течении процесса, поэтому крайне желательна как можно более ранняя диагностика ХОБЛ. Лечение любого обострения ХОБЛ следует начинать максимально рано. Важно также полноценная терапия обострения, ни в коем случае не допустимо переносить его «на ногах».
Зачастую люди решаются обратиться к врачу за медицинской помощью, начиная со II среднетяжелой стадии. При III стадии болезнь начинает оказывать довольно сильное влияние на пациента, симптомы становятся более выраженным (нарастание одышки и частые обострения). На IV стадии происходит заметное ухудшение качества жизни, каждое обострение становится угрозой для жизни. Течение болезни становится инвалидизирующим. Эта стадия сопровождается дыхательной недостаточностью, не исключено развитие лёгочного сердца.
На прогноз заболевания влияет соблюдение больным медицинских рекомендаций, приверженность лечению и здоровому образу жизни. Продолжение курения способствует прогрессированию заболевания. Отказ от курения приводит к замедлению прогрессирования заболевания и замедлению снижения ОФВ1. В связи с тем, что заболевание имеет прогрессирующее течение, многие пациенты вынуждены принимать лекарственные средства пожизненно, многим требуются постепенно возрастающие дозы и дополнительные средства в период обострений.
Наилучшим