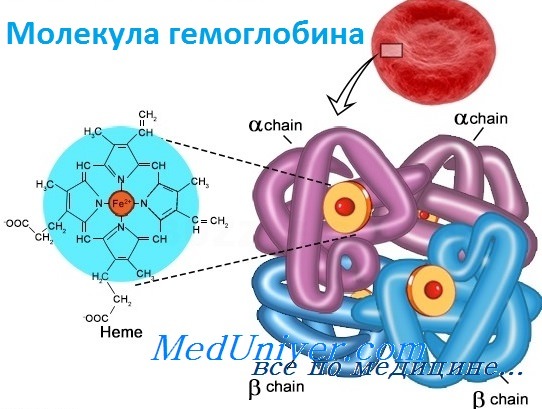
Объединение четырех глобул в молекулу гемоглобина
Содержание статьи
труктура и функция гемоглобина
Структура и функция гемоглобинаБолезни гемоглобинов человека, названные гемоглобинопатиями, занимают уникальную позицию в медицинской генетике. Это наиболее частые моногенные болезни у людей, к тому же вызывающие высокую смертность. По оценке Всемирной организации здравоохранения более 5% человеческой популяции — носители мутаций клинически значимых нарушений гемоглобина. Кроме того, поскольку гемоглобин был одной из первых исследованных белковых структур, а гены глобина у человека стали первыми клонированными генами, связанными с болезнями, их молекулярная и биохимическая патология изучена лучше, чем в любой другой группе генетических болезней. Глобины также проливают свет на процесс как молекулярной, так и популяционной эволюции и служат моделью действия генов в развитии. Прежде чем подробно обсуждать гемоглобинопатии, опишем вкратце нормальное состояние гена глобина и биологию гемоглобина. Гемоглобин — переносчик кислорода в эритроцитах позвоночных. Его молекула содержит четыре субъединицы: две а-цепи и две b-цепи. Каждая субъединица формируется цепью полипептида глобина и простетической группой, гемом, железосодержащим пигментом, соединяющимся с кислородом, придавая молекуле способность транспортировать кислород.
Каждая молекула гемоглобина состоит из двух пар полипептидных цепей разного типа. Цепи глобина в нормальном гемоглобине взрослых, гемоглобине А (НЬА), названы а и b соответственно. Четыре цепи складываются и объединяются, формируя шарообразный тетрамер с молекулярным весом приблизительно 64 500, структуру, обозначаемую для НbА — а2b2. Оба типа цепей почти равны по длине; а-цепь имеет 141 аминокислоту, b-цепь — 146. Цепи имеют заметное сходство друг с другом в аминокислотной последовательности (первичной структуре) и в трехмерной конфигурации (третичной структуре). Основные характеристики структуры глобина весьма консервативно сохранялись в ходе эволюции, что стало основой для понимания гемоглобинопатии. Более того, третичная структура полипептида глобина также оказалась в высшей степени консервативной: фактически все изученные глобины имеют семь или восемь извитых участков (в зависимости от цепи). В то же время только две аминокислоты сохраняются во всех глобинах в природе, и неудивительно, что мутации в любом из этих остатков связаны с болезнью. Исследование структуры гемоглобина позволило предсказать, какие типы мутаций, вероятно, окажутся патогенными. Таким образом, мутации, изменяющие строение глобина, замена высококонсервативной аминокислоты или одного из неполярных остатков, формирующих гидрофобную оболочку, исключающую попадание воды внутрь молекулы, вероятно, вызовут гемоглобинопатию. Как и все белки, глобин имеет «чувствительные области», мутации в которых не могут не влиять на функцию, и «нечувствительные области», мутации в которых переносятся более свободно. Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021 — Также рекомендуем «Гены гемоглобина человека» Оглавление темы «Выявление генов болезни»:
|
Источник
емоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.
| Оглавление темы «Функции клеток крови. Эритроциты. Нейтрофилы. Базофилы.»: 1. Функции клеток крови. Функции эритроцитов. Свойства эритроцитов. Цикл Эмбдена-Мейергофа. Строение эритроцитов. 2. Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина. 3. Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты. 4. Железо. Железо в норме. Роль ионов железа в эритропоэзе. Трансферрин. Потребность организма в железе. Дефицит железа. ОЖСС. 5. Эритропоэз. Эритробластические островки. Анемия. Эритроцитоз. 6. Регуляция эритропоэза. Эритропоэтин. Половые гормоны и эритропоэз. 7. Лейкоциты. Лейкоцитоз. Лейкопения. Гранулоциты. Лейкоцитарная формула. 8. Функции нейтрофильных гранулоцитов ( лейкоцитов ). Дефенсины. Кателицидины. Белки острой фазы. Хемотаксические факторы. 9. Бактерицидный эффект нейтрофилов. Гранулопоэз. Нейтрофильный гранулопоэз. Гранулоцитоз. Нейтропения. 10. Функции базофилов. Функции базофильных гранулоцитов. Нормальное количество. Гистамин. Гепарин. Гемоглобин. Типы ( виды ) гемоглобина. Синтез гемоглобина. Функция гемоглобина. Строение гемоглобина.Гемоглобин — это гемопротеин, с молекулярной массой около 60 тыс., окрашивающий эритроцит в красный цвет после связывания молекулы O2 с ионом железа (Fe++). У мужчин в 1 л крови содержится 157 (140-175) г гемоглобина, у женщин — 138 (123-153) г. Молекула гемоглобина состоит из четырех субъединиц гема, связанных с белковой частью молекулы — глобином, сформированной из полипептидных цепей.
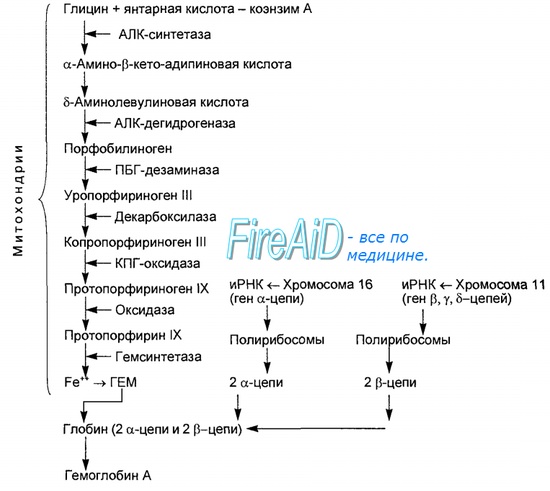
Синтез гема протекает в митохондриях эритробластов. Синтез цепей глобина осуществляется на полирибосомах и контролируется генами 11-й и 16-й хромосом. Схема синтеза гемоглобина у человека представлена на рис. 7.2. Гемоглобин, содержащий две а- и две В-цепи, называется А-тип (от adult — взрослый). 1 г гемоглобина А-типа связывает 1,34 мл O2. В первые три месяца жизни плода человека в крови содержатся эмбриональные гемоглобины типа Gower I (4 эпсилон цепи) и Gower II (2а и 25 цепи). Затем формируется гемоглобин F (от faetus — плод). Его глобин представлен двумя цепями а и двумя В. Гемоглобин F обладает на 20-30 % большим сродством к O2, чем гемоглобин А, что способствует лучшему снабжению плода кислородом. При рождении ребенка до 50-80 % гемоглобина у него представлены гемоглобином F и 15-40 % — типом А, а к 3 годам уровень гемоглобина F снижается до 2 %. Соединение гемоглобина с молекулой 02 называется оксигемоглобином. Сродство гемоглобина к кислороду и диссоциация оксигемоглобина (отсоединения молекул кислорода от оксигемоглобина) зависят от напряжения кислорода (Р02), углекислого газа (РС02) в крови, рН крови, ее температуры и концентрации 2,3-ДФГ в эритроцитах. Так, сродство повышают увеличение Р02 или снижение РС02 в крови, нарушение образования 2,3-ДФГ в эритроцитах. Напротив, повышение концентрации 2,3-ДФГ, снижение Р02 крови, сдвиг рН в кислую сторону, повышение РС02 и температуры крови — уменьшают сродство гемоглобина к кислороду, тем самым облегчая ее отдачу тканям. 2,3-ДФГ связывается с р-цепями гемоглобина, облегчая отсоединение 02 от молекулы гемоглобина. Увеличение концентрации 2,3-ДФГ наблюдается у людей, тренированных к длительной физической работе, адаптированных к длительному пребыванию в горах. Оксигемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. В состоянии физиологического покоя у человека гемоглобин в артериальной крови на 97 % насыщен кислородом, в венозной — на 70 %. Чем выраженней потребление кислорода тканями, тем ниже насыщение венозной крови кислородом. Например, при интенсивной физической работе потребление кислорода мышечной тканью увеличивается в несколько десятков раз и насыщение кислородом оттекающей от мышц венозной крови снижается до 15 %. Содержание гемоглобина в отдельном эритроците составляет 27,5-33,2 пикограмма. Снижение этой величины свидетельствует о гипохромном (т. е. пониженном), увеличение — о гиперхромном (т. е. повышенном) содержании гемоглобина в эритроцитах. Этот показатель имеет диагностическое значение. Например, гиперхромия эритроцитов характерна для В|2-дефицитной анемии, гипохромия — для железодефицитной анемии. — Также рекомендуем «Старение эритроцитов. Разрушение эритроцитов. Длительность жизни эритроцита. Эхиноцит. Эхиноциты.» |
Источник
Гемоглобин
Гемоглобин (от др.-греч. Гемо — кровь и лат. globus — шар) — это сложная белковая молекула внутри красных клеток крови — эритроцитов (у человека и позвоночных животных). Гемоглобин составляет примерно 98% массы всех белков эритроцита.
Гемоглобин (от др.-греч. Гемо — кровь и лат. globus — шар) — это сложная белковая молекула внутри красных клеток крови — эритроцитов (у человека и позвоночных животных). Гемоглобин составляет примерно 98% массы всех белков эритроцита. За счет своей структуры гемоглобин участвует в переносе кислорода от легких к тканям, и оксида углерода обратно.
Строение гемоглобина
Гемоглобин состоит из двух цепей глобина типа альфа и двух цепей другого типа (бета, гамма или сигма), соединенными с четырьмя молекулами гемма, содержащего железо. Структура гемоглобина записывается буквами греческого алфавита: α2γ2.
Обмен гемоглобина
Гемоглобин образуется эритроцитами в красном костном мозге и циркулирует с клетками в течение всей их жизни — 120 дней. Когда селезенкой удаляются старые клетки, компоненты гемоглобина удаляются из организма или поступают обратно в кровоток, чтобы включиться в новые клетки.
Типы гемоглобина
К нормальным типам гемоглобина относится гемоглобин А или HbA (от adult — взрослый), имеющий структуру α2β2, HbA2 (минорный гемоглобин взрослого, имеющий структуру α2σ2 и фетальный гемоглобин (HbF, α2γ2. Гемоглобин F — гемоглобин плода. Замена на гемоглобин взрослого полностью происходит к 4-6 месяцам (уровень фетального гемоглобина в этом возрасте менее 1%). Эмбриональный гемоглобин образовывается через 2 недели после оплодотворения, в дальнейшем, после образования печени у плода, замещается фетальным гемоглобином.
| Тип гемоглобина | Процент содержания у взрослого человека |
| HbA — взрослый гемоглобин | 98% |
| HbA2 — взрослый гемоглобин минорный | Около 2% |
| HbFi — фетальный гемоглобин | 0,5-1% |
| Эмбриональный гемоглобин | нет |
| HbA1C — гликированный гемоглобин |
Аномальных гемоглобинов более 300, их называют по месту открытия.
Функция гемоглобина
Основная функция гемоглобина — доставка кислорода от легких к тканям и углекислого газа обратно.
Формы гемоглобина
- Оксигемоглобин — соединение гемоглобина с кислородом. Оксигемоглобин преобладает в артериальной крови, идущей от легких к тканям. Из-за содержания оксигемоглобина артериальная кровь имеет алый цвет.
- Восстановленный гемоглобин или дезоксигемоглобин (HbH) — гемоглобин, отдавший кислород тканям
- Карбоксигемоглобин — соединение гемоглобина с углекислым газом. Находится в венозной крови и придает ей темный вишневый цвет.
Как же это происходит? Почему в легких гемоглобин забирает, а в тканях отдает кислород?
Эффект Бора
Эффект был описан датским физиологом Христианом Бором https://en.wikipedia.org/wiki/Christian_Bohr (отцом знаменитого физика Нильса Бора).
Христиан Бор заявил, что при большей кислотности (более низкое значение рН, например, в тканях) гемоглобин будет меньше связываться с кислородом, что позволит его отдать.
В легких, в условиях избытка кислорода, он соединяется с гемоглобином эритроцитов. Эритроциты с током крови доставляют кислород ко всем органам и тканям. В тканях организма с участием поступающего кислорода проходят реакции окисления. В результате этих реакций образуются продукты распада, в том числе, углекислый газ. Углекислый газ из тканей переносится в эритроциты, из-за чего уменьшается сродство к кислороду, кислород выделяется в ткани.
Эффект Бора имеет громадное значение для функционирования организма. Ведь если клетки интенсивно работают, выделяют больше СО2, эритроциты могут снабдить их большим количеством кислорода, не допуская кислородного «голодания». Следовательно, эти клетки могут и дальше работать в высоком темпе.
Какой уровень гемоглобина в норме?
В каждом миллилитре крови содержится около 150 мг гемоглобина! Уровень гемоглобина меняется с возрастом и зависит от пола. Так, у новорожденных гемоглобин значительно выше, чем у взрослых, а у мужчин выше, чем у женщин.
Что еще влияет на уровень гемоглобина?
Некоторые другие состояния также влияют на уровень гемоглобина, например, пребывание на высоте, курение, беременность.
Заболевания, связанные с изменением количества или структуры гемоглобина
- Повышение уровня гемоглобина наблюдается при эритроцитозах, обезвоживании.
- Снижение уровня гемоглобина наблюдается при различных анемиях.
- При отравлении угарным газом образуется карбгемоглобин (не путайте с карбоксигемоглобином!), который не может присоединять кислород.
- Под действием некоторых веществ образуется метгемоглобин.
- Изменение структуры гемоглобина называется гемоглобинопатией. Самые известные и частые заболевания этой группы — серповидно-клеточная анемия, бета-талассемия, персистенция фетального гемоглобина. См.гемоглобинопатии на сайте Всемирной организации здравоохранения https://www.who.int/centre/factsheets/fs308/ru/index.html
Знаете ли Вы?
- У беспозвоночных животных гемоглобин растворен в плазме крови.
- В сутки из легких в ткани переносится около 600 литров кислорода!
- Красный цвет крови придает гемоглобин, входящий в состав эритроцитов. У некоторых червей вместо гемоглобина хлорокруорин и кровь зеленая. А у каракатиц, скорпионов и пауков голубая, так как вместо гемоглобина — содержащий медь гемоцианин.
Другие статьи раздела
Распространенный возбудитель инфекций дыхательных путей (фарингиты, синуситы, отиты, бронхиты и пневмонии). Анализы на антитела используются для диагностики инфекции Chlamydophila pneumoniae при длительных инфекциях дыхательных путей.
Mycoplasma pneumoniae — возбудитель пневмонии человека, острых респираторных заболеваний (ОРЗ), заболеваний верхних дыхательных путей (фарингита, бронхита), а также некоторых нереспираторных заболеваний.
Азооспермия (azoospermia) — отсутствие сперматозоидов в эякуляте
Бактерии — одноклеточные микроорганизмы, некоторые из которых могут вызывать заболевания.
Mycoplasma pneumoniae (микоплазма пневмонии), Chlamydohpila pneumoniae (хламидофила пневмонии, прежнее название Chlamydia pneumoniae)
Гипофиз — непарная железа внутренней секреции, расположенная на основании головного мозга в костном кармане — гипофизарной ямке турецкого седла. Гипофиз вырабатывает гормоны, оказывающие влияние на работу всего организма — рост и развитие, обмен веществ, половую функцию.
Повышенный рост волос (гирсутизм) может быть следствием не только повышенного уровня андрогенов (см. «гиперандрогения»), но и высокой активности 5-альфа-редуказы в коже (фермента волосяных фолликулов, превращающего тестостерон в гораздо более активный дигидротестостерон.
По данным ВОЗ (Всемирная организация здравоохранения) заболеваемость в России составляет более 50 человек на 100 000 населения. Имеет важное значение то, что у женщин значительно чаще чем у мужчин (50-90% против 10%) возможно бессимптомное течение заболевания.
Делеция (ген.) — вид хромосомных мутаций, при котором происходит потеря какого-либо участка хромосомы.
Механизм обратной связи — система, которая используется организмом для контроля некоторых функций и поддержания состояния постоянства организма. Механизм обратной связи использует один из продуктов пути обмена веществ, обычно конечный продукт, для контроля активности пути обмена веществ и регуляции количества этого продукта. Обратная связь может быть отрицательной и положительной.
Источник
ÌØï(~HçxÀlÁ£x AçÊ»î,S ËÀµÊH3q@€ ]âê endstream endobj 130 0 obj 474 endobj 103 0 obj > endobj 104 0 obj > /ExtGe > /ColorSpace > >> endobj 105 0 obj > endobj 106 0 obj > stream H‰|ÓiPSYð{^ÃË‹$l»‹È Á…a»EDPZAEA@š]$€ã†2 «8 .`·±ÙDµ¦¤G[{QÑÂr¤9I_ìžX=w¾ÌTWåÿ’œ_÷êü12à!Œ±qx`hDðb׈ 9[ÒR|üjš6ÊÈ܇lšfpè#F-`¬;n¢ë6½4Mu×ÍÕO!#d†¤È¹!_ô’´E¢•(}Š²ÑN´•¢£èÒ ‹¨ÝB}è;4ŒFÐ{4,ÆØ;c/âp…×âDœ·ãb| -ãø,nÄmø¾ïãAü~‹µ2Óâ7&%yzxx*iPÑà÷ŸàåAƒ’ ^4xÓàCƒ/ Ôñ¢Ž’: ê(¨£PÐ@ATÐ TVPÙ›ÊÞTö¦ 7ò¥ /}ÿû})¨¤ ‘n¨¤ ‘n¨¤ »J *)¨¤ Š’*º¡ŠÊ**«¨¬¢²ŠÊ**«¨¬¢²•ý¨ìGe?*ûQÙÊ~TöSÒ«Õß$FH€Ð$Œ¦ ¼!ã)ÈÖÍæ!»æ£e»´!BiíCh3Â{ÊExŸ OµAÓ’ži`ËEñÆ™¢¨U` jCí¨SôÍ»Gh=»£ýoß ÑM¤ÃîxÎÄGðiøFü5üNþKƒ5cLˆÀ@’x!Ö‰LD¢’I«&}6iÀ0ΰv²xrüäFœÑn£_§äMé;ˆÓÄ?‡ï2®1¾jâoRn2dfú7Ó7f§$»ÉJÉ•©>S7±˜Mb›Ìeæ9æc ‹R‹-¡-w¬VÉVç¬F9Äùp¯¥6Ò;{»b»>ûÙöwb:§{Loqtwl˜!ŸQ=cÈi™Óiç$çû..?»¦¸Îœ?³~æ¸[«[û,fÖ’Yî î/=»¼w»ïÅúhr/Âß/¯¹ëë{[Í?-M‡Ÿ@vƒÄé¢tùlPtH¤»4TÝP-w¤Å-n-÷ âaÜú& ƒó»Ò’#ûKåê’wÕIëÚKkêå%¸³9ÚqÝi†Œ9² rnÁÄÌ3k]Ù·À€ÑƒòÊ}©»íϪÊ=Q,’WÃâìøX’¹f÷¿ˆ!1v%¦ÄÚïzÔ°üÈE6;î³;CÝà
vmiÇ]®»¥ýVK_öô»âà9«e’3Ñìó97£pakã*’îu_íi>’‡ÄUCC;üÖ»[~»œQ~G±µ 6ÐÈOØGb6ÇŽH‰õлö’?o-Å’,bîM̲DУ²ió»¤þ±Ï€kmî:ûzIú´$mw¢ü÷*ÁP’µÁÿ©˜¾Ä§ÌôE&V ‘,}]ü¿³’š’‰Ÿÿ°äê.,&nYžLŠšaróæè:¢f³Î«ož@Ä?à»/¤½¨ma‹S˜½’Ïs3Ë7H‰ÉÇj£Óýu]%¯žÊ $½êðŠ»îIÁà1ðôïgq!Y¢.úr¯&`ªß;÷ÖÍCçåLJÀâ=«¥d½(AÙภ,íÈìs^AQœYT¦[«Ö±ÖqtW¦…Ý€ÏEWˆšHÔUD¢¢yKƒ»Ì0Ãðzpx©Dqa|Ç(¨•õíF-0fÕ¤XWVs{êŽ[ûøHE»ÝÚ¿Ý}Ϲç»çÞûõ¬püíäÔ-Eí’V(¸[°WJÒÀ¼£Ëèì|ò $·ÚëâBçxãÄ œh ÑGíRÆAˆ@EFš¡¸¢XP~ŽR0Qç’m×ed1©9™þÙJšÚ¿4»&¦kÄ…ÕÖIBsáŽhR …F)¦P²§oƒ®h9ÄcÀ•Ø,$³a¤ÛiY®àMtAP2gm¤»µA³»éÿú~øI-Rž4E…¶ª¶ÐÄ’Ã%ù« ›PTËÉg‹ƒö…Æ]5û·þ·i+-9¥lÕéR‰DwÕ)}Øî4Œ’X¦YV)²¨XujÏfg•&quþ¡¥Á,jP†Ÿá|œ£ÈÉéÑà2È%×H’üaz¼‹#qÊUØ¡@ƒ=üþûg8¾‰´R»‡,’Ã/EŠ® «›~Aá¿(ØÞà±à2ÂðNí¨(mi.jaÉ‹qΊsg»ÂÇ’Ä ë8Ù A7Ù£Pi~uŠA^(Þ Ö}¼‰ú…ØIŸ,TžìúyHôDÈFXL5·çMÑqìä©)ùëòÈ_•@uœß1µŠ«$Bn+Ü= 5¯yùm‹½çúÛ’èÎë;k8’Aªî p¢ÕVqH$-e- O%d%’±©ÉC,g ‰,Yâ‰4Ê L²»óWßüGU× ‰tmÁ‰~e‰€|ÉPJø9½),xÛÇ,zþœà3XæP¡øÞñÄeDÚ7f8-ؽv0ƒA|OiCx&{~Ubò·Ÿ‹oÇcYô¾Á2{ˆMòVx%Ã)ªv‹3 I¿ûi`!¯^³%>w_u-ò‹ôôÒd6&%5fã’ˆ¯ai!Ę8’}kÿ?~6Ž§÷©÷ä’2£» Ãi_Ág2 1ù±j¥-‘^Xxü»Ë˜z‡ã’Á|Ò±q}c}}kk}íý-]¶9×2vÈLòx0˜bÏ;Ï[®c^ùò!û™W&Nz¥¤Cl±•œ¨Áï(-æµ= »¬÷¥eT‰÷¤VݯÖm#…ÙÖ:ÒÆ»^}Ø!†wH`«’œ§Nÿ9!ô gmÉàAý$³¬½R£EJ½BÓ¼NÌ‹-A ªÍ2¦˜]&zL»Ž&¸pâÑÈCÜp.Ar!ˆÃ`pDwàôm ö 2 >è¾zd^d8mïŠNv-øøT;|ÕþªE»`»üö+0hè̮ڼ~qiÅT2w…*ô{+ÕuìI°ÏDgÏ?ùNTmÖëÉÈD?ÁríMæ- ôP ƒÞûŸÑçG€óAÂÌ€18>@ôÇ™èHöÕÌ>œnaÊ~»€×»˜¦· Rö»HÄ&ˆú‡A[b’l?Ù‰pÍ šþÚÇ[^iJêФî¦aÞ•Â*Z¦‹iÚ`Æ• q¸#ôuÃ0
ˇ’o°z·’Éœô°á8ò•-ón+#Ž2¨†’†£’dí-¸?ùq[-À ^漾ΚûwhwB^C ü}ÉÍ)Ì¡¢Š{±16£JºœÄL´š]¥oÑÖµ-`¡q»ÖâôÜeŽBʸ#ãB0pËŠÊË»õzýA1RªlΪÙçÂ×Qâå$¦´Ùpx軿.e=+¬KWù‹€:BݨLÎQ¤È˜wQÅRŒ4…z-Æ*]]¡Ÿì|ÚŠR+Õo›ó>Ú¿Jñ»£VØP]f9…—EFqåa¾ÇËb¤Á^Hµ»©15®žZ?½/‰OJŒÊŸ+…úl»=£¬¶R£Ñ»3`Îb¸%Š2Yžð¸¸0µ·•GôDt¹¤*ùâÁ‡sþ ž•uÆÆ®IÀ†õ6èä™Ù ¹»Y‹ýa·@S¨Ö -â2ZƒÌmºÇ^Ñs &U-fQ’Ž¿ OîÚDQZ•-U•æ0ji®*»ŠÎz`cà=Ö§ÜRe·OZ½ã^£1=Uš/.Èf-!=š öÔ~»Ö¬œÄIôúÉvÖ£Ãzê/ÀSRÏÓ4kÛ(ð塾‰mÖIyJI¬/…üxÐÇnãNž«ïã|-É¡®MÕZ›ÑÁ¤ôv¥ ú;j‡LB-÷pbòÇQ»ä°^-ÄTŠ²ì¢’ýŠ>θ;Ç’ŽÊÇÝÀ>Þ¥K‰%Å«wTU¨Ê+hUö)Y¶0F´JBóám88½ !Ÿ;9~vˆ:2ùÃó1h&¶…>·á»Àmc-s:ÙYÎàù$¼!™•H†J®BÈGà-Óá/ ðÐé¸|¶&clãõ?·’£œGb«ÝÀ»‡ý]ÏçWÁ÷š À Š’150ƒ÷‰²9ÝtÈe»ˆ+JÓb!JLÈŽ‹5§uÛ¯ÔÀ[D°ë&îsÍìSž`¦»Õ`0hKUt¾¡B©¡ìÚÓÕçö»H£½ÓÐfb&!€&†¼u÷ ¼ñ·àa¯•AÞKÜ?÷½Ï¬’P^³7µôwG¢×‹öG¬(‘·«éDô ²ëHö[Ä[Eï C(à Â#3‹+F!ärä»Áz@xÈdÿ ¼Ú£š¸³°ˆ™Ñ³%Ž¡©™ÖR+jÀéÁR,õuµ®¨( ò1ˆ$¢¼0$™ðÆÈ«VTÀnQWÁÓuøX+pù’3ó»¿ûÝï~÷~ÄWÑęƴÚ쵇 žŠÉ14Hù»c/ûEPFõ TT®Ý-*MܯôM#nài_]ZåÎ+X);¨)¬°ïÙxÀîeÒŒ&î¥Ä÷syUÜ: 9c¶WÓ˜&áÁÏ’3fÍ,µãå»G@ÖÁ¸?/Z¾K»±c >¦÷gãTÇ»NÇU»Êc•,Øwà¾z›+:Ä)´Åqœø§Ñˆ¡ñÄXÄ°uƒL~ûó†ñYÄ ß€=ιqE4óî áÌW7¥ð)®Êñ’1ñž(HòË«òÊXp¸ü‰Ç’ ÞHËã trŽq~˜-gªÑV°·CÞ_øÙš7öîÑj9qÕ¨ñ}z¦Yøƒ5ßûä;îȘµÄón ¯$K9«ÙbGÍ9CÅC@Ē퀉éüqÔÞ}¯‰tÂu¡Vx€SbqbàV vús,»P0åj,:âLÔ~ˆÈP˜ÌR¡š®Òœ½kµ»L¯ei€b-?àcªóì]’Ñ·Rñ0A®ÎµBÉx>IÕŠ˜»·ÃbœYôƒs°’j8™é¢åxÈRQ.ÙÛ2£Y%ÄʵÏp-çJòIsÉžØUÁ‡ØÕÒÑ|º3Ǚë*À}PÛƒÂÃ|UÓU ãéÄdcI©®oâ ‰ðØ$Žö AxH¤Wê’öIS’Se£Ÿúòáæím¨€VðŸÊªê*ó‰ÃG»§óKd°ªãp’ÙtUÎÙA’ö%ŒÙ4ÆÁNyw•´¢¼°Jf»¥ÉRwÀÕf¨:=Kp|äN ¼ëž`»˜¨/´µßÂËì® ïwÖù¢»ž‹ ó[ô¹-yðÇÁ`|Ée•ï»Îk®tÇq»U¢e WÝ€%››ðÒÐæ!œmâ i¦ù›ò+=ßKºÇ)áQê¬YzdzZ•OðÑ Áðg˜=ŽM ‘§È²fâ#¡vbÊi4X-ˆ»cHÈÍÏB¾0ܳ3 íUôM&Nê»1*$ZZlUF•R»3Ož-³~I/×ml[Öû ÐáL’Ì »öG`_aF0K}ëÓ±n :[ Þa’ßÈKߤ±™²§Ñ-*ê¶!Lξ`R@`»Re,RËŠÔIÆD6,=2y{]lgEe¡®ŒÇ‹©»Z+¥Œl£ÅÂ;cé¶ d Ø’Þª÷'»ôoîx`â
ˇ’ÜÕ]#´™€bg;²pd½$•’k÷«Xe²ÎÍ•ú‡dQ‹v¸=1Üж»cðê.¡Rôæâ…ñkYã’ë°Ø»pzø÷MøzÇÁEȦÒé$‡tÓlZ»‰LTS¾©¦²`ké£&¢ÑG L5yEå1WûÂ;õÕÏyP*A/x,Ê,Î.ÕKk닚Ⱦú¹Šî©8ÄÂ*òKŒ&›}¢Ê Kã)JyJL9©µkÈN}«Muu-{[aÑáü’Ý)RÕ~Ef*Y®zsù‡'»Mæ~ž¬XbPË+@m#ÑÖ Ü,ç»4žÎò’Œ±’Âøù’K±L1±(‡ipQƒßïa‹lüÁOÈLtuAËMk¥1ÂrCò¡ç6Â:)xÁÌóÃØÚçÁ̵è%Åu8wû‡yäNo>éLÓèØèË0‡×oO,tÀ¨HPøg’5|OÇ…i‹tYv’à-Œd’+¥òй†ˆŽ™§£ÛÚhÆ•Pï ‹!ª©½úø¥bÄ}:¯$9Yš»-œ-«CGŠbøLtÀ¡7Ikj[dVa:`˜#³ŸR³‡¿mrj (&q +_3’Éž ±»?*4¿¶’Ê’éò>ìúž»^’Òåð/Þæo$ŒŽ(ÄÈÚicAp>½ò ¾+›/jÞ-á$ÈO*Õt’‡JÉú-Ó€óŸÅ.ýGZü»ßìט»vûØQÿGü³4~áŠ9óßúF’vV·B×)h7Û@g‰RÝ¢ˆåg>t•…™ÅEù†QË’›zÉ`ÄlžêÍ+kúŠ… gm@o…ÔÂK÷7Êâ•»t¿ wXð’žaD»íßfâ’åÑÉ)Û¸m)!™š®éd¸ÎS±þ’àZ3«áŽïmð`b»À~‰R•˜-ÌîK×Wpð9]§ùzº,7%©ª.®-észéÑ2sÏ Ö;IæK3Å8’™Pœ.ÝTã{ôrÎÀ72Æg§Æ°¡ƒmklüm#G^ù¨^²W²#ŒõS˜[†4Ü«ãÄ!ê&aq¼ÒoÓ¦a[!|d£$%+5åã=Š¼=ì|ôÜßá°ßü8_ˆàWÞ0ÑÆoéÚx.»úsF=| Ky£†gOý%ÿÇ2Wÿs‰ÄwÁEp‡Å×êO=
Источник