Обмен углеводов и синтез холестерина
Содержание статьи
7.15. Взаимосвязь липидного и углеводного обменов
Обмен углеводов и липидов тесно взаимосвязан как в физиологических условиях, так и при патологии. Эта взаимосвязь возможна благодаря наличию общих метаболитов в обмене углеводов и липидов.
Углеводы могут использоваться для синтеза различных классов липидов.
Некоторые возможные пути перехода углеводов в липиды:
Глюкоза→фосфодигидроксиацетон→глицерофосфат→ТАГ, ФЛ
Глюкоза→ацетил-КоА→жирные кислоты, холестерин→липиды
Глюкоза→ ацетил-КоА→ холестерин→ стероиды
Глюкоза→НАДФН2(пентозофосфатный путь)→синтез жирных кислот, синтез сфингозина, синтез холестерина.
У детейуглеводы очень активно используются для синтеза липидов.
Схема взаимодействия углеводного и липидного обмена.
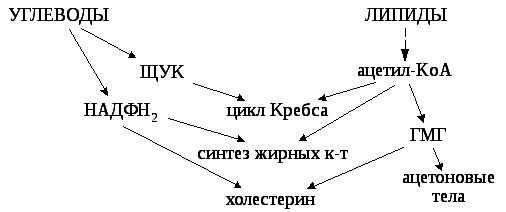
У детейуглеводы очень активно используются для синтеза липидов.
7.15.1. Ацетоновые тела
Распад липидов ведёт к образованию веществ, называемых ацетоновыми телами. К ацетоновым телам относятся:

Основная масса ацетоновых тел синтезируются в печени из ацетил — КоА через стадию гидроксиметилглютарил — КоА (ГМГ) по схеме:

В норме концентрация ацетоновых тел очень мала, составляя не более 0,6 ммоль/л. В физиологических условиях ацетоновые тела являются важным водорастворимым энергетическим материалом для различных тканей. Из печени они транспортируются в ткани, где активируются под действием НS-КоА или сукцинил-КоА (ацетоуксусная кислота +HS-КоА→ацетоацетил — КоА). Активная форма ацетоновых тел окисляется в цикле Кребса с образованием энергии (ацетоацетил — КоА→24 АТФ).
В патологических условиях при высокой концентрации ацетоновых тел развивается кетоацидоз. Основными причинами кетоацидоза являются длительное углеводное голодание и сахарный диабет.У детейвыражена склонность к кетоацидозу, поскольку у них ограничены запасы гликогена как энергетического материала. В детском возрасте выше скорость распада ТАГ, так как очень лябильна ТАГ-липаза. У детей активно протекает распад кетогенных аминокислот. В то же время усвоение ацетоновых тел в детском возрасте снижено.
7.16. Регуляция липидного обмена
На состояние липидного обмена влияют многие физиологические факторы, в том числе калорийность рациона, интенсивность физической нагрузки.
Нервная регуляция липидного обмена подтверждается тем, что жировая ткань богато иннервирована.
Эндокринная регуляция осуществляется гормонами гипофиза (липотропин, соматостатин), щитовидной железы (тироксин), надпочечников (адреналин, глюкокортикоиды), поджелудочной железы (инсулин, глюкагон), половых желез (андрогены и эстрогены).
Инсулин активирует синтез ТАГ из глюкозы (липогенез) за счёт активации фермента ацетил — КоА — карбоксилазы. Одновременно инсулин обладает антилиполитическим действием (тормозит липолиз) за счёт активирующего влияния на ключевой фермент — ТАГ — липазу.
Большинство других гормонов, участвующих в регуляции липидного обмена, угнетают липогенез, и в большей степени активирует липолиз. Так, гормоны адреналин и глюкагон активируют ТАГ — липазу, а глюкокортикоиды индуцируют синтез ТАГ — липазы.
В регуляции обмена холестерина участвует гормоны тироксин и эстрогены, которые снижают уровень холестерина в крови.
Существует авторегуляция отдельных звеньев липидного обмена. Например, синтез холестерина регулируется по принципу обратной связи (высокая концентрация холестерина в клетках угнетает фермент ГМГ — редуктазу и, тем самым, уменьшает его образование)
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
09.03.201623.62 Mб20Belov_Yu_V_Rukovodstvo_po_sosudistoy_khirurgii_s.djvu
- #
- #
- #
- #
- #
- #
- #
Источник
ХОЛЕСТЕРИНОВЫЙ ОБМЕН
ХОЛЕСТЕРИНОВЫЙ ОБМЕН (греческий chole желчь + stereos твердый) — совокупность реакций биосинтеза холестерина (см.) и его распада в организме человека и животных. В организме человека за сутки около 500 мг холестерина окисляется в желчные кислоты, примерно такое же количество стеринов экскретируется с фекалиями, около 100 мг выделяется с кожным салом, небольшое количество холестерина (около 40 мг) используется для образования кортикоидных и половых гормонов, а также витамина D3, 1-2 мг холестерина выводится с мочой. У кормящих женщин с грудным молоком выделяется 100- 200 мг холестерина в сутки. Эти потери восполняются за счет синтеза холестерина в организме (у взрослого человека в сутки около 700-1000 мг) и поступления его с пищей (300- 500 мг). Холестерин, а также часть холестерина, поступившего в просвет кишечника с желчью, всасывается в тонкой кишке в форме жировых мицелл (см. Жировой обмен). Эфиры холестерина предварительно гидролизуются при действии холестеринэстеразы (см.) панкреатического и кишечного соков. В стенке тонкой кишки холестерин используется для образования хиломикронов (см. Липопротеиды), в составе которых он поступает сначала в лимфатическую систему, а затем в кровяное русло.
В капиллярах жировой и некоторых других тканей в результате воздействия на хиломикроны липопротеид-липазы образуются частицы, обогащенные эфирами холестерина и фосфолипидами, получившие название ремнантных (остаточных) частиц. Эти частицы задерживаются в печени, где подвергаются распаду. Освободившийся при этом холестерин наряду с холестерином, синтезированным в печени, образует так называемый общий пул печеночного холестерина, который используется по мере необходимости для образования липопротеидов (см.).
Установлено, что у человека и некоторых животных липопротеиды низкой плотности транспортируют холестерин в органы и ткани, причем захват липоиротеидных частиц клетками этих органов и тканей осуществляется при участии специфических рецепторов. Холестерин, доставленный в клетку в составе липопротеидных частиц, идет на покрытие потребностей клетки (образование мембран при делении клетки, синтез стероидных гормонов и др.). Избыточная часть неэтерифицированного (свободного) холестерина превращается в его эфиры при действии содержащегося в клетке фермента — холестеролацилтрансферазы (КФ 2.3.1.26). Обратный транспорт неэтерифицированного холестерина из различных органов и тканей в печень осуществляется липопротеидами высокой плотности, причем в кровяном русле происходит этерификация захваченного холестерина при участии лецитина и фермента холестерин-лецитин — ацилтрансферазы (КФ 2.3.1.43). Доставленный таким путем в печень холестерин идет на образование желчных кислот (см.).
Синтез холестерина

Общая схема биосинтеза холестерина
Синтез холестерина осуществляется в клетках почти всех органов и тканей, однако в значительных количествах он образуется в печени (80%), стенке тонкой кишки (10%) и коже (5%). К. Блох, Ф. Линен и др. показали основные реакции биосинтеза холестерина (их не менее 30). Сложный процесс биосинтеза холестерина можно разделить на три стадии: 1) биосинтез мевалоновой кислоты; 2) образование сквалена из мевалоновой кислоты; 3) циклизация сквалена и образование холестерина (см. схему).
Считают, что главным источником образования мевалоновой кислоты в печени является ацетил-КоА, а в мышечной ткани — лейцин. И то и другое соединения в результате ряда энзиматических реакций образуют бета-гидрокси-бета-метилглутарил-КоА (ГМГ-КоА), который затем восстанавливается в мевалоновую кислоту. В последнее время показано, что в синтез мевалоновой кислоты в печени может включаться и малонил-КоА.
Реакцией, определяющей скорость биосинтеза холестерина в целом, является восстановление ГМГ-КоА в мевалоновую кислоту; этот процесс катализирует фермент НАДФ-Н2-зависимая ГМГ-КоА-редуктаза (КФ 1.1.1.34). Именно этот фермент подвержен воздействиям со стороны ряда факторов. Так, активность ГМГ-КоА-редуктазы повышается (или содержание ее в печени возрастает) и скорость синтеза холестерина в целом увеличивается при действии ионизирующего излучения, введении тиреоидных гормонов, поверхностно-активных веществ, холестирамина, а также при гипофизэктомии. Угнетение синтеза холестерина отмечается при голодании, тиреоидэктомии и при поступлении в организм пищевого холестерина. Последний угнетает активность (или синтез) фермента ГМГ-КоА-редуктазы.
Синтез холестерина в стенке тонкой кишки регулируется исключительно концентрацией желчных кислот. Так, отсутствие их в кишечнике при наличии наружного желчного свища ведет к повышению синтеза холестерина в тонкой кишке в 5-10 раз.
На второй стадии синтеза происходит фосфорилирование мевалоновой кислоты при участии АТФ и образование нескольких фосфорилированные промежуточных продуктов (см. Фосфорилирование). При декарбоксилировании одного из них образуется изопентенил-пирофосфат, часть которого превращается в диметилаллил-пирофосфат. Взаимодействие этих двух соединений приводит к образованию димера — геранил-пирофосфата, содержащего 10 атомов углерода. Геранил-пирофосфат конденсируется с новой молекулой изопентенил-пирофосфата и образует тример — фарнезил-пирофосфат, содержащий 15 атомов углерода. Эта реакция идет с отщеплением молекулы пирофосфата. Затем две молекулы фарнезил-пирофосфата конденсируются, теряя каждая свой пирофосфат, и образуют гексамер сквален, содержащий 30 атомов углерода.
Третья стадия синтеза включает окислительную циклизацию сквалена, сопровождающуюся миграцией двойных связей и образованием первого циклического соединения — ланостерина. Ланостерин уже имеет гидроксильную группу в положении 3 и три лишние (по сравнению с холестерином) метильные группы. Дальнейшее превращение ланосте-рина может совершаться двумя путями, причем и в том и в другом случае промежуточными продуктами являются соединения стериновой природы. Более доказанным считается путь через 24, 25-дигидроланостерин и ряд других стеринов, включая 7-дигидрохолестерин, служащий непосредственным предшественником холестерина. Другой возможный путь — превращение ланостерина в зимостерин, а затем в десмостерин, из которого при восстановлении образуется холестерин.
Если суммировать общий итог всех реакций биосинтеза холестерина, то он может быть представлен в следующем виде:
18CH3CO-S-KoA + 10(H+) + 1/2O2 -> C27H46O + 9CO2 + 18KoA-SH. Источником углерода холестерина является ацетил-КоА (им может быть также малонил-КоА и лейцин), источником водорода — вода и никотин-амида дениндинуклеотидфосфат, а источником кислорода — молекулярный кислород.
Начиная со сквалена и кончая холестерином все промежуточные продукты биосинтеза нерастворимы в водной среде, поэтому они участвуют в конечных реакциях биосинтеза холестерина в связанном со сквален или стеринпереносящими белками состоянии. Это позволяет им растворяться в цитоплазме клетки и создает условия для протекания соответствующих реакций. Холестерин-переносящий белок обеспечивает также перемещение стеринов внутри клетки, что имеет важное значение для вхождения его в мембрану клетки, а также для транспорта в клеточные системы, осуществляющие катаболизм холестерина.
Катаболизм холестерина протекает в печени (окисление его в желчные кислоты), в надпочечниках и плаценте (образование из холестерина стероидных гормонов), в тестикулярной ткани и яичниках (образование половых гормонов). При биосинтезе холестерина в коже на завершающей стадии образуется небольшое количество 7-дегидрохолестерина. Под влиянием УФ-лучей он превращается в витамин D3.
Своеобразные превращения претерпевает холестерин в толстой кишке. Речь идет о той части пищевого холестерина или холестерина, поступившего в кишечник с желчью, которая не подверглась всасыванию. Под влиянием микробной флоры толстой кишки происходит восстановление холестерина и образование так наз. нейтральных стеринов. Главным их представителем является копростерин. Экспериментальные исследования, проведенные с использованием радиоизотопных и других методов, показали, что скорость обновления холестерина в различных органах и тканях неодинакова; наиболее высока она в надпочечниках и печени и чрезвычайно низка в мозге взрослых животных.
Патология холестеринового обмена
Нарушения холестеринового обмена обычно связаны с дисбалансом между количеством синтезируемого в организме и поступающего с пищей холестерина, с одной стороны, и количеством холестерина, подвергающегося катаболизму,- с другой. Эти нарушения проявляются в изменении уровня холестерина в плазме крови, которые классифицируются как гиперхолестеринемия или гипохолестеринемия (для взрослого населения высокоразвитых стран величины выше 270 мг/100 мл и ниже 150 мг/100 мл соответственно).
Гиперхолестеринемия может быть первичной (наследственной или алиментарной) и вторичной, обусловленной различными заболеваниями. Наследственная (семейная) гиперхолестеринемия характеризуется высоким уровнем холестерина и липопротеидов низкой плотности (ЛПНГЛ в плазме крови. При гомозиготной гиперхолестеринемии уровень холестеринемии может достигать 700- 800 мг/100 мл, а при гетерозиготной — 300-500 мг/100 мл. В основе наследственной гиперхолестеринемии лежит генетически обусловленное отсутствие (у гомозигот) или недостаток (у гетерозигот) специфических рецепторов к липопротеидам низкой плотности у клеток, вследствие чего резко снижается захват и последующий катаболизм этих богатых холестерином липопротеидов клетками паренхиматозных органов и тканей. В результате пониженного захвата и снижения катаболизма липопротеидов низкой плотности развивается гиперхолестеринемия (см.). Последняя приводит к раннему развитию атеросклероза (см.) и его клинических проявлений — ишемической болезни сердца (см.), преходящей ишемии мозга (см. Инсульт) и др. Особенно тяжело протекает атеросклероз при гомозиготной форме; у таких больных часто наблюдается ксантоматоз (см.), липоидная дуга роговицы (отложение холестерина в роговицу глаз), инфаркт миокарда в юношеском возрасте.
Распространенность гомозиготной формы гиперхолестеринемии невелика (примерно один случай на 1 млн. жителей). Чаще встречается гетерозиготная форма — один случай на 500 жителей.
Алиментарная гиперхолестеринемия характеризуется повышенным уровнем холестерина в плазме крови вследствие длительного потребления больших количеств пищи, богатой холестерином (куриные желтки, икра, печень, животные жиры и др.). Алиментарная гиперхолестеринемия той или иной степени выраженности характерна для жителей высокоразвитых индустриальных стран. Согласно популяционным исследованиям имеется прямая зависимость между уровнем холестерина в крови и распространенностью ишемической болезни сердца.
В эксперименте на различных животных (кролики, морские свинки, обезьяны) показано, что введение массивных доз холестерина с пищей приводит к резко выраженной гиперхолестеринемии и быстрому развитию атеросклероза. Экспериментальные модели гиперхолестеринемии и атеросклероза, впервые предложенные H. Н. Аничковым и С. С. Халатовым (1913), широко используются в научных исследованиях.
Вторичная гиперхолестеринемия встречается при гипотиреозе (см.), сахарном диабете (см. Диабет сахарный), нефротическом синдроме (см.), подагре (см.) и др. и нередко сопровождается развитием атеросклероза (см. Гиперхолестеринемия).
Выделяют первичную и вторичную гипохолестеринемию. Первичная гипохолестеринемия характерна для наследственного заболевания — абеталипопротеинемии (см.). При этой болезни отмечается почти полное отсутствие в плазме крови липопротеидов низкой плотности (у гомозигот) или значительное их снижение (у гетерозигот). Уровень общего холестерина не превышает 75 мг/ 100 мл. Гомозиготная форма болезни протекает исключительно тяжело. В основе абеталипопротеинемии лежит генетически обусловленное нарушение синтеза апопротеина В — главного белка липопротеидов низкой плотности.
Вторичные гипохолестеринемии наблюдаются при кахексии, гипертиреоидизме, аддисоновой болезни и паренхиматозных заболеваниях печени, при ряде инфекционных болезней и интоксикациях (см. Гипохолестеринемия). При недостаточной активности в плазме крови фермента лецитин — холестерин -ацилтрансферазы, или ЛХАТ (наследственная ЛXАТ-недостаточность), ответственного за этерификацию холестерина плазмы, наблюдается накопление неэтерифицированного холестерина в мембранах эритроцитов и клетках почек, печени, селезенки, костного мозга, роговицы глаза. Резко снижается доля этерифицированного холестерина в плазме крови и одновременно повышается уровень неэтерифицированного холестерина и лецитина. У больных с наследственной ЛXAT-недостаточностыо стенки артерий и капилляров подвержены деструктивным изменениям, что связано с отложением в них липидов. Наиболее тяжелые изменения происходят в сосудах почечных клубочков, что приводит к развитию почечной недостаточности (см.).
Одним из распространенных нарушений холестериновый обмен. является образование желчных камней, основной составной частью которых является холестерин (см. Желчнокаменная болезнь). Образование желчных камней происходит вследствие выкристаллизовывания холестерина при относительно высокой его концентрации в желчи и относительно низкой концентрации в ней желчных кислот и фосфолипидов, обладающих способностью растворять холестерин. Исследования показали, что имеется прямая связь между уровнем холестерина в плазме крови и распространенностью холестероза (см.) и желчнокаменной болезни.
Библиогр.: Климов А. Н, и Н икульчева Н. Г. Липопротеиды, дислипопротеидемии и атеросклероз, Л., 1984; Полякова Э. Д. Пути биосинтеза холестерина в печени и их регуляция, в кн.: Липиды, структура,биосинтез, превращения и функции, под ред. С. Е. Северина, с. 131, М., 1977;она же, Регуляция содержания холестерина в клетке, в кн.: Биохимия липидов и их роль в обмене веществ, под ред.С. Е. Северина, с. 120, М., 1981; Финагин Л. К. Обмен холестерина и его регуляция, Киев, 1980; Lipids and lipidoses, ed. by G. Schettler, B.- Heidelberg, 1967; Sodhi H. S., Kudchod-k a r B. J. a. Mason D. T. Clinical methods in study of cholesterol bolism, Basel a. o., 1979.
A. H. Климов
Источник
7.14. Обмен холестерина
Ежесуточно в организме взрослого человека обменивается до 1,5 г холестерина. Примерно половина этого количества синтезируется в организме (эндогенный холестерин), а половина поступает с пищей (экзогенный холестерин). Холестерин пищевых продуктов всасывается в тонком кишечнике при участии жёлчных кислот.
7.14.1. Биосинтез холестерина
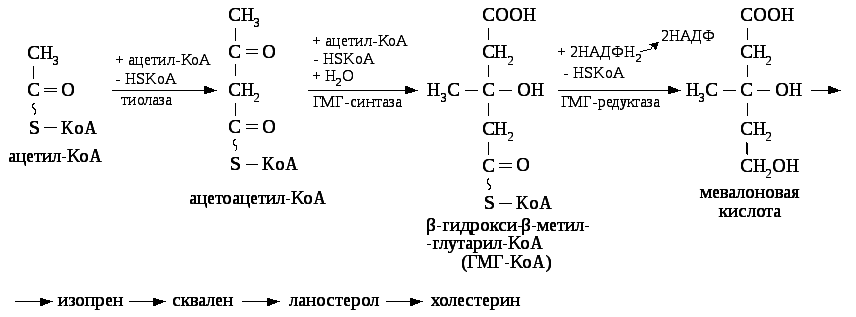
Синтез холестерина происходит в печени из ацетил-КоА. Синтез холестерина представляет собой сложный многоэтапный процесс, протекающий в 20 стадий. Начальная стадия — образование мевалоновой кислоты является ключевой
ГМГ — редуктаза — ключевой фермент синтеза холестерина, она угнетается высокими концентрациями холестерина. Синтезированный в печени холестерин включается в состав липопротеидов ЛПОНП. Под действием липопротеидной липазы ЛПОНП переходят в ЛПНП, которые транспортируют холестерин от печени к органам и тканям. В тканях имеются рецепторы к липопротеидам, при участии которых происходит захват холестерина и проникновение его в клетки.
В клетках часть холестерина превращается в эфиры при участии фермента АХАТ (ацилхолестеролацилтрансфераза). Эфиры холестерина депонируются в тканях.
7.14.2. Использование холестерина в тканях
Холестерин необходим для всех клеток и тканей.
1. В печени примерно половина синтезирующегося холестерина превращается в жёлчные кислоты при участии ключевого фермента 7-α-гидроксилазы. Применение веществ, адсорбирующих жёлчные кислоты в кишечнике, повышает переход холестерина в жёлчные кислоты и снижает его уровень в крови.
2. Холестерин используется для построения клеточных мембран, где он составляет примерно треть всех липидов мембран и определяет физико-химические свойства липидной фазы мембран.
3. В надпочечниках, половых железах холестерин используется на синтез стероидных гормонов
4. В коже из производного холестерина происходит образование витамина Д3(холекальциферола).
7.14.3. Выведение холестерина из организма
Избыток холестерина удаляется из тканей при участии ЛПВП, которые адсорбируют холестерин из клеток и переносят его в печень. Основная часть холестерина выводится из организма через кишечник в виде жёлчных кислот, продуктов их обмена и образующихся из холестерина под действием микрофлоры холестанола и копростанола. Выведение холестерина из организма в небольших количествах происходит со слущивающимся эпителием, с мочой в виде соединений стероидных гормонов с глюкуроновой кислотой.
7.14.4. Нарушение обмена холестерина
В норме концентрация холестерина в крови взрослых людей составляет 3,5 — 5,2 ммоль/л. У детейконцентрация холестерина в крови ниже, чем у взрослых. У новорожденных уровень холестерина равен 2,67 ммоль/л, у детей в возрасте одного года — 4,03 ммоль/л.
Симптом повышения уровня холестерина в крови называется гиперхолестеринемией. Врождённые гиперхолестеринемии встречаются редко, чаще развиваются приобретённые (вторичные) гиперхолестеринемии. На фоне гиперхолестеринемии возможно развитие таких заболеваний как атеросклероз и жёлчекаменная болезнь.
При атеросклерозеизбыток холестерина откладывается в эндотелии сосудов, что ведёт к развитию асептического воспаления, отложению кальция, вследствие чего нарушается кровоснабжение тканей. Для диагностики атеросклероза рекомендуется определение коэффициента атерогенности, который показывают соотношение между ЛПНП и ЛПВП.
К атерогенности = (Хобщ. — ХЛПВП)/ХЛПВП≤ 3.
Для лечения атеросклероза применяют ингибиторы ГМГ-редуктазы, которые блокируют синтез холестерина.
Жёлчекаменная болезнь связана с нарушением соотношения между водонерастворимым холестерином и гидрофильными фосфолипидами и жёлчными кислотами в составе жёлчи. Холестерин является основой формирования камней в жёлчных путях.
При циррозах печени, гепатитах возможно развитие гипохолестеринемии.
Источник