Повышение гемоглобина при почечной недостаточности
Tweets
/ / ()
|
2-11-2018, 14:59
|
 () , , . « » XX XXI « ».
() , , . « » XX XXI « ».
– (, ) () ( « ()»). ( 1).
(), | ||
I | , | > 90 |
II | , | 60-89 |
IIIA | 45-59 | |
III | 30-44 | |
IV | 15-29 | |
V | < 15 |
III-V , < 60 /), « ». V – – .
, :
: , , .
, – , (). (Richard Bright) . .
– . , 36 /, , , 30%.
, , , (). , , , . , .
() , . , .
. :
- —
- ( )
, — ( ), — .
, ( ) – . – , — ( ).
1/3-1/2 — , . , ( 5-6 , 2 ). . B9 ( ) ( — — ). . , .
(), , . , . ( 55-120 /; – 17-35%). , () ( 1).
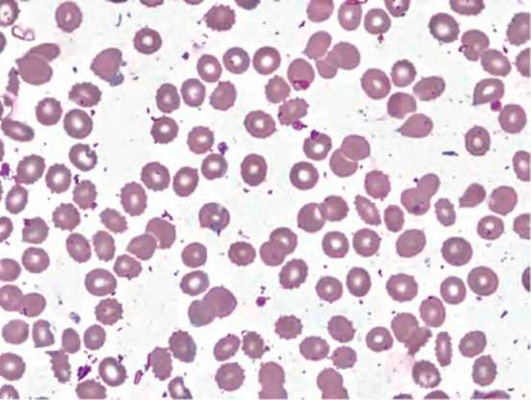
1. . . (. -, . ×100)
, . , , . , 40-105 / . , , , . , .
—
Kidney Disease: Improving Global Outcomes (KDIGO) 2012 , — (), . .
, «» 15 , (Hb) < 130 / < 120 / . 6 5 «» < 110 /; 5 12 – Hb < 115 /; 12 15 – Hb < 120 /. , , :
- III – 1
- IV-V – 2 (1 6 )
- V , ( ) – 1 3 .
, -, :
- III-V – 1 3
- V – 1
— . . < 30 / . , .
KDIGO (2012 ) , -, ( – 1-3- ).
, — , ( – 1-3- ), -, ( ) < 30% < 500 / (/).
, , :
- /
, , (, , ), , — ( -), . , .
– — , ( ).
— : , . , . , ( , , , ). — .
– . ( — 2-3 1000 ), (, ) . , , , , . — , .
:
- , B9 B12
— . ( ), < 80 / -. 80-100 / ( «. . »), , -. ( ) -.
— () – . — – (-; : , , ). — , , , ( 1000 , 2000 , 2500 , 3000 , 4000 , 5000 , 10 000 , 20 000 , 40 000 ). , , .
, . — – — (). — 1 2-4 ( III-IV , , ).
() 20 / 3 . ( 0,62 / (1 /) 4 ), 40 / 3 4 . 25% 1 . – 40 / 3 . 80 / 3 4 . 25% 1 . , – 700 /.
-, , :
- – 4
(-, , ) 100-200 / ( 2-3 ) . 100 / / , 1000-2000 /, , 1,5-2 , 1/2 ( ) 5 8 . , 5 , ( , ).
— 33-36% — 75 / / 3 . 150 / / 3 . ( ) .
, – — 75-100 / / 3 /. 2-6 , , 1-2% . 2% , 25%. – , 25%. 1 4 , . ( ), , 10-12- — .
( ) , , . , — , . , . — , .
, , ; – . 2 12 . – 25 50 /. 1 4 – 100-120 /. 105 /. — 11,7 .
, — , , , . , , — , ( ), —. :
- 40 /
- < 10 000/
KDIGO , « , » -. . , 37 , — ( ), , 29 (78%), , (), 8 , , . — . , , () – , .
, ( ), . 100-115 /, – 30-33%. . , , .
. .
-, 130 /. — – ( «. . »), — , , . – 10 / .
III-IV — — . , — III-IV , , . , III-IV ( ), -:
- ( — )
- ( )
- ( B9) ( B12)
, ( ).
— :
- ( )
.
, , 20-50 / 3 . , 4 , 4 , .
— () , 0,45 / 1 ; 0,75 / 1 2 . 10 / 2 , — 25%. -, .
III-IV . ; 1 2-3 – ; 1 3-6 – , , , . 35%, , 40; — 38%, 2/3-3/4 . — , 30-35% ( 25-200 /), 1 4-6 .
— – . 23% . , — ( ). , , , , — , NO- . , ( , β-, ). , , ( , ) ( ).
Источник
Методы коррекции анемии у больных с хронической почечной недостаточностью
Хроническая почечная недостаточность (ХПН) является одной из актуальных проблем не только нефрологии, но и многих смежных специальностей, учитывая рост числа больных c этой патологией во всем мире. Основной задачей врача при лечении ХПН является улучшение качества жизни и прогноза у данной категории больных. Несмотря на все более широкое распространение методов заместительной почечной терапии, таких как гемодиализ и трансплантация почки, что способствует увеличению продолжительности жизни пациентов с ХПН, летальность больных остается высокой, а качество жизни хуже, чем у людей, не страдающих этой патологией. При этом распространенность именно терминальной стадии почечной недостаточности, со скоростью клубочковой фильтрации (СКФ) <15 мл/мин., в России неуклонно растет.
Наиболее частым спутником ХПН является анемия, которая в большинстве случаев появляется у больных при уменьшении СКФ ниже 50 мл/мин./1,73 м2, однако у 25% больных анемия отмечается при СКФ >50 мл/мин./ 1,73 м2 [1]. Основной причиной развития анемии при ХПН является снижение синтеза гормона роста эритроцитов эритропоэтина в перитубулярных клетках проксимальной части нефрона при сморщивании почек, в результате чего уровень плазменного эритропоэтина становится относительно низким.
В меньшем объеме на развитие анемии оказывает влияние укорочение жизни эритроцитов. При нормальных физиологических условиях в костном мозге до полноценных эритроцитов, выходящих в кровяное русло, доживают 95% клеток, что называется эффективным эритропоэзом. При ХПН эритроидные клетки в большей степени разрушаются в костном мозге или выходят в кровоток, не достигнув полного созревания, что было охарактеризовано как неэффективный эритропоэз. Также определенное влияние оказывает тромбоцитарная дисфункция, обусловливающая кровоточивость, действие уремических токсинов на эритроциты, снижение уровня железа из–за неадекватного всасывания в кишечнике и гемодиализных кровопотерь и удаление при гемодиализе фолиевой кислоты [2]. В норме секреция эритропоэтина и эритропоэз находятся в сбалансированном состоянии, поддерживающем равенство между продукцией и гибелью эритроцитов.
Анемия при ХПН в большинстве случаев нормоцитарная и нормохромная, а при развитии недостаточности железа — гипохромная. При патологии почек обратная линейная зависимость между уровнем плазменного эритропоэтина и концентрацией гемоглобина отсутствует, в результате чего синтез эритропоэтина не увеличивается пропорционально тяжести анемии. Это приводит к развитию неэффективного эритропоэза, сопровождающегося внутрикостномозговым гемолизом и сокращением средней продолжительности жизни эритроцитов [3]. Эритропоэтиндефицитная анемия свойственна больным с ХПН, находящимся на диализе, при этом после аллотрансплантации почки анемия встречается редко.
Также значительный вклад в течение ХПН у больных с анемией вносит сопутствующее поражение сердечно–сосудистой системы, что нередко развивается у молодых и в тяжелых случаях приводит к фатальному исходу. Возникающая на фоне анемии гипоксия приводит к дилатации периферических сосудов и уменьшению сосудистой сопротивляемости, что, в свою очередь, ведет к снижению уровня артериального давления (АД). Для поддержания нормального АД включаются механизмы вазоконстрикции периферических сосудов, увеличения частоты сокращений сердца и ударного объема на фоне повышения активности симпатической нервной системы. При этом задействованы другие механизмы повышенной активности симпатической нервной системы: вазоконстрикция почечных сосудов, приводящая к замедлению кровотока в почках, уменьшению скорости клубочковой фильтрации, ишемии почек. Замедление кровотока в почках активирует ренин–ангиотензин–альдостероновую систему и выделение антидиуретического гормона.
Все это вызывает задержку жидкости в организме, увеличение объема плазмы, гипертрофию миокарда левого желудочка (ГЛЖ) и дальнейшее повышение нагрузки на уже пораженное сердце [4]. Гипертрофия миокарда левого желудочка обнаруживается у 45–55% больных, находящихся на гемодиализе. При далеко зашедшей ГЛЖ летальность увеличивается в 4 раза, риск острого инфаркта миокарда – в 3–6 раз, риск развития острой левожелудочковой недостаточности и тяжелых нарушений ритма – в 4 раза [5–8]. ГЛЖ приводит к некрозу и апоптозу кардиомиоцитов и снижению фракции выброса левого желудочка, что является причиной возникновения застойной сердечной недостаточности. Ренин, ангиотензин и альдостерон, выделяемые в повышенных количествах, оказывают прямое повреждающее действие на кардиомиоциты, усугубляя существующее поражение [9,10].
Взаимосвязь между ХПН, анемией и заболеванием сердца была доказана в нескольких крупных исследованиях [11], вот почему необходимы своевременное определение степени поражения сердечно–сосудистой системы и назначение соответствующей терапии этой категории больных.
Особенно важным является тот факт, что длительность и степень выраженности анемии при ХПН во многом определяют клиническое состояние пациента. Так, была показана взаимосвязь между тяжестью астенического синдрома, степенью переносимости физической нагрузки, снижением эффективности умственной деятельности, чувствительности к инфекциям и увеличением опасности постгемотрансфузионного гемохроматоза у больных с анемией [5,12]. Также появились доказательства того, что ранняя коррекция анемии препаратами улучшает качество жизни и снижает риск смерти от сердечно–сосудистых осложнений у больных при последующем лечении программным гемодиализом [1,2,13].
Как и в общетерапевтической практике, основным диагностическим критерием развития анемии при ХПН является снижение концентрации гемоглобина менее 95% от уровня у здоровых лиц. При этом показатель гемоглобина необходимо соотносить с возрастом и полом пациента. Так, диагностически значимым считается снижение уровня гемоглобина менее 11,5 г/дл для взрослых женщин, менее 13,5 г/дл – для взрослых мужчин и менее 12,0 г/дл – для мужчин старше 70 лет [1,2]. Что же касается необходимости в определении уровня эритропоэтина, то она возникает крайне редко, например, при верификации нефрогенной анемии, в случае, когда концентрация гемоглобина снижена, а функция почек изменена незначительно (СКФ 60–120 мл/мин.).
При ХПН и анемии снижение уровня гемоглобина всего лишь на 1 г/дл повышает летальность почти на 20%, что в большей степени связано с сердечно–сосудистыми и инфекционными осложнениями, и существенно снижает качество жизни больных. Вот почему крайне важна своевременная коррекция анемии у больных с ХПН. К сожалению, в настоящее время менее 25% этой категории больных получают антианемическую терапию [1], при этом лечение, как правило, начинают поздно – при среднем уровне гемоглобина 9 г/дл [12].
Наиболее значительный шаг в лечении анемии при ХПН был сделан еще в 1985 г. Тогда было проведено первое успешное клиническое испытание препарата рекомбинантного человеческого эритропоэтина. В дальнейшем было неоднократно показано, что фармакологическая коррекция дефицита эритропоэтина при ХПН (заместительная гормональная терапия) обеспечивает адекватную стимуляцию костного мозга и прекращает неэффективный эритропоэз. Эритропоэтин стимулирует рост стволовых эритроидных предшественников, которые называют колониеобразующими единицами эритропоэза.
Препараты эритропоэтина – это высокоочищенные гликопротеиды с молекулярной массой около 30 кДа, состоят из полипептидных цепей и карбогидратной части, на концах которой расположены сиаловые группы, предотвращающие инактивацию гормона. В зависимости от типов продуцентов и генов выделяют эпоэтины αβωδ:
− ЕРО α и β синтезированы в культурах клеток яичников китайского хомячка (СНО). Если в технологии получения используется природный экспрессируемый ген, то синтезируется эпоэтин α, если копийный ген – эпоэтин β. В России зарегистрированы следующие препраты: Эральфон, Эпокрин, Эпрекс, Аэприн (эпоэтин альфа); Рекормон, Эпостим, Эритростим, Веро-Эпоэтин (эпоэтин бета);
− ЕРО ω синтезируется в культуре клеток почки детеныша хомячка (BHK). Имеют более высокий уровень гликозилирования;
− ЕРО δ синтезирован в культурах клеток человеческой фибросаркомы (линия РТ–1080). Он называется генно-активированным ЕРО, т.к. экспрессия человеческого гена ЕРО активирована цитомегаловирусом. В отличие от ЕРО альфа и бета он не содержит N–гликолилнейраминовую кислоту (Neu5Cc).
Эти препараты разносторонне стимулируют пролиферацию эритроидных клеток, их созревание, скорость синтеза глобина, порфиринов, а также влияют на утилизацию железа, скорость выхода ретикулоцитов из костного мозга в кровь и превращение их в зрелые эритроциты [7,8].
В России препараты эритропоэтина используются с 1989 г., среди них особый интерес представляет стимулятор гемопоэза рекомбинантного человеческого эритропоэтина препарат Эральфон® (эпоэтин альфа), выпускаемый фармацевтической компанией «Сотекс». Препарат выпускается в виде раствора для внутривенного и подкожного введения в шприцах от 0,3 до 1,0 мл. В шприце содержится от 1000 до 40 000 МЕ активного вещества – эпоэтина альфа.
Эральфон® – это гликопротеид, специфически стимулирующий эритропоэз, активирует цитоз и созревание эритроцитов из клеток–предшественников эритроцитарного ряда. Как уже было сказано ранее, рекомбинантный эпоэтин альфа синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий человеческий эритропоэтин. По своему составу, биологическим и иммунологическим свойствам эпоэтин альфа идентичен природному эритропоэтину человека. Введение эпоэтина альфа в организм человека приводит к повышению уровней гемоглобина и гематокрита, улучшению кровоснабжения тканей и работы сердца. Наиболее выраженный эффект от применения эпоэтина альфа наблюдается при анемиях именно у больных ХПН.
Что же касается оптимального способа введения препарата Эральфон® при ХПН, то в рандомизированных исследованиях пациентов, получавших гемодиализ, было показано, что эпоэтин, введенный подкожно, не уступает по эффективности внутривенно введенному препарату, но при этом можно снизить дозировку эпоэтина, что существенно уменьшает стоимость лечения [1,2,7]. Также было отмечено, что эффективная доза эпоэтина альфа, назначаемого подкожно, на 22% меньше дозы, необходимой для внутривенного введения. При подкожном способе введения эпоэтин альфа имеет меньшую биодоступность и наибольший период полувыведения по сравнению с внутривенным путем введения [1].
Лечение анемии с использованием препаратов эритропоэтина должно состоять из двух этапов: начального, заключающегося в коррекции имеющейся анемии, и этапа поддерживающей терапии. В большинстве случаев эпоэтин альфа Эральфон® назначают 2–3 раза в неделю, учитывая продолжительность периода полувыведения этого препарата [1,2]. По результатам проведенного мета–анализа рандомизированных исследований существенной разницы между введением эпоэтина у пациентов на гемодиализе с одно–, двух– и трехкратным интервалом в неделю выявлено не было [14]. Подкожное введение эпоэтина рекомендовано как пациентам с додиализными стадиями ХПН и больным на программном гемодиализе, так и пациентам, перенесшим трансплантацию почки [1,2]. При этом больным на программном гемодиализе Эральфон® назначается как подкожно (60 МЕ/кг/нед.), так и внутривенно (100 МЕ/кг/нед).
По данным некоторых исследований, эпоэтин способен эффективно купировать анемический синдром при его назначении подкожно в дозе 20 МЕ/кг 3 раза/нед. в фазу коррекции и 40 МЕ/кг 1 раз/нед. в фазу поддерживающей терапии. Скорость повышения концентрации гемоглобина на начальном этапе терапии должна составлять 1–2 г/дл в месяц. При скорости повышения концентрации гемоглобина >2 г/дл в месяц возникает необходимость в снижении общей недельной дозы препарата на 25–50% либо его временной отмены. На этапе коррекции уровень гемоглобина необходимо определять каждые 2–4 нед., а при поддерживающей терапии и стабилизации уровня гемоглобина концентрация его должна определяться каждые 1–2 мес. [1,2].
Также не стоит забывать о необходимости коррекции недостатка железа при анемии у больных с ХПН. Железосодержащие препараты и препараты эпоэтина взаимодействуют как синергисты. Препараты эпоэтина стимулируют синтез примерно 2 млн новых эритроцитов в секунду [14], при недостатке доступного железа из костного мозга в кровь поступают ретикулоциты с пониженным содержанием гемоглобина [12]. В свою очередь, наличие адекватного количества доступного железа стимулирует эритропоэз и сокращает потребность в эпоэтине [5].
Помимо использования препарата Эральфон® для лечения анемии при ХПН его применение показано для профилактики и лечения анемий у больных с солидными опухолями; с анемией и вирусом иммунодефицита человека, вызванных применением зидовудина, при уровне эндогенного эритропоэтина менее 500 МЕ/мл; для профилактики и лечения анемий у больных с миеломной болезнью, неходжскинскими лимфомами низкой степени злокачественности, хроническим лимфолейкозом, ревматоидным артритом; для лечения анемии у недоношенных детей, родившихся с низкой массой тела (до 1,5 кг); в качестве подготовительной программы перед обширным хирургическим вмешательством у больных с уровнем гематокрита, равным 33–39% [15].
При применении препарата Эральфон® следует помнить о возможности возникновения лекарственных взаимодействий. Так, Эральфон® снижает концентрацию циклоспорина из–за увеличения степени связывания его с эритроцитами, что может привести к необходимости коррекции дозы циклоспорина. Также препарат фармацевтически несовместим с растворами других лекарственных средств.
Во время лечения рекомбинантными человеческими эритропоэтинами необходимо контролировать уровень АД и количество тромбоцитов, уровень гематокрита и ферритина. У больных с контролируемой артериальной гипертензией или тромботическими осложнениями в анамнезе может потребоваться повышение дозы гипотензивных препаратов и/или антикоагулянтов. При наличии факторов риска систолической артериальной гипертензии дозу эпоэтина следует повышать не чаще 1 раза в месяц и не более чем на 20 ЕД/кг массы тела, чтобы ежемесячный прирост гемоглобина был ниже 1 г/дл (соответственно прирост гематокрита – не более 0,5%).
При назначении пациентам с печеночной недостаточностью возможны замедление метаболизма эпоэтина альфа и выраженное усиление эритропоэза. Перед проведением планового хирургического вмешательства пациенты, находящиеся на терапии эпоэтином альфа, должны получать адекватную профилактическую антитромбоцитарную терапию. В очень редких случаях при длительном применении эритропоэтина для терапии анемических состояний может наблюдаться образование нейтрализующих антител к эритропоэтину [15].
Таким образом, препарат Эральфон®, применяемый для патогенетической терапии анемии у больных с ХПН, увеличивает выживаемость и повышает качество жизни больных, обладая при этом необходимой безопасностью и эффективностью.
Литература
1. Revised European Best Practice Guidelines for the Management of anemia in Patients with Cronic Renal Failure. // Nephrol. Dial. Transplant. 2004; 19; 2: 2–45.
2. Российские национальные рекомендации по диагностике и лечению анемии при хронической болезни почек. // Анемия. – 2006. – № 3.
3. Hsu C.Y., McCulloch C.E., Curhan G.C. et al. Epidemiology of anemia associated with chronic renal insufficiency among adults in the United States: results from the Third National Health and Nutrition Examination Survey. // J. Am. Soc. Nephrol. 2002; 13: 504–510.
4. Anand I.S., Chandrashekhar Y., Ferran R., Poole–Wilson P.A., Hams P.C. Pathogenesis of oedema in chronic severe anaemia – studies of body water and sodium, renal function, haemodynamic variables, and plasma hormones. // Br Hear. J. 1993; 70: 357–362.
5. Hue J.L., St Peter W.R., Ebben J.P. et al. Anemia treatment in the pre–ESRD period and associated mortality in elderly patients. // Am. J. Kidney Dis. 2002; 40: 1153–1161.
6. Волгина Г.В., Перепеченных Ю.В., Бикбов Б.Т. и др. Факторы риска кардиоваскулярных заболеваний у больных с хронической почечной недостаточностью. // Нефрология и диализ. – 2000. – № 2, 4. – С. 252–259.
7. NKF–K/DOQI Clinical Practice Guidelines for Anemia of Chronic Kidney Disease: update 2000. // Am. J. Kidney Dis. 2001; 37 [Suppl. 1]: s182–s238.
8. Weiss G., Goodnough L.T. Anemia of Chronic Disease. // N. Engl. J. Med. 2005; 352: 1011–23.
9. Katz A.M. The cardiomyopathy of overload: an unnatural growth response in the hypertrophied heart. // Ann Intern Med 1994; 121: 363–371.
10. Johnson D.B., Dell’ltalia 1J. Cardiac hypertrophy and failure in hyperlension. Curr Opin Nephrol Hypertens 1996; 5: 186–191.
11. Foley R.N. Parfrey P.S, Harnett J.D et al. Clinical and echocardiographic disease in patients starting end–stage renal disease therapy Kidney Int 1995; 47: 186–192.
12. Cody J., Daly C., Campbell M. et al. Recombinant human erythropoieetin for chronic renal failure anemia in pre–dialysis patients (Cochrane Review). In: The Cochrane Library. Issue 3, 2003. Update Software, Oxford.
13. Милованова Л.Ю., Николаев А.Ю., Козлова Т.А. и др. Прогностическое значение ранней коррекции анемии у больных хронической почечной недостаточностью. // Нефрол. и диал. – 2004. – № 1. – С. 54–57.
14. Horl W.H., Macdougall I.C., Rossert J., et al. Predialysis survey on anemia management: patient referrral. // Am. J. Kidney Dis. 2003; 41: 49–61.
15. Ершова А.К. Этиология, патогенез и лечение железодефицитной анемии. // РМЖ. Клинические рекомендации и алгоритмы для практикующих врачей. – Т. 19. № 12. С. 790–794.
Источник