Превращение холестерина в желчные кислоты
Содержание статьи
ХОЛЕСТЕРИНОВЫЙ ОБМЕН — Большая Медицинская Энциклопедия
ХОЛЕСТЕРИНОВЫЙ ОБМЕН (греческий chole желчь + stereos твердый) — совокупность реакций биосинтеза холестерина (см.) и его распада в организме человека и животных. В организме человека за сутки около 500 мг холестерина окисляется в желчные кислоты, примерно такое же количество стеринов экскретируется с фекалиями, около 100 мг выделяется с кожным салом, небольшое количество холестерина (около 40 мг) используется для образования кортикоидных и половых гормонов, а также витамина D3, 1—2 мг холестерина выводится с мочой. У кормящих женщин с грудным молоком выделяется 100— 200 мг холестерина в сутки. Эти потери восполняются за счет синтеза холестерина в организме (у взрослого человека в сутки около 700—1000 мг) и поступления его с пищей (300— 500 мг). Холестерин, а также часть холестерина, поступившего в просвет кишечника с желчью, всасывается в тонкой кишке в форме жировых мицелл (см. Жировой обмен). Эфиры холестерина предварительно гидролизуются при действии холестеринэстеразы (см.) панкреатического и кишечного соков. В стенке тонкой кишки холестерин используется для образования хиломикронов (см. Липопротеиды), в составе которых он поступает сначала в лимфатическую систему, а затем в кровяное русло.
В капиллярах жировой и некоторых других тканей в результате воздействия на хиломикроны липопротеид-липазы образуются частицы, обогащенные эфирами холестерина и фосфолипидами, получившие название ремнантных (остаточных) частиц. Эти частицы задерживаются в печени, где подвергаются распаду. Освободившийся при этом холестерин наряду с холестерином, синтезированным в печени, образует так называемый общий пул печеночного холестерина, который используется по мере необходимости для образования липопротеидов (см.).
Установлено, что у человека и некоторых животных липопротеиды низкой плотности транспортируют холестерин в органы и ткани, причем захват липоиротеидных частиц клетками этих органов и тканей осуществляется при участии специфических рецепторов. Холестерин, доставленный в клетку в составе липопротеидных частиц, идет на покрытие потребностей клетки (образование мембран при делении клетки, синтез стероидных гормонов и др.). Избыточная часть неэтерифицированного (свободного) холестерина превращается в его эфиры при действии содержащегося в клетке фермента — холестеролацилтрансферазы (КФ 2.3.1.26). Обратный транспорт неэтерифицированного холестерина из различных органов и тканей в печень осуществляется липопротеидами высокой плотности, причем в кровяном русле происходит этерификация захваченного холестерина при участии лецитина и фермента холестерин-лецитин — ацилтрансферазы (КФ 2.3.1.43). Доставленный таким путем в печень холестерин идет на образование желчных кислот (см.).
Синтез холестерина

Общая схема биосинтеза холестерина
Синтез холестерина осуществляется в клетках почти всех органов и тканей, однако в значительных количествах он образуется в печени (80%), стенке тонкой кишки (10%) и коже (5%). К. Блох, Ф. Линен и др. показали основные реакции биосинтеза холестерина (их не менее 30). Сложный процесс биосинтеза холестерина можно разделить на три стадии: 1) биосинтез мевалоновой кислоты; 2) образование сквалена из мевалоновой кислоты; 3) циклизация сквалена и образование холестерина (см. схему).
Считают, что главным источником образования мевалоновой кислоты в печени является ацетил-КоА, а в мышечной ткани — лейцин. И то и другое соединения в результате ряда энзиматических реакций образуют бета-гидрокси-бета-метилглутарил-КоА (ГМГ-КоА), который затем восстанавливается в мевалоновую кислоту. В последнее время показано, что в синтез мевалоновой кислоты в печени может включаться и малонил-КоА.
Реакцией, определяющей скорость биосинтеза холестерина в целом, является восстановление ГМГ-КоА в мевалоновую кислоту; этот процесс катализирует фермент НАДФ-Н2-зависимая ГМГ-КоА-редуктаза (КФ 1.1.1.34). Именно этот фермент подвержен воздействиям со стороны ряда факторов. Так, активность ГМГ-КоА-редуктазы повышается (или содержание ее в печени возрастает) и скорость синтеза холестерина в целом увеличивается при действии ионизирующего излучения, введении тиреоидных гормонов, поверхностно-активных веществ, холестирамина, а также при гипофизэктомии. Угнетение синтеза холестерина отмечается при голодании, тиреоидэктомии и при поступлении в организм пищевого холестерина. Последний угнетает активность (или синтез) фермента ГМГ-КоА-редуктазы.
Синтез холестерина в стенке тонкой кишки регулируется исключительно концентрацией желчных кислот. Так, отсутствие их в кишечнике при наличии наружного желчного свища ведет к повышению синтеза холестерина в тонкой кишке в 5—10 раз.
На второй стадии синтеза происходит фосфорилирование мевалоновой кислоты при участии АТФ и образование нескольких фосфорилированные промежуточных продуктов (см. Фосфорилирование). При декарбоксилировании одного из них образуется изопентенил-пирофосфат, часть которого превращается в диметилаллил-пирофосфат. Взаимодействие этих двух соединений приводит к образованию димера — геранил-пирофосфата, содержащего 10 атомов углерода. Геранил-пирофосфат конденсируется с новой молекулой изопентенил-пирофосфата и образует тример — фарнезил-пирофосфат, содержащий 15 атомов углерода. Эта реакция идет с отщеплением молекулы пирофосфата. Затем две молекулы фарнезил-пирофосфата конденсируются, теряя каждая свой пирофосфат, и образуют гексамер сквален, содержащий 30 атомов углерода.
Третья стадия синтеза включает окислительную циклизацию сквалена, сопровождающуюся миграцией двойных связей и образованием первого циклического соединения — ланостерина. Ланостерин уже имеет гидроксильную группу в положении 3 и три лишние (по сравнению с холестерином) метильные группы. Дальнейшее превращение ланосте-рина может совершаться двумя путями, причем и в том и в другом случае промежуточными продуктами являются соединения стериновой природы. Более доказанным считается путь через 24, 25-дигидроланостерин и ряд других стеринов, включая 7-дигидрохолестерин, служащий непосредственным предшественником холестерина. Другой возможный путь — превращение ланостерина в зимостерин, а затем в десмостерин, из которого при восстановлении образуется холестерин.
Если суммировать общий итог всех реакций биосинтеза холестерина, то он может быть представлен в следующем виде:
18CH3CO-S-KoA + 10(H+) + 1/2O2 —> C27H46O + 9CO2 + 18KoA-SH. Источником углерода холестерина является ацетил-КоА (им может быть также малонил-КоА и лейцин), источником водорода — вода и никотин-амида дениндинуклеотидфосфат, а источником кислорода — молекулярный кислород.
Начиная со сквалена и кончая холестерином все промежуточные продукты биосинтеза нерастворимы в водной среде, поэтому они участвуют в конечных реакциях биосинтеза холестерина в связанном со сквален или стеринпереносящими белками состоянии. Это позволяет им растворяться в цитоплазме клетки и создает условия для протекания соответствующих реакций. Холестерин-переносящий белок обеспечивает также перемещение стеринов внутри клетки, что имеет важное значение для вхождения его в мембрану клетки, а также для транспорта в клеточные системы, осуществляющие катаболизм холестерина.
Катаболизм холестерина протекает в печени (окисление его в желчные кислоты), в надпочечниках и плаценте (образование из холестерина стероидных гормонов), в тестикулярной ткани и яичниках (образование половых гормонов). При биосинтезе холестерина в коже на завершающей стадии образуется небольшое количество 7-дегидрохолестерина. Под влиянием УФ-лучей он превращается в витамин D3.
Своеобразные превращения претерпевает холестерин в толстой кишке. Речь идет о той части пищевого холестерина или холестерина, поступившего в кишечник с желчью, которая не подверглась всасыванию. Под влиянием микробной флоры толстой кишки происходит восстановление холестерина и образование так наз. нейтральных стеринов. Главным их представителем является копростерин. Экспериментальные исследования, проведенные с использованием радиоизотопных и других методов, показали, что скорость обновления холестерина в различных органах и тканях неодинакова; наиболее высока она в надпочечниках и печени и чрезвычайно низка в мозге взрослых животных.
Патология холестеринового обмена
Нарушения холестеринового обмена обычно связаны с дисбалансом между количеством синтезируемого в организме и поступающего с пищей холестерина, с одной стороны, и количеством холестерина, подвергающегося катаболизму,— с другой. Эти нарушения проявляются в изменении уровня холестерина в плазме крови, которые классифицируются как гиперхолестеринемия или гипохолестеринемия (для взрослого населения высокоразвитых стран величины выше 270 мг/100 мл и ниже 150 мг/100 мл соответственно).
Гиперхолестеринемия может быть первичной (наследственной или алиментарной) и вторичной, обусловленной различными заболеваниями. Наследственная (семейная) гиперхолестеринемия характеризуется высоким уровнем холестерина и липопротеидов низкой плотности (ЛПНГЛ в плазме крови. При гомозиготной гиперхолестеринемии уровень холестеринемии может достигать 700— 800 мг/100 мл, а при гетерозиготной — 300—500 мг/100 мл. В основе наследственной гиперхолестеринемии лежит генетически обусловленное отсутствие (у гомозигот) или недостаток (у гетерозигот) специфических рецепторов к липопротеидам низкой плотности у клеток, вследствие чего резко снижается захват и последующий катаболизм этих богатых холестерином липопротеидов клетками паренхиматозных органов и тканей. В результате пониженного захвата и снижения катаболизма липопротеидов низкой плотности развивается гиперхолестеринемия (см.). Последняя приводит к раннему развитию атеросклероза (см.) и его клинических проявлений — ишемической болезни сердца (см.), преходящей ишемии мозга (см. Инсульт) и др. Особенно тяжело протекает атеросклероз при гомозиготной форме; у таких больных часто наблюдается ксантоматоз (см.), липоидная дуга роговицы (отложение холестерина в роговицу глаз), инфаркт миокарда в юношеском возрасте.
Распространенность гомозиготной формы гиперхолестеринемии невелика (примерно один случай на 1 млн. жителей). Чаще встречается гетерозиготная форма — один случай на 500 жителей.
Алиментарная гиперхолестеринемия характеризуется повышенным уровнем холестерина в плазме крови вследствие длительного потребления больших количеств пищи, богатой холестерином (куриные желтки, икра, печень, животные жиры и др.). Алиментарная гиперхолестеринемия той или иной степени выраженности характерна для жителей высокоразвитых индустриальных стран. Согласно популяционным исследованиям имеется прямая зависимость между уровнем холестерина в крови и распространенностью ишемической болезни сердца.
В эксперименте на различных животных (кролики, морские свинки, обезьяны) показано, что введение массивных доз холестерина с пищей приводит к резко выраженной гиперхолестеринемии и быстрому развитию атеросклероза. Экспериментальные модели гиперхолестеринемии и атеросклероза, впервые предложенные H. Н. Аничковым и С. С. Халатовым (1913), широко используются в научных исследованиях.
Вторичная гиперхолестеринемия встречается при гипотиреозе (см.), сахарном диабете (см. Диабет сахарный), нефротическом синдроме (см.), подагре (см.) и др. и нередко сопровождается развитием атеросклероза (см. Гиперхолестеринемия).
Выделяют первичную и вторичную гипохолестеринемию. Первичная гипохолестеринемия характерна для наследственного заболевания — абеталипопротеинемии (см.). При этой болезни отмечается почти полное отсутствие в плазме крови липопротеидов низкой плотности (у гомозигот) или значительное их снижение (у гетерозигот). Уровень общего холестерина не превышает 75 мг/ 100 мл. Гомозиготная форма болезни протекает исключительно тяжело. В основе абеталипопротеинемии лежит генетически обусловленное нарушение синтеза апопротеина В — главного белка липопротеидов низкой плотности.
Вторичные гипохолестеринемии наблюдаются при кахексии, гипертиреоидизме, аддисоновой болезни и паренхиматозных заболеваниях печени, при ряде инфекционных болезней и интоксикациях (см. Гипохолестеринемия). При недостаточной активности в плазме крови фермента лецитин — холестерин -ацилтрансферазы, или ЛХАТ (наследственная ЛXАТ-недостаточность), ответственного за этерификацию холестерина плазмы, наблюдается накопление неэтерифицированного холестерина в мембранах эритроцитов и клетках почек, печени, селезенки, костного мозга, роговицы глаза. Резко снижается доля этерифицированного холестерина в плазме крови и одновременно повышается уровень неэтерифицированного холестерина и лецитина. У больных с наследственной ЛXAT-недостаточностыо стенки артерий и капилляров подвержены деструктивным изменениям, что связано с отложением в них липидов. Наиболее тяжелые изменения происходят в сосудах почечных клубочков, что приводит к развитию почечной недостаточности (см.).
Одним из распространенных нарушений холестериновый обмен. является образование желчных камней, основной составной частью которых является холестерин (см. Желчнокаменная болезнь). Образование желчных камней происходит вследствие выкристаллизовывания холестерина при относительно высокой его концентрации в желчи и относительно низкой концентрации в ней желчных кислот и фосфолипидов, обладающих способностью растворять холестерин. Исследования показали, что имеется прямая связь между уровнем холестерина в плазме крови и распространенностью холестероза (см.) и желчнокаменной болезни.
Библиогр.: Климов А. Н, и Н икульчева Н. Г. Липопротеиды, дислипопротеидемии и атеросклероз, Л., 1984; Полякова Э. Д. Пути биосинтеза холестерина в печени и их регуляция, в кн.: Липиды, структура,биосинтез, превращения и функции, под ред. С. Е. Северина, с. 131, М., 1977;она же, Регуляция содержания холестерина в клетке, в кн.: Биохимия липидов и их роль в обмене веществ, под ред.С. Е. Северина, с. 120, М., 1981; Финагин Л. К. Обмен холестерина и его регуляция, Киев, 1980; Lipids and lipidoses, ed. by G. Schettler, B.— Heidelberg, 1967; Sodhi H. S., Kudchod-k a r B. J. a. Mason D. T. Clinical methods in study of cholesterol metabolism, Basel a. o., 1979.
A. H. Климов
Источник
37. Превращение холестерина в желчные кислоты, выведение из организма х и жк.
Жёлчные
кислоты синтезируются в печени из
холестерола. Часть жёлчных кислот в
печени подвергается реакции конъюгации
— соединения с гидрофильными молекулами
(глицином и таурином). Жёлчные кислоты
обеспечивают эмульгирование жиров,
всасывание продуктов их переваривания
и некоторых гидрофобных веществ,
поступающих с пищей, например
жирорастворимых витаминов и холестерола.
Жёлчные кислоты также всасываются,
через юротную вену попадают опять в
печень и многократно используются для
эмульгирования жиров. Этот путь называют
энтерогепатической циркуляцией жёлчных
кислот.
Синтез
жёлчных кислот
В
организме за сутки синтезируется 200-
600 мг жёлчных кислот. Первая реакция
синтеза — образование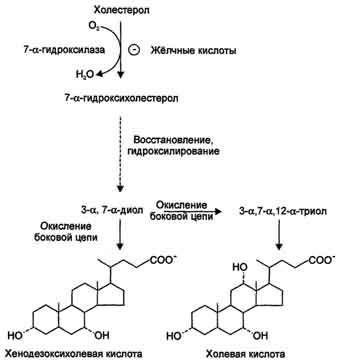
7-α-гидроксихолестерола
— является регуляторной. Фермент
7-α-гидроксилаза, катализирующий эту
реакцию, ингибируется конечным продуктом
— жёлчными кислотами. 7-α-Гидроксилаза
представляет собой одну из форм цитохрома
Р450 и
использует кислород как один из
субстратов. Один атом кислорода из
О2 включается
в гидроксильную группу в положении 7, а
другой восстанавливается до воды.
Последующие реакции синтеза приводят
к формированию 2 видов жёлчных кислот:
холевой и хенодезоксихолевой (рис.
8-71), которые называют «первичными
жёлчными кислотами».
(думаю
тут достаточно написать, без таблиц,
т.к. много получается)
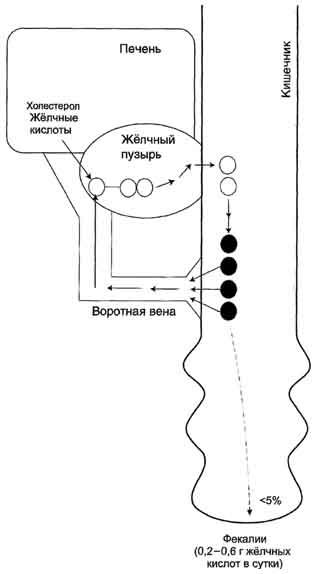
Путь
выведения жёлчных кислот одновременно
служит и основным путём выведения
холестерола из организма. Для восполнения
потери жёлчных кислот с фекалиями в
печени постоянно происходит синтез
жёлчных кислот из холестерола в
количестве, эквивалентном выведенным
жёлчным кислотам. В результате пул
жёлчных кислот (2-4 г) остаётся постоянным.
38. Конъюгация желчных кислот, первичные и вторичные жк
Конъюгирование
— присоединение ионизированных молекул
глицина или таурина к карбоксильной
группе жёлчных кислот; усиливает их
детергентные свойства, так как увеличивает
амфифильность молекул
Конъюгация
происходит в клетках печени и начинается
с образования активной формы жёлчных
кислот — производных КоА
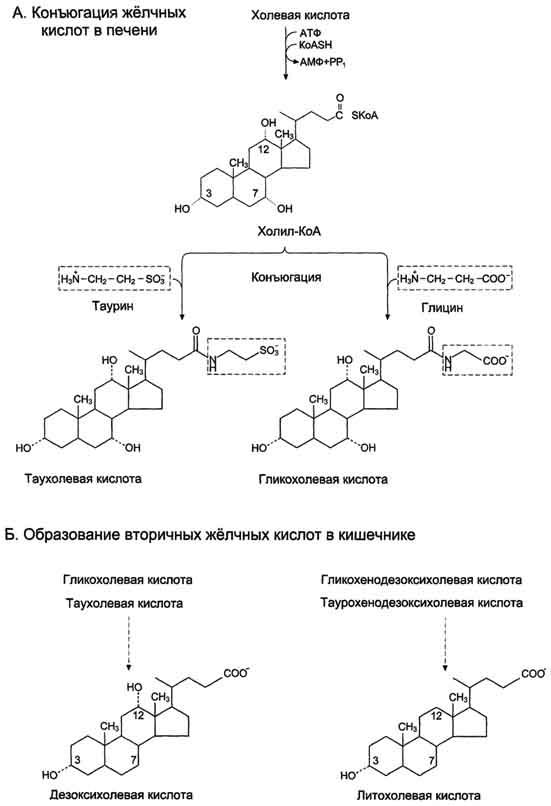
Затем
присоединяется таурин или глицин, и в
результате образуется 4 варианта
конъюгатов: таурохолевая и
таурохенодезоксихолевая, гликохолевая
или гликохенодезоксихолевая кислоты
(они значительно более сильные эмульгаторы,
чем исходные жёлчные кислоты). А потом
они превращаются во вторичные жк,
таурохолевая в дезоксихолевую, а
таурохендодезоксихолевая в литохолевую.
Ну а про первичные смотри выше.
39. Гиперхолестеринэмия и ее причины.
Гиперхолестеролемия.
Роль алиментарных факторов в развитии
гиперхолестеролемии
Концентрация
холестерола в крови взрослых людей
составляет 200±50 мг/дл (5,2±1,2 ммоль/л) и,
как правило, увеличивается с возрастом.
Превышение нормальной концентрации
холестерола в крови называют
гиперхолестеролемией.
Гиперхолестеролемия
часто развивается вследствие избыточного
поступления холестерола с пищей, а также
углеводов и жиров. Гиперкалорийное
питание — один из распространённых
факторов развития гиперхолестеролемии,
так как для синтеза холестерола необходимы
только ацетил-КоА, АТФ и NADPH. Все эти
субстраты образуются при окислении
глюкозы и жирных кислот, поэтому
избыточное поступление этих компонентов
пищи способствует развитию
гиперхолестеролемии. В норме поступление
холестерола с пищей снижает синтез
собственного холестерола в печени,
однако с возрастом эффективность
регуляции у многих людей снижается.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
ЖЁЛЧНЫЕ КИСЛОТЫ — Большая Медицинская Энциклопедия
ЖЁЛЧНЫЕ КИСЛОТЫ (син. холевые кислоты) — органические кислоты, являющиеся специфическими компонентами желчи и играющие важную роль в переваривании и всасывании жиров, а также в некоторых других процессах, происходящих в желудочно-кишечном тракте, в том числе в переносе липидов в водной среде. Ж. к. представляют собой также конечный продукт обмена холестерина (см.), который выводится из организма в основном в виде Ж. к.
По своей хим. природе Ж. к. являются производными холановой к-ты (C23H39COOH), к кольцевой структуре к-рой присоединены одна, две или три гидроксильные группы. Боковая цепь Ж. к., так же как и в молекуле холановой к-ты, включает 5 углеродных атомов с COOH-группой на конце.
В желчи человека содержатся: холевая (3-альфа,7-альфа,12-альфа-триокси-5-бета-холановая) к-та:

хенодезоксихолевая (антроподезоксихолевая) (3-альфа,7-альфа-диокси-5-бета-холановая) к-та:

и дезоксихолевая (3-альфа,12-альфа-диокси-5-бета-холановая) к-та:

кроме того, в малых количествах или в виде следов содержатся литохолевая (З-альфа-моноокси-5-бета-холановая), а также аллохолевая и урсодезоксихолевая к-ты — стереоизомеры холевой и хенодезоксихолевой к-т. Все Ж. к. присутствуют в желчи (см.) в конъюгированном виде. Часть их конъюгирована с глицином (гликоколом) в гликохолевую или гликохенодезоксихолевую к-ту, а часть — с таурином в таурохолевую:

или таурохенодезоксихолевую к-ту. В печеночной желчи Ж. к. диссоциируют и находятся в форме желчнокислых солей натрия и калия (холатов и дезоксихолатов Na и К), что объясняется щелочными значениями pH желчи (7,5—8,5).
Из всех Ж. к. только холевая и хенодезоксихолевая к-ты первично образуются в печени (их называют первичными), тогда как другие образуются в кишечнике под влиянием ферментов кишечной микрофлоры и носят название вторичных. Они всасываются в кровь и затем вновь секретируются печенью в составе желчи.
У безмикробных животных, выращенных в стерильных условиях, в желчи присутствуют лишь холевая и хенодезоксихолевая к-ты, а дезоксихолевая и литохолевая отсутствуют и появляются в желчи только с внесением в кишечник микроорганизмов. Это подтверждает вторичное образование этих Ж. к. в кишечнике под влиянием микрофлоры из холевой и хенодезоксихолевой к-т соответственно.
Первичные Ж. к. образуются в печени из холестерина.

Этот процесс довольно сложен, т. к. Ж. к. отличаются от холестерина по стереохим. конфигурации двух участков молекулы. Гидроксильная группа у 3-го C-атома в молекуле Ж. к. находится в альфа-положении, a в молекуле холестерина — в бета-положении. Водород у 3-го C-атома Ж. к. находится в p-положении, что соответствует транс-конфигурации колец А и В, а в холестерине — в a-положении (цис-конфигурация колец А и В). Кроме того, Ж. к. содержат большее количество гидроксильных групп, более короткую боковую цепь, которая характеризуется наличием карбоксильной группы.
Процесс превращения холестерина в холевую к-ту начинается с гидроксилирования холестерина в 7альфа-положении, т. е. с включения гидроксильной группы в положение 7, затем следует окисление OH-группы у 3-го С-атома в кетогруппу, перемещение двойной связи от 5-го С-атома к 4-му C-атому, гидроксилирование в 12-альфа-положении и т. д. Все эти реакции катализируются микросомальными ферментами печени в присутствии НАД•H или НАДФ•Н. Окисление боковой цепи в молекуле холестерина осуществляется при участии ряда дегидрогеназ в присутствии АТФ, КоА и ионов Mg2+. Процесс идет через стадию образования 3-альфа, 7-альфа, 12-альфа-триоксикопростановой к-ты, к-рая затем подвергается бета-окислению. В завершающей стадии отделяется трехуглеродный фрагмент, представляющий собой пропионил-КоА, и боковая цепь молекулы, т. о., укорачивается. Последовательность этих реакций в некоторых звеньях может меняться. Напр., образование кетогруппы в 3-бета-положении может происходить не до, а после гидроксилирования в 12-альфа-положении. Однако это не изменяет основного направления процесса.
Процесс образования хенодезоксихолевой к-ты из холестерина имеет некоторые особенности. В частности, окисление боковой цепи с образованием гидроксила у 26-го С-атома может начинаться на каждой стадии процесса, причем гидроксилированный продукт участвует далее в реакциях в обычной последовательности. Возможно, что раннее присоединение OH-группы к 26-му C-атому по сравнению с обычным течением процесса является важным фактором в регуляции синтеза хенодезоксихолевой к-ты. Установлено, что эта к-та не является предшественником холевой и не превращается в нее; равным образом и холевая к-та в организме человека и животных не превращается в хенодезоксихолевую.
Конъюгирование Ж. к. протекает в две стадии. Первая стадия заключается в образовании ацил-КоА, т. е. КоА-эфиров Ж. к. Для первичных Ж. к. эта стадия осуществляется уже на конечном этапе их образования. Вторая стадия конъюгирования Ж. к.— собственно Конъюгирование — состоит в соединении посредством амидной связи молекулы Ж. к. с глицином или таурином. Этот процесс катализируется лизосомальной ацилтрансферазой.
В желчи человека основные Ж. к.— холевая, хенодезоксихолевая и дезоксихолевая — находятся в количественном соотношении 1:1:0,6; глициновые и тауриновые конъюгаты этих к-т — в соотношении 3:1. Соотношение между двумя этими конъюгатами меняется в зависимости от характера пищи: в случае преобладания в ней углеводов увеличивается относительное содержание глициновых конъюгатов, а при высокобелковой диете — тауриновых конъюгатов. Кортикостероидные гормоны повышают относительное содержание тауриновых конъюгатов в желчи. Наоборот, при заболеваниях, сопровождающихся белковой недостаточностью, увеличивается доля глициновых конъюгатов.
Отношение глицин-конъюгированных к таурин-конъюгированным Ж. к. у человека изменяется под влиянием тиреоидного гормона, увеличиваясь при гипотиреоидной состоянии. Кроме того, у больных с гипотиреоидизмом холевая к-та имеет большее время полусуществования и медленнее обменивается, чем у больных с гипертиреоидизмом, что сопровождается повышением содержания холестерина в крови у больных с пониженной функцией щитовидной железы.
У животных и человека при кастрации повышается содержание холестерина в крови. В эксперименте снижение концентрации холестерина в сыворотке крови и увеличение образования Ж. к. наблюдали при введении эстрогена. Тем не менее действие гормонов на биосинтез Ж. к. изучено еще недостаточно.
В желчи различных животных состав Ж. к. сильно варьирует. У многих из них обнаруживаются Ж. к., отсутствующие у человека. Так, у некоторых амфибий главным компонентом желчи является кипринол — желчный спирт, который, в отличие от холевой к-ты, имеет более длинную боковую цепь с двумя гидроксильными группами у 26-го и 27-го С-атомов. Этот спирт конъюгируется преимущественно с сульфатом. У других амфибий преобладает желчный спирт буфол, имеющий ОН-группы у 25-го и 26-го C-атомов. У свиньи в желчи присутствует гиохолевая к-та с OH-группойв положении 6-го С-атома (3-альфа,6-альфа,7-альфа-триоксихолановая к-та). У крыс и мышей имеются альфа- и бета-марихолевые к-ты — стереоизомеры гиохолевой к-ты. У животных, питающихся растительной пищей, в желчи преобладает хенодезоксихолевая к-та. Напр., у морской свинки она является единственной из основных Ж. к. Холевая к-та, напротив, более характерна для плотоядных животных.
Одна из главных функций Ж. к.— перенос липидов в водной среде — связана с их детергентными свойствами, т. е. с их способностью растворять липиды путем образования мицеллярного раствора. Эти свойства Ж. к. проявляются уже в ткани печени, где при их участии из ряда компонентов желчи образуются (или окончательно формируются) мицеллы, получившие название липидного комплекса желчи. Благодаря включению в этот комплекс секретируемые печенью липиды и некоторые другие плохо растворимые в воде вещества переносятся в кишечник в виде гомогенного р-ра в составе желчи.
В кишечнике соли Ж. к. участвуют в эмульгировании жира. Они входят в состав эмульгирующей системы, включающей в себя насыщенный моноглицерид, ненасыщенную жирную к-ту и соли Ж. к. При этом они играют роль стабилизаторов жировой эмульсии. Ж. к. выполняют также важную роль в качестве своеобразного активатора панкреатической липазы (см.). Их активирующее влияние выражается в смещении оптимума действия липазы, который в присутствии Ж. к. перемещается с pH 8,0 до pH 6,0, т. е. до той величины pH, к-рая более постоянно поддерживается в двенадцатиперстной кишке в ходе переваривания жирной пищи.
После расщепления жира липазой продукты этого расщепления — моноглицериды и жирные кислоты (см.) образуют мицеллярный р-р. Решающую роль в этом процессе играют соли Ж. к. Благодаря их детергент-ному действию в кишечнике образуются устойчивые в водной среде мицеллы (см. Молекула), содержащие продукты расщепления жира, холестерин и часто фосфолипиды. В таком виде эти вещества переносятся с эмульсионных частиц, т. е. с места гидролиза липидов, к всасывающей поверхности кишечного эпителия. В виде мицеллярного р-ра, образующегося при участии солей Ж. к., переносятся в жел.-киш. тракте и жирорастворимые витамины. Выключение Ж. к. из пищеварительных процессов, напр, при экспериментальном отведении желчи из кишечника, приводит к снижению всасывания жира в жел.-киш. тракте на 50% и к нарушению всасывания жирорастворимых витаминов вплоть до развития явлений витаминной недостаточности, напр, недостаточности витамина К. Помимо этого, Ж. к. оказывают стимулирующее действие на рост и функции нормальной кишечной микрофлоры: при прекращении поступления желчи в кишечник жизнедеятельность микрофлоры претерпевает существенные изменения.
Выполнив свою физиол, роль в кишечнике, Ж. к. в подавляющем количестве всасываются в кровь, возвращаются к печени и вновь секретируются в составе желчи. Происходит, т. о., постоянная циркуляция Ж. к. между печенью и кишечником. Этот процесс называется печеночно-кишечной (энтерогепатической или портально-билиарной) циркуляцией Ж. к.
Основная масса Ж. к. всасывается в конъюгированном виде в подвздошной кишке. В проксимальной части тонкой кишки нек-рое количество Ж. к. переходит в кровь путем пассивного всасывания.
Исследования, проведенные с помощью меченных 14C Ж. к., показали, что в желчи содержится лишь небольшая часть Ж. к., вновь синтезированных печенью [С. Бергстрем, Даниэльссон (H. Danielsson), 1968]. На их долю приходится только 10—15% от общего количества Ж. к. Основную же массу Ж. к. желчи (85—90%) составляют Ж. к., реабсорбированные в кишечнике и повторно секретируемые в составе желчи, т. е. Ж. к., участвующие в печеночно-кишечной циркуляции. Общий пул Ж. к. у человека в среднем составляет 2,8—3,5 г, причем они совершают 5—6 оборотов за сутки. У разных животных число оборотов, совершаемых Ж. к. за сутки, сильно варьирует: у собаки оно также равно 5—6, а у крысы 10—12.
Часть Ж. к. подвергается в кишечнике деконъюгированию под влиянием нормальной кишечной микрофлоры. При этом нек-рое количество их теряет гидроксильную группу, превращаясь в дезоксихолевую, литохолевую или в другие к-ты. Все они всасываются и после конъюгирования в печени секретируются в составе желчи. Однако 10—15% всех поступивших в кишечник Ж. к. после деконъюгирования подвергается более глубокой деградации. В результате процессов окисления и восстановления, вызываемых ферментами микрофлоры, эти Ж. к. претерпевают различные изменения, сопровождающиеся частичным разрывом их кольцевой структуры. Целый ряд образующихся продуктов затем выделяется с фекалиями.
Биосинтез Ж. к. контролируется по типу отрицательной обратной связи определенным количеством Ж. к., возвращающихся в печень в процессе печеночно-кишечной циркуляции.
Показано, что разные Ж. к. оказывают качественно и количественно различное регулирующее действие. У человека, напр., хенодезоксихолевая к-та тормозит образование холевой к-ты.
Увеличение содержания холестерина в пище приводит к усилению биосинтеза Ж. к.
Разрушение и выброс части Ж. к, представляют важнейший путь экскреции конечных продуктов обмена холестерина. Показано, что у безмикробных животных, лишенных кишечной микрофлоры, сокращается число оборотов, совершаемых Ж. к. между печенью и кишечником, и резко снижается экскреция Ж. к. с фекалиями, что сопровождается повышением содержания холестерина в сыворотке крови.
Т. о., достаточно интенсивная секреция Ж. к. в составе желчи и их превращение в кишечнике под влиянием микрофлоры чрезвычайно важны как для пищеварения, так и для обмена холестерина.
В норме в моче у человека Ж. к. не содержатся, очень небольшие их количества появляются в моче при обтурационной желтухе (ранние стадии) и острых панкреатитах. Ж. к. являются самыми сильными холеретиками, напр, дегидрохолевая кислота (см.). Это свойство Ж. к. используется для введения их в состав желчегонных средств (см.) — дехолина, аллохола и др. Ж. к. стимулируют перистальтику кишечника. Запоры, наблюдаемые у больных с желтухой, могут быть обусловлены дефицитом холатов (солей Ж. к.). Однако одномоментное поступление большого количества конц. желчи в кишечник, а с нею и большого количества Ж. к., наблюдающееся у ряда больных после удаления желчного пузыря, может вызвать понос. Кроме того, Ж. к. обладают бактериостатическим действием.
Общая концентрация Ж. к. в крови и их соотношение существенно изменяются при ряде заболеваний печени и желчного пузыря, что используется в диагностических целях. При паренхиматозных поражениях печени резко снижается способность печеночных клеток захватывать Ж. к. из крови, в результате чего они накапливаются в крови и выделяются с мочой. Повышение концентрации Ж. к. в крови наблюдается и при затруднении оттока желчи, особенно при обтурации общего желчного протока (камень, опухоль), что сопровождается также нарушением печеночно-кишечной циркуляции с резким уменьшением или исчезновением конъюгатов дезоксихолатов из желчи. Длительное и существенное повышение концентрации Ж. к. в крови может оказывать повреждающее действие на печеночные клетки с развитием некрозов и изменением активности некоторых ферментов в сыворотке крови.
Высокая концентрация холатов в крови вызывает брадикардию и гипотонию, кожный зуд, гемолиз, повышение осмотической резистентности эритроцитов, нарушает процессы свертывания крови, замедляет скорость оседания эритроцитов. С выделением при болезнях печени Ж. к. через почки связывают развитие почечной недостаточности.
При острых и хрон, холециститах наблюдается уменьшение концентрации или полное исчезновение холатов из пузырной желчи, что объясняется уменьшением их образования в печени и ускорением всасывания их слизистой оболочкой воспаленного желчного пузыря.
Ж. к. и их производные разрушают в течение нескольких минут клетки крови, в том числе и лейкоциты, что следует учитывать при оценке диагностического значения количества лейкоцитов в дуоденальном содержимом. Холаты разрушают также и ткани, не соприкасающиеся в физиол, условиях с желчью, вызывают повышение проницаемости мембран и местное воспаление. При попадании желчи, напр., в брюшную полость быстро развивается тяжелый перитонит. В механизме развития острого панкреатита, антрального гастрита и даже язвы желудка определенную роль отводят Ж. к. Допускается возможность повреждения самого желчного пузыря конц. желчью, содержащей большое количество Ж. к. («химический» холецистит) .
Ж. к. являются исходным продуктом для производства стероидных гормонов. Благодаря сходству химического строения стероидных гормонов и Ж. к. последние обладают выраженным противовоспалительным действием. На этом свойстве Ж. к. основан метод лечения артритов местным применением конц. желчи (см. Желчь).
Для лечения поносов, возникающих после оперативного удаления части кишечника, и упорного кожного зуда у больных с заболеваниями печени и желчных путей применяются препараты, связывающие Ж. к. в кишечнике, напр, холестирамин.
См. также Жировой обмен, Печень.
Библиография: Комаров Ф. И. и Иванов А. И. Желчные кислоты, физиологическая роль, клиническое значение, Тер. арх., т. 44, № 3, с. 10, 1972; Куваева И. Б. Обмен веще