Процесс превращения холестерина в желчные кислоты
Содержание статьи
37. Превращение холестерина в желчные кислоты, выведение из организма х и жк.
Жёлчные кислоты синтезируются в печени из холестерола. Часть жёлчных кислот в печени подвергается реакции конъюгации — соединения с гидрофильными молекулами (глицином и таурином). Жёлчные кислоты обеспечивают эмульгирование жиров, всасывание продуктов их переваривания и некоторых гидрофобных веществ, поступающих с пищей, например жирорастворимых витаминов и холестерола. Жёлчные кислоты также всасываются, через юротную вену попадают опять в печень и многократно используются для эмульгирования жиров. Этот путь называют энтерогепатической циркуляцией жёлчных кислот.
Синтез жёлчных кислот
В организме за сутки синтезируется 200- 600 мг жёлчных кислот. Первая реакция синтеза — образование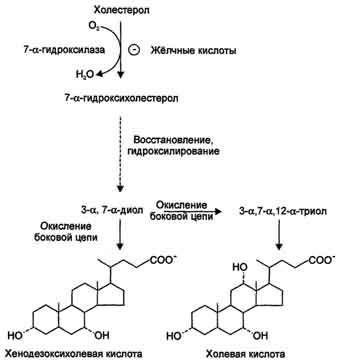
7-α-гидроксихолестерола — является регуляторной. Фермент 7-α-гидроксилаза, катализирующий эту реакцию, ингибируется конечным продуктом — жёлчными кислотами. 7-α-Гидроксилаза представляет собой одну из форм цитохрома Р450 и использует кислород как один из субстратов. Один атом кислорода из О2 включается в гидроксильную группу в положении 7, а другой восстанавливается до воды. Последующие реакции синтеза приводят к формированию 2 видов жёлчных кислот: холевой и хенодезоксихолевой (рис. 8-71), которые называют «первичными жёлчными кислотами».
(думаю тут достаточно написать, без таблиц, т.к. много получается)
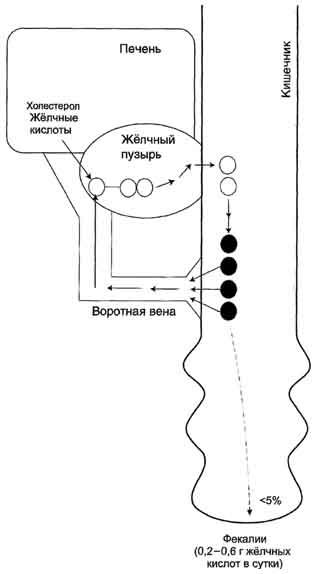
Путь выведения жёлчных кислот одновременно служит и основным путём выведения холестерола из организма. Для восполнения потери жёлчных кислот с фекалиями в печени постоянно происходит синтез жёлчных кислот из холестерола в количестве, эквивалентном выведенным жёлчным кислотам. В результате пул жёлчных кислот (2-4 г) остаётся постоянным.
38. Конъюгация желчных кислот, первичные и вторичные жк
Конъюгирование — присоединение ионизированных молекул глицина или таурина к карбоксильной группе жёлчных кислот; усиливает их детергентные свойства, так как увеличивает амфифильность молекул
Конъюгация происходит в клетках печени и начинается с образования активной формы жёлчных кислот — производных КоА
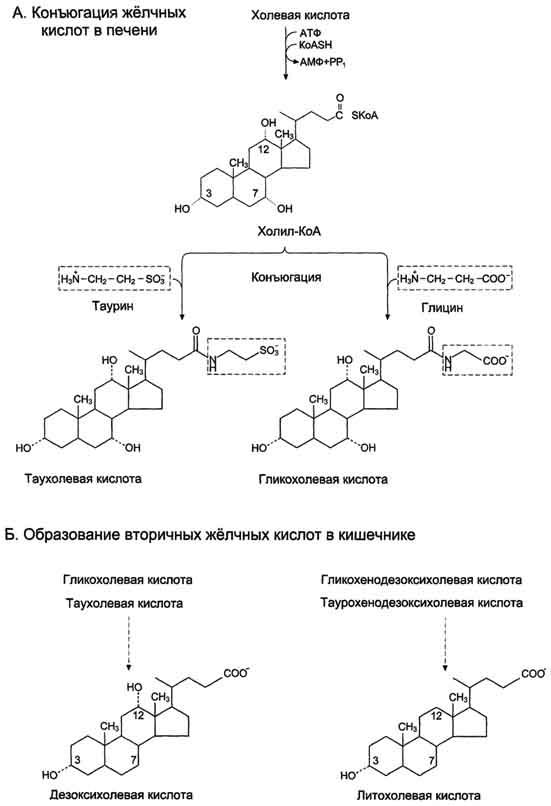
Затем присоединяется таурин или глицин, и в результате образуется 4 варианта конъюгатов: таурохолевая и таурохенодезоксихолевая, гликохолевая или гликохенодезоксихолевая кислоты (они значительно более сильные эмульгаторы, чем исходные жёлчные кислоты). А потом они превращаются во вторичные жк, таурохолевая в дезоксихолевую, а таурохендодезоксихолевая в литохолевую. Ну а про первичные смотри выше.
39. Гиперхолестеринэмия и ее причины.
Гиперхолестеролемия. Роль алиментарных факторов в развитии гиперхолестеролемии
Концентрация холестерола в крови взрослых людей составляет 200±50 мг/дл (5,2±1,2 ммоль/л) и, как правило, увеличивается с возрастом. Превышение нормальной концентрации холестерола в крови называют гиперхолестеролемией.
Гиперхолестеролемия часто развивается вследствие избыточного поступления холестерола с пищей, а также углеводов и жиров. Гиперкалорийное питание — один из распространённых факторов развития гиперхолестеролемии, так как для синтеза холестерола необходимы только ацетил-КоА, АТФ и NADPH. Все эти субстраты образуются при окислении глюкозы и жирных кислот, поэтому избыточное поступление этих компонентов пищи способствует развитию гиперхолестеролемии. В норме поступление холестерола с пищей снижает синтез собственного холестерола в печени, однако с возрастом эффективность регуляции у многих людей снижается.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
ХОЛЕСТЕРИНОВЫЙ ОБМЕН
ХОЛЕСТЕРИНОВЫЙ ОБМЕН (греческий chole желчь + stereos твердый) — совокупность реакций биосинтеза холестерина (см.) и его распада в организме человека и животных. В организме человека за сутки около 500 мг холестерина окисляется в желчные кислоты, примерно такое же количество стеринов экскретируется с фекалиями, около 100 мг выделяется с кожным салом, небольшое количество холестерина (около 40 мг) используется для образования кортикоидных и половых гормонов, а также витамина D3, 1-2 мг холестерина выводится с мочой. У кормящих женщин с грудным молоком выделяется 100- 200 мг холестерина в сутки. Эти потери восполняются за счет синтеза холестерина в организме (у взрослого человека в сутки около 700-1000 мг) и поступления его с пищей (300- 500 мг). Холестерин, а также часть холестерина, поступившего в просвет кишечника с желчью, всасывается в тонкой кишке в форме жировых мицелл (см. Жировой обмен). Эфиры холестерина предварительно гидролизуются при действии холестеринэстеразы (см.) панкреатического и кишечного соков. В стенке тонкой кишки холестерин используется для образования хиломикронов (см. Липопротеиды), в составе которых он поступает сначала в лимфатическую систему, а затем в кровяное русло.
В капиллярах жировой и некоторых других тканей в результате воздействия на хиломикроны липопротеид-липазы образуются частицы, обогащенные эфирами холестерина и фосфолипидами, получившие название ремнантных (остаточных) частиц. Эти частицы задерживаются в печени, где подвергаются распаду. Освободившийся при этом холестерин наряду с холестерином, синтезированным в печени, образует так называемый общий пул печеночного холестерина, который используется по мере необходимости для образования липопротеидов (см.).
Установлено, что у человека и некоторых животных липопротеиды низкой плотности транспортируют холестерин в органы и ткани, причем захват липоиротеидных частиц клетками этих органов и тканей осуществляется при участии специфических рецепторов. Холестерин, доставленный в клетку в составе липопротеидных частиц, идет на покрытие потребностей клетки (образование мембран при делении клетки, синтез стероидных гормонов и др.). Избыточная часть неэтерифицированного (свободного) холестерина превращается в его эфиры при действии содержащегося в клетке фермента — холестеролацилтрансферазы (КФ 2.3.1.26). Обратный транспорт неэтерифицированного холестерина из различных органов и тканей в печень осуществляется липопротеидами высокой плотности, причем в кровяном русле происходит этерификация захваченного холестерина при участии лецитина и фермента холестерин-лецитин — ацилтрансферазы (КФ 2.3.1.43). Доставленный таким путем в печень холестерин идет на образование желчных кислот (см.).
Синтез холестерина

Общая схема биосинтеза холестерина
Синтез холестерина осуществляется в клетках почти всех органов и тканей, однако в значительных количествах он образуется в печени (80%), стенке тонкой кишки (10%) и коже (5%). К. Блох, Ф. Линен и др. показали основные реакции биосинтеза холестерина (их не менее 30). Сложный процесс биосинтеза холестерина можно разделить на три стадии: 1) биосинтез мевалоновой кислоты; 2) образование сквалена из мевалоновой кислоты; 3) циклизация сквалена и образование холестерина (см. схему).
Считают, что главным источником образования мевалоновой кислоты в печени является ацетил-КоА, а в мышечной ткани — лейцин. И то и другое соединения в результате ряда энзиматических реакций образуют бета-гидрокси-бета-метилглутарил-КоА (ГМГ-КоА), который затем восстанавливается в мевалоновую кислоту. В последнее время показано, что в синтез мевалоновой кислоты в печени может включаться и малонил-КоА.
Реакцией, определяющей скорость биосинтеза холестерина в целом, является восстановление ГМГ-КоА в мевалоновую кислоту; этот процесс катализирует фермент НАДФ-Н2-зависимая ГМГ-КоА-редуктаза (КФ 1.1.1.34). Именно этот фермент подвержен воздействиям со стороны ряда факторов. Так, активность ГМГ-КоА-редуктазы повышается (или содержание ее в печени возрастает) и скорость синтеза холестерина в целом увеличивается при действии ионизирующего излучения, введении тиреоидных гормонов, поверхностно-активных веществ, холестирамина, а также при гипофизэктомии. Угнетение синтеза холестерина отмечается при голодании, тиреоидэктомии и при поступлении в организм пищевого холестерина. Последний угнетает активность (или синтез) фермента ГМГ-КоА-редуктазы.
Синтез холестерина в стенке тонкой кишки регулируется исключительно концентрацией желчных кислот. Так, отсутствие их в кишечнике при наличии наружного желчного свища ведет к повышению синтеза холестерина в тонкой кишке в 5-10 раз.
На второй стадии синтеза происходит фосфорилирование мевалоновой кислоты при участии АТФ и образование нескольких фосфорилированные промежуточных продуктов (см. Фосфорилирование). При декарбоксилировании одного из них образуется изопентенил-пирофосфат, часть которого превращается в диметилаллил-пирофосфат. Взаимодействие этих двух соединений приводит к образованию димера — геранил-пирофосфата, содержащего 10 атомов углерода. Геранил-пирофосфат конденсируется с новой молекулой изопентенил-пирофосфата и образует тример — фарнезил-пирофосфат, содержащий 15 атомов углерода. Эта реакция идет с отщеплением молекулы пирофосфата. Затем две молекулы фарнезил-пирофосфата конденсируются, теряя каждая свой пирофосфат, и образуют гексамер сквален, содержащий 30 атомов углерода.
Третья стадия синтеза включает окислительную циклизацию сквалена, сопровождающуюся миграцией двойных связей и образованием первого циклического соединения — ланостерина. Ланостерин уже имеет гидроксильную группу в положении 3 и три лишние (по сравнению с холестерином) метильные группы. Дальнейшее превращение ланосте-рина может совершаться двумя путями, причем и в том и в другом случае промежуточными продуктами являются соединения стериновой природы. Более доказанным считается путь через 24, 25-дигидроланостерин и ряд других стеринов, включая 7-дигидрохолестерин, служащий непосредственным предшественником холестерина. Другой возможный путь — превращение ланостерина в зимостерин, а затем в десмостерин, из которого при восстановлении образуется холестерин.
Если суммировать общий итог всех реакций биосинтеза холестерина, то он может быть представлен в следующем виде:
18CH3CO-S-KoA + 10(H+) + 1/2O2 -> C27H46O + 9CO2 + 18KoA-SH. Источником углерода холестерина является ацетил-КоА (им может быть также малонил-КоА и лейцин), источником водорода — вода и никотин-амида дениндинуклеотидфосфат, а источником кислорода — молекулярный кислород.
Начиная со сквалена и кончая холестерином все промежуточные продукты биосинтеза нерастворимы в водной среде, поэтому они участвуют в конечных реакциях биосинтеза холестерина в связанном со сквален или стеринпереносящими белками состоянии. Это позволяет им растворяться в цитоплазме клетки и создает условия для протекания соответствующих реакций. Холестерин-переносящий белок обеспечивает также перемещение стеринов внутри клетки, что имеет важное значение для вхождения его в мембрану клетки, а также для транспорта в клеточные системы, осуществляющие катаболизм холестерина.
Катаболизм холестерина протекает в печени (окисление его в желчные кислоты), в надпочечниках и плаценте (образование из холестерина стероидных гормонов), в тестикулярной ткани и яичниках (образование половых гормонов). При биосинтезе холестерина в коже на завершающей стадии образуется небольшое количество 7-дегидрохолестерина. Под влиянием УФ-лучей он превращается в витамин D3.
Своеобразные превращения претерпевает холестерин в толстой кишке. Речь идет о той части пищевого холестерина или холестерина, поступившего в кишечник с желчью, которая не подверглась всасыванию. Под влиянием микробной флоры толстой кишки происходит восстановление холестерина и образование так наз. нейтральных стеринов. Главным их представителем является копростерин. Экспериментальные исследования, проведенные с использованием радиоизотопных и других методов, показали, что скорость обновления холестерина в различных органах и тканях неодинакова; наиболее высока она в надпочечниках и печени и чрезвычайно низка в мозге взрослых животных.
Патология холестеринового обмена
Нарушения холестеринового обмена обычно связаны с дисбалансом между количеством синтезируемого в организме и поступающего с пищей холестерина, с одной стороны, и количеством холестерина, подвергающегося катаболизму,- с другой. Эти нарушения проявляются в изменении уровня холестерина в плазме крови, которые классифицируются как гиперхолестеринемия или гипохолестеринемия (для взрослого населения высокоразвитых стран величины выше 270 мг/100 мл и ниже 150 мг/100 мл соответственно).
Гиперхолестеринемия может быть первичной (наследственной или алиментарной) и вторичной, обусловленной различными заболеваниями. Наследственная (семейная) гиперхолестеринемия характеризуется высоким уровнем холестерина и липопротеидов низкой плотности (ЛПНГЛ в плазме крови. При гомозиготной гиперхолестеринемии уровень холестеринемии может достигать 700- 800 мг/100 мл, а при гетерозиготной — 300-500 мг/100 мл. В основе наследственной гиперхолестеринемии лежит генетически обусловленное отсутствие (у гомозигот) или недостаток (у гетерозигот) специфических рецепторов к липопротеидам низкой плотности у клеток, вследствие чего резко снижается захват и последующий катаболизм этих богатых холестерином липопротеидов клетками паренхиматозных органов и тканей. В результате пониженного захвата и снижения катаболизма липопротеидов низкой плотности развивается гиперхолестеринемия (см.). Последняя приводит к раннему развитию атеросклероза (см.) и его клинических проявлений — ишемической болезни сердца (см.), преходящей ишемии мозга (см. Инсульт) и др. Особенно тяжело протекает атеросклероз при гомозиготной форме; у таких больных часто наблюдается ксантоматоз (см.), липоидная дуга роговицы (отложение холестерина в роговицу глаз), инфаркт миокарда в юношеском возрасте.
Распространенность гомозиготной формы гиперхолестеринемии невелика (примерно один случай на 1 млн. жителей). Чаще встречается гетерозиготная форма — один случай на 500 жителей.
Алиментарная гиперхолестеринемия характеризуется повышенным уровнем холестерина в плазме крови вследствие длительного потребления больших количеств пищи, богатой холестерином (куриные желтки, икра, печень, животные жиры и др.). Алиментарная гиперхолестеринемия той или иной степени выраженности характерна для жителей высокоразвитых индустриальных стран. Согласно популяционным исследованиям имеется прямая зависимость между уровнем холестерина в крови и распространенностью ишемической болезни сердца.
В эксперименте на различных животных (кролики, морские свинки, обезьяны) показано, что введение массивных доз холестерина с пищей приводит к резко выраженной гиперхолестеринемии и быстрому развитию атеросклероза. Экспериментальные модели гиперхолестеринемии и атеросклероза, впервые предложенные H. Н. Аничковым и С. С. Халатовым (1913), широко используются в научных исследованиях.
Вторичная гиперхолестеринемия встречается при гипотиреозе (см.), сахарном диабете (см. Диабет сахарный), нефротическом синдроме (см.), подагре (см.) и др. и нередко сопровождается развитием атеросклероза (см. Гиперхолестеринемия).
Выделяют первичную и вторичную гипохолестеринемию. Первичная гипохолестеринемия характерна для наследственного заболевания — абеталипопротеинемии (см.). При этой болезни отмечается почти полное отсутствие в плазме крови липопротеидов низкой плотности (у гомозигот) или значительное их снижение (у гетерозигот). Уровень общего холестерина не превышает 75 мг/ 100 мл. Гомозиготная форма болезни протекает исключительно тяжело. В основе абеталипопротеинемии лежит генетически обусловленное нарушение синтеза апопротеина В — главного белка липопротеидов низкой плотности.
Вторичные гипохолестеринемии наблюдаются при кахексии, гипертиреоидизме, аддисоновой болезни и паренхиматозных заболеваниях печени, при ряде инфекционных болезней и интоксикациях (см. Гипохолестеринемия). При недостаточной активности в плазме крови фермента лецитин — холестерин -ацилтрансферазы, или ЛХАТ (наследственная ЛXАТ-недостаточность), ответственного за этерификацию холестерина плазмы, наблюдается накопление неэтерифицированного холестерина в мембранах эритроцитов и клетках почек, печени, селезенки, костного мозга, роговицы глаза. Резко снижается доля этерифицированного холестерина в плазме крови и одновременно повышается уровень неэтерифицированного холестерина и лецитина. У больных с наследственной ЛXAT-недостаточностыо стенки артерий и капилляров подвержены деструктивным изменениям, что связано с отложением в них липидов. Наиболее тяжелые изменения происходят в сосудах почечных клубочков, что приводит к развитию почечной недостаточности (см.).
Одним из распространенных нарушений холестериновый обмен. является образование желчных камней, основной составной частью которых является холестерин (см. Желчнокаменная болезнь). Образование желчных камней происходит вследствие выкристаллизовывания холестерина при относительно высокой его концентрации в желчи и относительно низкой концентрации в ней желчных кислот и фосфолипидов, обладающих способностью растворять холестерин. Исследования показали, что имеется прямая связь между уровнем холестерина в плазме крови и распространенностью холестероза (см.) и желчнокаменной болезни.
Библиогр.: Климов А. Н, и Н икульчева Н. Г. Липопротеиды, дислипопротеидемии и атеросклероз, Л., 1984; Полякова Э. Д. Пути биосинтеза холестерина в печени и их регуляция, в кн.: Липиды, структура,биосинтез, превращения и функции, под ред. С. Е. Северина, с. 131, М., 1977;она же, Регуляция содержания холестерина в клетке, в кн.: Биохимия липидов и их роль в обмене веществ, под ред.С. Е. Северина, с. 120, М., 1981; Финагин Л. К. Обмен холестерина и его регуляция, Киев, 1980; Lipids and lipidoses, ed. by G. Schettler, B.- Heidelberg, 1967; Sodhi H. S., Kudchod-k a r B. J. a. Mason D. T. Clinical methods in study of cholesterol bolism, Basel a. o., 1979.
A. H. Климов
Источник
Глава 4 Печень и обмен холестерина
Глава 4
Печень и обмен холестерина
Эволюционная роль холестерина заключается в том, что он служит каркасом клеточных мембран человека. Все цитоплазматические мембраны и мембраны органелл клеток млекопитающих и человека в основном состоят из фосфолипидов, гликолипидов и холестерина. Фосфолипиды являются пластичной, жидкой и фунциональной частью мембран, взаимодействуют с включенными в мембрану ферментами и рецепторами (рис. 12). Холестерин образует каркас клеточной мембраны, занимая свободное пространство между нерастворимыми в воде хвостами фосфолипидов и не позволят им изгибаться. Мембраны с низким содержанием холестерина — более гибкие и функционально активные, с высоким содержанием холестерина — более жесткие и инертные. Свободный (не этерифицированный и не связанный с липопротеидами) холестерин может свободно проникать в клеточные мембраны и образовывать эфиры с жирными кислотами, входящими в состав фосфолипидов, нарушая их функциональное состояние. Именно образование этого резервного компартмента холестерина, как и дефицит эссенциальных фосфолипидов, приводит к снижению вязкости и текучести, «старению» клеточных мембран и коррелирует с выраженностью атеросклероза. Таким образом, борьба с излишками холестерина в тканях и циркуляцией свободного холестерина в плазме для человека является эволюционной задачей, которую здоровый и молодой организм успешно решает путем его этерификации, включения в ЛПВП и транспортировки в печень для утилизации.
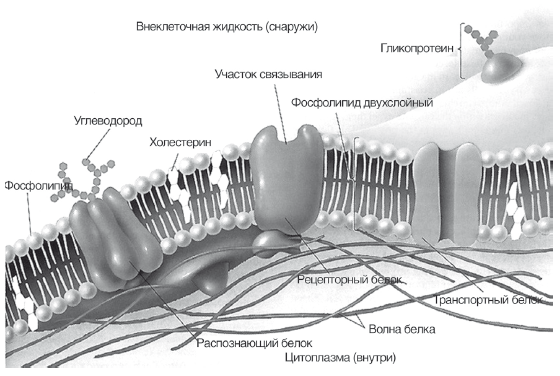
Рис. 12.
Виртуальная модель цитоплазматической мембраны клетки человека
Рис. 13.
Формула холестерина. Холестерин обеспечивает стабильность клеточных мембран в широком интервале температур. Он необходим для выработки витамина D, стероидных и половых гормонов, а также для деятельности синапсов головного мозга и иммунной системы, включая защиту от рака
В 1769 году Пулетье де ла Саль из желчных камней получил плотное белое вещество («жировоск»), обладавшее свойствами жиров. В 1815 году Мишель Шеврёль также выделил это соединение и назвал его холестерином («холе» — желчь, «стерин» — жирный). Однако формулу и химические свойства холестерина установил Антуан Франсуа де Фуркруа. Холестерин и фосфолипиды (98 % их — фосфатидилхолин) составляют липидный комплекс желчи.
В сухом остатке желчи фосфатидилхолин (ФХ) составляет 22 %, а ХС — 4 %. В сутки через каналикулярную мембрану гепатоцита путем активного транспорта переносчиком фосфолипидфлиппазой (MDR3) или в составе фосфолипиднохолестериновых пузырьков и мицелл переносится 1,8-8,2 г ФХ. В кишечнике ФХ желчи расщепляется до лизофосфолипидов и реабсорбируется. Основная функция ФХ заключается в солюбилизации практически нерастворимого в воде ХС путем формирования ядра устойчивых простых (ФХ + холестерин, диаметр до 3 нм) или смешанных мицелл (ФХ + холестерин + желчные кислоты, диаметр 3-6 нм), а также везикул (ФХ + холестерин + желчные кислоты, диаметр 25-130 нм).
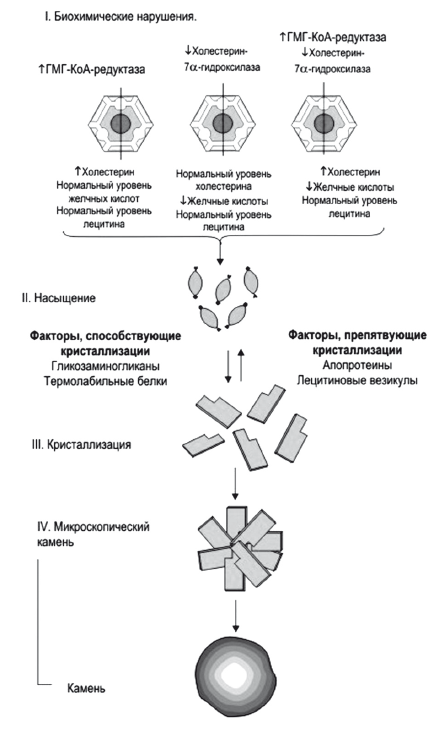
Рис. 14.
Растворимость холестерина в желчи
Потребность в холестерине в организме и печени зависит от активности человека — настройки симпато-адреналовой системы — человеку холестерин жизненно необходим для синтеза прогестерона, стероидных и половых гормонов, деятельности синапсов головного мозга, выработки витамина D. При стрессе и длительном напряжении в организме печень синтезирует много холестерина, который не весь расходуется на синтетические процессы и остается в виде эфиров в цитоплазме гепатоцита. Кроме того, длительное физическое и нервно-психическое напряжение может создать избыток холестерина в тканях преимущественно в форме ЛПНП. Высокое содержание (> 2 %) холестерина в пище также увеличивает фракцию ЛПНП и ЛПВП. При высоком содержании холестерина в пище синтез эндогенного холестерина в печени и других тканях ингибируется по механизму обратной связи.
В норме утилизация избытка холестерина касается только ЛПНП. Захват печенью циркулирующих в плазме ЛПНП — процесс активного транспорта через синусоидальную мембрану гепатоцита. После захвата ЛПНП скавендер-рецепторами гепатоцита они транспортируются в лизосомы, где из них высвобождается свободный холестерин, который используется для синтеза желчных кислот, стероидных гормонов и нейтральных стероидов или секретируется в желчь. Активная экскреция в желчь является основным физиологическим способом выведения избытков холестерина у человека (рис. 15). В сутки у человека образуется 500-1000 мл желчи. При относительно постоянном дебите желчи из организма человека в норме выводится до 1 г продуктов метаболизма холестерина в сутки.
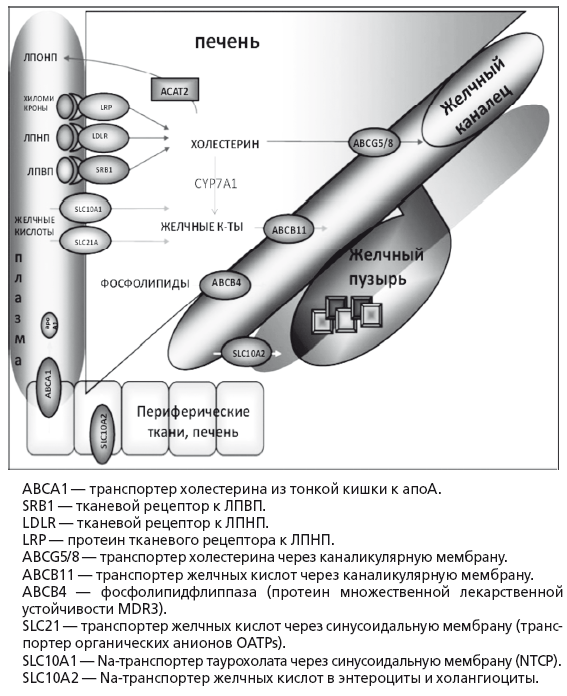
Рис. 15.
Транспорт основных метаболитов в печени (по Marschall HU, Einaon С, 2007)
Приблизительно половина этого количества экскретируется с фекалиями после превращения в желчные кислоты, оставшаяся часть представляет собой нейтральные стероиды. Холестерин секретируется в желчь активно, в желчные канальцы его переносит специальный насос ABCG5/8 (25). Поскольку холестерин не растворим в воде, его удержание в жидкой фракции желчи прямо зависит от концентрации эмульгирующих его желчных кислот и эссенциальных фосфолипидов — преимущественно ФХ, который обеспечивает его растворимость путем образования мицелл. При недостатке желчных кислот образуются более крупные частицы — везикулы, состоящие из лецитина и холестерина. При недостатке ФХ происходит кристаллизация холестерина и образуется желчный камень. Дефицит ФХ в желчи возникает при низком поступлении эссенциальных фосфолипидов или основной функциональной части — незаменимых полиненасыщенных жирных кислот (ПНЖК) в рационе питания. Относительный дефицит эссенциальных фосфолипидов также создается при их высоком потреблении гепатоцитами или другими тканями организма в печени при хронических воспалительных заболеваниях или интоксикациях, в частности, при хронической алкогольной интоксикации. Секреция в желчь холестерина, желчных кислот и ФХ — это энерго- и взаимозависимый, сложный процесс, который может нарушаться при первичном токсическом и аутоиммунном поражении гепатоцитов и холангиоцитов, а также лекарственном или инфекционном холестазе. Увеличение содержания холестерина в желчи форсирует синтез и секрецию в желчь эссенциальных фосфолипидов и базовых желчных кислот, без которых в желчи невозможно поддержание холестерина в растворимой форме и последовательно приводит к увеличению содержания всех этих веществ в тонкой кишке, крови воротной вены и фекалиях.
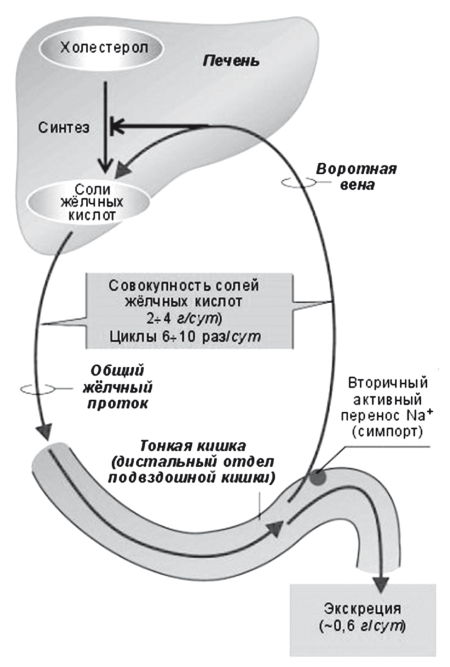
Рис. 16.
Схема энтерогепатической циркуляции желчных кислот
В процессе пассажа химуса по ЖКТ на всем протяжении кишечника всасывается до 90 % «съеденного» холестерина и реабсорбируется около 98 % желчных кислот и около 50 % холестерина, экскретированного с желчью. Оставшееся количество под действием микрофлоры толстой кишки превращается в стеролы, либо выводится с фекалиями, потому что связано с плохо растворимыми желчными кислотами (например, с литохолевой). Энтерогепатическая циркуляция желчных кислот протекает настолько эффективно, что суточная потеря желчных кислот с фекалиями составляет не более 500-1000 мг. Для восполнения потери первичные желчные кислоты — у человека холевая и хенодезоксихолевая кислоты — посредством фермента 7?-гидроксилазы (СУР7А1) постоянно синтезируются из холестерина в эндоплазматическом ретикулуме гепатоцитов, конъюгируются с глицином или таурином и активно секретируются в желчные канальцы (рис. 15). При помощи CYP7a в гепатоцитах из холестерина ежедневно синтезируются около 500 мг новых желчных кислот взамен тех, что были выведены с фекалиями (около 5 % общего пула). Этот метаболический путь является основным не только для синтеза желчных кислот, но и для утилизации избытков холестерина, поскольку приводит к утилизации около 80 % холестерина, циркулирующего в плазме (рис. 17).
Вторичные и третичные желчные кислоты: дезоксихолевая, литохолевая (около 1 % от общего пула желчных кислот) и урсодезоксихо-левая (< 3 % от общего пула желчных кислот) кислоты (УДХК) образуются из первичных желчных кислот под действием бактерий в толстой кишке и также частично реабсорбируются. Этот процесс тонко регулируется по механизму обратной связи — желчные кислоты синтезируются в гепатоците в точном соответствии с их потерей с фекалиями в энтерогепатической циркуляции. Интересно, что синтез желчных кислот более активно протекает в гепатоцитах III зоны печеночной дольки. Напротив, желчные кислоты, реабсорбируемые из кишечника и плазмы, концентрируются в гепатоцитах перипортальной зоны [36].
При увеличении потребности в синтезе нового холестерина в гепатоците активируется ген, кодирующий активность ключевого фермента ГМГ-КоА-редуктазы (рис. 17). Синтез первичных желчных кислот резко уменьшается. Это приводит к уменьшению секреции желчных кислот в желчь и снижению растворимости холестерина в желчи, притом что его концентрация в желчи увеличивается. В общем смысле этот механизм всегда сопутствует прогрессирующему атерогенезу, пожилому возрасту и терапии статинами. Таким образом, неудивительно, что у европейцев с сердечно-сосудистой патологией частота ЖКБ в 1,5 раза превышает среднюю во взрослой популяции, а в возрасте старше 71 года ЖКБ болеют около 14,3 % населения Европы и чаще — мужчины с ССЗ [36]. У представителей некоторых рас и этнических групп возможно также генетически детерминированное увеличение активности ГМГ-КоА-редуктазы: например, известна зависимость частоты ЖКБ от степени экспрессии американо-индейского гена. Накопление холестерина в гепатоцитах также может происходить при DOWN-регуляции CYP7a/
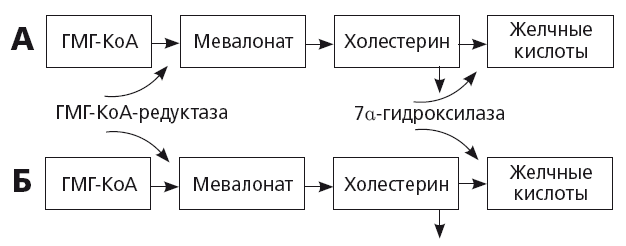
Рис. 17.
Регуляция секреции холестерина и желчных кислот у здоровых людей (А) и пациентов с ожирением и желчнокаменной болезнью (Б) [36]
Установлено, что активность CYP7a увеличивается при уровне холестерина в рационе более 2 %, и происходит это посредством активации ядерных рецепторов LXR, регулирующих экспрессию гена, кодирующего активность этого фермента. Напротив, активная реабсорбция желчных кислот из кишечника тормозит CYP7a и синтез желчных кислот по механизму отрицательной обратной связи и приводит к накоплению холестерина в гепатоцитах. Цель этого тонкого механизма — защита гепатоцитов и холангиоцитов от избыточного накопления желчных кислот, обладающих токсичным детергентным действием.
На первый взгляд, это плохо и тоже должно увеличивать литогенность желчи вследствие снижения секреции желчных кислот. Однако in vivo так не происходит. Изучение молекулярных механизмов ауторегуляции синтеза желчных кислот недавно привело к более тонкому пониманию ключевого регулирующего влияния желчных кислот на метаболизм холестерина, триглицеридов и самих себя. В 1999 году две независимые группы исследователей: в Японии — Makishima М. и соавторы и в Великобритании — Parks D.J. и соавторы почти одновременно опубликовали результаты исследований, впервые показавших, что соли желчных кислот являются прямыми активаторами ядерных рецепторов FXRa (NR1H4), которые регулируют экспрессию генов, участвующих в секреции, транспорте и метаболизме первичных желчных кислот, холестерина и триглицеридов как в гепатоцитах, так и в плазме. Посредством активации FXR желчными кислотами, поступающими из энтерогепатической циркуляции, и происходит подавление синтеза новых желчных кислот в цитозоле гепатоцита (рис. 18).
Активация FXR предотвращает накопление ТГ и ЛПОНП в печени, висцеральной клетчатке и плазме. При этом в печени действительно накапливается холестерин, который в данный момент «не нужен» для синтеза желчных кислот. Однако одновременно стимуляция FXR активирует экскрецию не этерифицированного холестерина в желчь при помощи переносчика ABCG5/8 [60]. Стимуляция FXR также увеличивает скорость захвата желчных кислот из плазмы посредством переносчиков ОАТР (SLC21) и NTCP (SLC10A1) и активирует экскрецию солей желчных кислот в первичные желчные канальцы переносчиком BSEP (АВСВ11). Одновременно стимуляция FXR активирует переносчик MDR3, секретирующий в желчь ФХ.
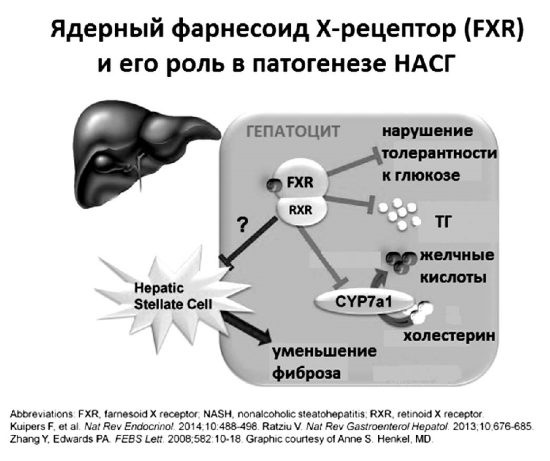
Рис. 18.
Ядерный фарнесоид Х-рецептор (FXR) и его роль в патогенезе НАСГ
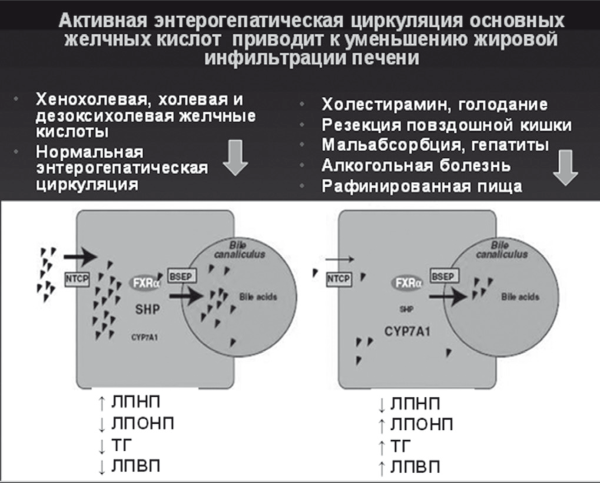
Рис. 19.
Эндокринная функция желчных кислот (модифицировано по S.M. Нouten, М. Watanabe, J. Auwerx, 2006)
Интегрально-активная энтерогепатическая циркуляция обеспечивает включение многокомпонентного механизма защиты гепатоцитов от токсичности желчных кислот при одновременном уменьшении сатурации холестерина в желчи и снижении риска образования желчных камней [60]. Позднее было установлено, что эндогенные желчные кислоты также являются сигнальными молекулами для синергичных FXR рецепторов TGR5 к G-протеину, которые находятся в тонкой кишке и опосредуют секрецию инкретинов. Стимуляция TGR5 желчными кислотами активирует активность щитовидной железы и энергообмен посредством увеличения секреции глюкагонподобных пептидов, которые препятствуют инсулинорезистентности [61]. В эксперименте на мышах оказалось, что добавление холевой кислоты к высококалорийному рациону позволяет предотвратить ожирение и развитие инсулинорезистентности путем увеличения липолиза в бурой жировой клетчатке. Таким образом, высокая реабсорбция желчных кислот при активной физиологической энтерогепатической циркуляции — как это происходит после приема холегенной и богатой жирами пищи — приводит к уменьшению синтеза желчи и накоплению в гепатоците ЛПНП, при одновременном уменьшении содержания ТГ и ЛПВП. Напротив, уменьшение всасывания желчных кислот (например, при голодании, применении секвестрантов, диарее любого происхождения) является сигналом к увеличению синтеза желчных кислот, для чего гепатоцит активно накапливает ТГ, ЛПОНП и ЛПВП. Другими словами, сбалансированный рацион питания, содержащий пищевые жиры и холеретики, служит надежной профилактикой образования желчных камней и развития жировой инфильтрации печени с дислипидемией и инсулинорезистентностью [60, 61].
Источник