Распад гемоглобина до непрямого билирубина
Распад гемоглобина в тканях (образование желчных пигментов)
Продолжительность жизни эритроцитов составляет 120 дней, затем они разрушаются и освобождается гемоглобин. Главными органами, в которых происходят разрушение эритроцитов и распад гемоглобина, являются печень, селезенка и костный мозг, хотя в принципе оба процесса могут происходить и в клетках других органов. Распад гемоглобина в печени начинается с разрыва α-метиновой связи между I и II кольцами порфиринового кольца. Этот процесс катализируется НАДФ-содержащей ок-сидазой и приводит к образованию зеленого пигмента вердоглобина (холеглобина):
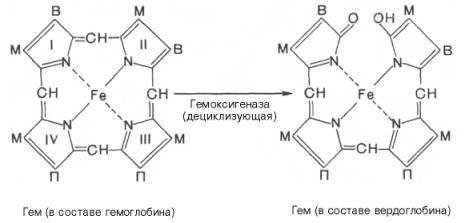
В приведенных структурных формулах здесь и далее в желчных пигментах М — метильная СН3-группа, В — (-СН=СН2) — винильная группа и П — (-СН2-СН2-СООН) — остаток пропионовой кислоты.
Как видно из приведенных формул, в молекуле вердоглобина еще сохраняются атом железа и белковый компонент. Имеются экспериментальные доказательства, что в этом окислительном превращении гемоглобина принимают участие витамин С, ионы Fe2+и другие кофакторы. Дальнейший распад вердоглобина, вероятнее всего, происходит спонтанно с освобождением железа, белка-глобина и образованием одного из желчных пигментов — биливердина. Спонтанный распад сопровождается перераспределением двойных связей и атомов водорода в пиррольных кольцах и метиновых мостиках. Образовавшийся биливердин ферментативным путем восстанавливается в печени в билирубин, являющийся основным желчным пигментом у человека и плотоядных животных:
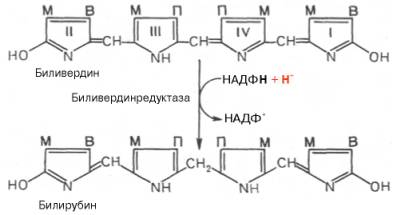
Основное место образования билирубина — печень, селезенка и, по-видимому, эритроциты (при распаде их иногда разрывается одна из метиновых связей в протопорфирине). Образовавшийся во всех этих клетках билирубин поступает в печень, откуда вместе с желчью попадает в желчный пузырь (см. главу 16). Билирубин, образовавшийся в клетках системы макрофагов, называется свободным, или непрямым, билирубином, поскольку вследствие плохой растворимости в воде он легко адсорбируется на белках плазмы крови и для его определения в крови необходимо предварительное осаждение белков спиртом. После этого билирубин вступает во взаимодействие с диазореактивом Эрлиха.
В крови взрослого здорового человека содержится относительно постоянное количество общего билирубина — от 4 до 26 мкмоль/л, в среднем 15 мкмоль/л. Около 75% этого количества приходится на долю непрямого билирубина. Повышение его концентрации в крови до 35 мкмоль/л приводит к желтухе. Более высокий уровень билирубина в крови вызывает явления тяжелого отравления. Непрямой билирубин, поступая с током крови в печень, подвергается обезвреживанию путем связывания с глюку-роновой кислотой. В этом процессе принимают участие особый фермент УДФ-глюкуронилтрансфераза и УДФ-глюкуроновая кислота, являющаяся донором глюкуроновой кислоты. При этом к билирубину присоединяются 2 остатка глюкуроновой кислоты с образованием сравнительно индифферентного комплекса — билирубин-диглюкуронида, хорошо растворимого в воде и дающего прямую реакцию с диазореактивом. В желчи всегда присутствует прямой билирубин. В крови количество прямого и непрямого билирубина, а также соотношение между ними резко меняются при поражениях печени, селезенки, костного мозга, болезнях крови и т.д., поэтому определение содержания обеих форм билирубина в крови имеет существенное значение при дифференциальной диагностике различных форм желтухи. При желчнокаменной болезни в составе желчных камней наряду с основным их компонентом — холестерином всегда обнаруживается непрямой билирубин. Вследствие плохой растворимости в воде он выпадает в осадок в желчном пузыре в виде билирубината кальция, участвующего в формировании камней.
Дальнейшая судьба желчных пигментов, точнее билирубина, связана с их превращениями в кишечнике под действием бактерий. Сначала глю-куроновая кислота отщепляется от комплекса с билирубином и освободившийся билирубин подвергается восстановлению в стеркобилиноген, который выводится из кишечника. В сутки человек выделяет около 300 мг стеркобилиногена. Последний легко окисляется под действием света и воздуха в стеркобилин. Механизм бактериальных превращений билирубина до стеркобилина до конца еще не расшифрован. Имеются данные, что промежуточными продуктами восстановления являются последовательно мезобилирубин и мезобилиноген (уробилиноген). После всасывания небольшая часть мезобилиногена поступает через воротную вену в печень, где подвергается разрушению с образованием моно- и дипиррольных соединений. Кроме того, очень небольшая часть стеркобилиногена после всасывания через систему геморроидальных вен попадает в большой круг кровообращения, минуя печень, и в таком виде выводится с мочой. Однако называть его уробилиногеном не совсем точно (см. главу 18). Суточное содержание стеркобилиногена в моче составляет около 4 мг, и, пожалуй, именно стеркобилиноген является нормальной органической составной частью мочи. Если с мочой выделяется повышенное содержание уробилиногена (точнее, мезобилиногена), то это является свидетельством недостаточности функции печени, например, при печеночной или гемолитической желтухе, когда печень частично теряет способность извлекать этот пигмент из крови воротной вены. Химически уробилиноген (мезо-билиноген) неидентичен стеркобилиногену (уробилиногену) мочи. Исчезновение стеркобилиногена (уробилиногена) из мочи при наличии билирубина и биливердина является свидетельством полного прекращения поступления желчи в кишечник. Такое состояние часто наблюдается при закупорке протока желчного пузыря (желчнокаменная болезнь) или общего желчного протока (желчнокаменная болезнь, раковые поражения поджелудочной железы и др.).
Таким образом, количественный и качественный анализ желчных пигментов в моче может представлять большой клинический интерес.
Источник
Билирубин и его фракции (общий, прямой, непрямой)
[40-120] Билирубин и его фракции (общий, прямой, непрямой)
380 руб.
Анализ, в ходе которого определяется содержание в крови желчных пигментов и их фракций. Они являются метаболитами распада гемоглобина, и их уровень повышается при усиленном разрушении эритроцитов, нарушении функции печени и желчевыводящих путей.
Результаты исследований выдаются с бесплатным комментарием врача.
Метод исследования
Колориметрический фотометрический метод.
Диапазон определения
- Билирубин общий: 2,5 ‑ 550 мкмоль/л.
- Билирубин прямой: 1,5 — 291 мкмоль/л.
Единицы измерения
Мкмоль/л (микромоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную, капиллярную кровь.
Как правильно подготовиться к исследованию?
- Не принимать пищу в течение 12 часов до исследования.
- Исключить физическое и эмоциональное перенапряжение за 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Билирубин — желтый пигмент, который является компонентом желчи и образуется в селезенке и костном мозге при распаде эритроцитов. В норме эритроциты разрушаются через 110-120 дней после выхода из костного мозга. При этом из погибших клеток высвобождается металлопротеин гемоглобин, состоящий из железосодержащей части — гема и белкового компонента — глобина. От гема отщепляется железо, которое повторно используется в качестве необходимого компонента ферментов и других белковых структур, а гемовые белки превращаются в билирубин. Непрямой (неконъюгированный) билирубин с помощью альбуминов доставляется кровью в печень, где благодаря ферменту глюкуронилтрансферазе соединяется с глюкуроновой кислотой и образует прямой (конъюгированный) билирубин. Процесс превращения водонерастворимого билирубина в водорастворимый называется конъюгацией. Связанная фракция пигмента практически не поступает в кровь и в норме экскретируется с желчью. Билирубин в просвете кишечника под действием бактерий кишечника метаболизируется и выводится с калом, придавая ему темную окраску.
Прямой билирубин назван так в связи с методикой лабораторного исследования. Данный водорастворимый пигмент непосредственно взаимодействует с реактивами (диазореактивом Эрлиха), добавленными в пробу крови. Неконъюгированный (непрямой, свободный) билирубин нерастворим в воде, и для его определения необходимы дополнительные реактивы.
В норме за сутки в человеческом организме вырабатывается 250-350 мг билирубина. Выработка более 30-35 мкмоль/л проявляется желтушностью кожных покровов и склер. По механизму развития желтухи и преобладанию фракций билирубина в крови выделяют надпеченочную (гемолитическую), печеночную (паренхиматозную) или подпеченочную (механическую, обтурационную) желтуху.
При повышенном разрушении эритроцитов (гемолизе) или нарушенном захвате печенью желчного пигмента увеличивается содержание билирубина за счет неконъюгированной фракции без повышения уровня связанного пигмента (надпеченочная желтуха). Данная клиническая ситуация наблюдается при некоторых врождённых состояниях, связанных с нарушением конъюгации билирубина, например при синдроме Жильбера.
При наличии преграды на пути выхода желчи в двенадцатиперстную кишку или нарушениях желчевыделения в крови повышается прямой билирубин, что нередко является признаком обтурационной (механической) желтухи. При обструкции желчевыводящих путей прямой билирубин попадает в кровь, а затем и в мочу. Он является единственной фракцией билирубина, способной выделяться почками и окрашивать мочу в темный цвет.
Увеличение билирубина за счет прямой и непрямой фракции указывает на заболевание печени с нарушением захвата и выделения желчных пигментов.
Повышение непрямого билирубина нередко наблюдается у новорождённых в первые 3 дня жизни. Физиологическая желтуха связана с повышенным распадом эритроцитов с фетальным гемоглобином и недостаточной зрелостью ферментных систем печени. При затянувшейся желтухе у новорождённых необходимо исключать гемолитическую болезнь и врождённую патологию печени и желчевыводящих путей. При конфликте групп крови матери и ребенка возникает повышенный распад эритроцитов малыша, что приводит к повышению непрямого билирубина. Неконъюгированный билирубин обладает токсическим действием на клетки нервной системы и может привести к повреждению головного мозга новорождённого. Гемолитическая болезнь новорождённых требует немедленного лечения.
У 1 из 10 тысяч младенцев выявляется атрезия желчевыводящих путей. Данная угрожающая жизни ребенка патология сопровождается повышением билирубина за счет прямой фракции и требует срочного хирургического вмешательства и в некоторых случаях трансплантации печени. У новорождённых также существует вероятность наличия гепатита с повышением как прямого, так и непрямого билирубина.
Изменения уровня фракций билирубина в крови с учетом клинической картины позволяют оценить возможные причины желтухи и определиться с дальнейшей тактикой обследования и лечения.
Для чего используется исследование?
- Для дифференциальной диагностики состояний, сопровождающихся желтушностью кожных покровов и склер.
- Для оценки степени гипербилирубинемии.
- Для дифференциальной диагностики желтух новорождённых и выявления риска развития билирубиновой энцефалопатии.
- Для диагностики гемолитической анемии.
- Для исследования функционального состояния печени.
- Для диагностики нарушений оттока желчи.
- Для наблюдения за пациентом, принимающим препараты с гепатотоксическими и/или гемолитическими свойствами.
- Для динамического наблюдения за пациентами с гемолитической анемией или патологией печени и желчевыводящих путей.
Когда назначается анализ?
- При клинических признаках патологии печени и желчевыводящих путей (желтуха, потемнение мочи, обесцвечивание стула, зуд кожных покровов, тяжесть и боли в правом подреберье).
- При обследовании новорождённых с выраженной и затянувшейся желтухой.
- При подозрении на гемолитическую анемию.
- При обследовании пациентов, регулярно употребляющих алкоголь.
- При использовании лекарственных препаратов с вероятным гепатотоксическим и/или гемолитическим побочным действием.
- При инфицировании вирусами гепатитов.
- При наличии хронических заболеваний печени (цирроз, гепатит, холецистит, желчнокаменная болезнь).
- При комплексном профилактическом обследовании пациента.
Что означают результаты?
Референсные значения
- Общий билирубин
Возраст | Референсные значения |
Меньше 1 дня | 24 — 149 мкмоль/л |
1-3 дня | 58 — 197 мкмоль/л |
3-6 дней | 26 — 205 мкмоль/л |
Больше 6 дней |
- Прямой билирубин: ≤ 5 мкмоль/л.
- Непрямой билирубин — расчетный показатель.
Причины повышения уровня общего билирубина
1. Преимущественно за счет непрямого билирубина (непрямая гипербилирубинемия, связанная с избыточным гемолизом или нарушением захвата и связывания свободного билирубина печенью)
- Аутоиммунный гемолиз.
- Гемолитическая анемия.
- Пернициозная анемия.
- Серповидно-клеточная анемия.
- Врождённый микросфероцитоз.
- Талассемия.
- Эмбриональный тип кроветворения.
- Синдром Жильбера.
- Синдром Криглера — Найяра.
- Постгемотрансфузионная реакция.
- Переливание несовместимых групп крови.
- Малярия.
- Инфаркт миокарда.
- Сепсис.
- Геморрагический инфаркт легкого.
- Кровоизлияние в ткани.
2. Преимущественно за счет прямого билирубина (прямая гипербилирубинемия, связанная с билиарной обструкцией или нарушением выделения связанного билирубина печенью)
- Холедохолитиаз.
- Желчнокаменная болезнь.
- Вирусный гепатит.
- Склерозирующий холангит.
- Билиарный цирроз печени.
- Рак головки поджелудочной железы.
- Синдром Дабина — Джонсона.
- Синдром Ротора.
- Атрезия желчевыводящих путей.
- Алкогольная болезнь печени.
- Беременность.
3. За счет прямого и непрямого билирубина (паренхиматозная желтуха с нарушением захвата билирубина и выделения желчи)
- Вирусный гепатит.
- Алкогольная болезнь печени.
- Цирроз.
- Инфекционный мононуклеоз.
- Токсический гепатит.
- Эхинококкоз печени.
- Абсцессы печени.
- Метастазы или массивные опухоли печени.
Что может влиять на результат?
- Внутривенное введение контрастного препарата за 24 часа до исследования искажает результат.
- Длительное голодание, интенсивные физические нагрузки способствуют повышению уровня билирубина.
- Никотиновая кислота и атазанавир увеличивают содержание непрямого билирубина.
- Лекарственные препараты, повышающие уровень общего билирубина: аллопуринол, анаболические стероиды, противомалярийные препараты, аскорбиновая кислота, азатиоприн, хлорпропамид, холинергические препараты, кодеин, декстран, диуретики, эпинефрин, изопротеренол, леводопа, ингибиторы моноаминооксигеназы, меперидин, метилдопа, метотрексат, морфин, пероральные контрацептивы, феназопиридин, фенотиазиды, хинидин, рифампин, стрептомицин, теофиллин, тирозин, витамин А.
- Лекарственные препараты, снижающие общий билирубин: амикацин, барбитураты, вальпроевая кислота, кофеин, хлорин, цитрат, кортикостероиды, этанол, пенициллин, протеин, противосудорожные, салицилаты, сульфаниламиды, урсодиол, мочевина.
Важные замечания
- Непрямой билирубин обладает нейротоксическим действием у детей в первые 2-4 недели жизни. У детей старших возрастных групп и взрослых гематоэнцефалический барьер обеспечивает достаточную защиту от неконъюгированого билирубина.
- Любое повышение билирубина требует уточнения его причины и обследования пациента.
- Степень повышения билирубина не всегда зависит от тяжести патологического процесса.
Также рекомендуется
- Лабораторное обследование печени
- Лабораторное обследование поджелудочной железы
- Лабораторная диагностика анемий
- Лабораторная диагностика гепатита — биохимические маркеры
- Вирусные гепатиты. Первичная диагностика
- anti-HAV, IgM
- HBsAg
- anti-HCV, антитела
- Общий анализ крови (без лейкоцитарной формулы и СОЭ)
- Общий анализ мочи с микроскопией осадка
- Копрограмма
- Гамма-глютамилтранспептидаза (гамма-ГТ)
- Аланинаминотрансфераза (АЛТ)
- Аспартатаминотрансфераза (АСТ)
- Амилаза общая в сыворотке
- Липаза
- Лактатдегидрогеназа (ЛДГ) общая
- Фосфатаза щелочная общая
- Холестерол общий
- Альбумин в сыворотке
- Альфа-фетопротеин (альфа-ФП)
- Антитела к антигенам аутоиммунных заболеваний печени (антитела к микросомам печени-почек 1 типа (LKM-1), пируват-декарбоксилазному комплексу митохондрий (PDC/М2), цитозольному антигену (LC-1) и растворимому антигену печени (SLA/LP))
- Наследственная гипербилирубинемия. Синдром Жильбера
- УДФ-глюкуронозил трансфераза 1A1 (UGT1A1). Выявление мутации (TA)6/7 (регуляторная область гена)
- Группа крови ABO
- Аллоиммунные антиэритроцитарные антитела (в том числе антирезусные), титр
Кто назначает исследование?
Терапевт, гастроэнтеролог, гепатолог, гематолог, педиатр, хирург, врач общей практики.
Литература
- Назаренко Г. И., Кишкун А. Клиническая оценка результатов лабораторных исследований. — М.: Медицина, 2000. — 157-161.
- Fischbach F.T., Dunning M.B. A Manual of Laboratory and Diagnostic Tests, 8th Ed. Lippincott Williams & Wilkins, 2008: 1344 p.
- Wilson D. McGraw-Hill Manual of Laboratory and Diagnostic Tests 1st Ed. Normal, Illinois, 2007: 666 p.
Источник
42. Гемоглобин. Строение. Синтез и распад гемоглобина. Формы билирубина. Пути выведения билирубина и других желчных пигментов. Желтухи.
Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем — структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
Строение гемоглобина. Гемоглобин представляет собой белок, включающий 4 гемсодержащие белковые субъединицы. Между собой протомеры соединяются гидрофобными, ионными, водородными связями по принципу комплементарности. При этом они взаимодействуют не произвольно, а определенным участком — контактной поверхностью. Этот процесс высокоспецифичен, контакт происходит одновременно в десятках точек по принципу комплементарности. Взаимодействие осуществляют разноименно заряженные группы, гидрофобные участки, неровности на поверхности белка. Белковые субъединицы в нормальном гемоглобине могут быть представлены различными типами полипептидных цепей: α, β, γ, δ, ε, ξ (соответственно, греч. — альфа, бета, гамма, дельта, эпсилон, кси). В состав молекулы гемоглобина входят по две цепи двух разных типов. Гем состоит из иона двухвалентного железа и порфирина. В основе структуры порфиринов находится порфин. Порфин представляет собой четыре пиррольных кольца, связанных между собой метеновыми мостикамиГем соединяется с белковой субъединицей, во-первых, через остаток гистидина координационной связью железа, во-вторых, через гидрофобные связи пиррольных колец и гидрофобных аминокислот. Гем располагается как бы «в кармане» своей цепи и формируется гемсодержащий протомер.
Существует несколько нормальных вариантов гемоглобина:
HbР — примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7-12 неделями жизни,
HbF — фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 недель внутриутробного развития и является основным после 3 месяцев,
HbA — гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 месяца жизни и к рождению составляет 80% всего гемоглобина,
HbA2 — гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи,
HbO2 — оксигемоглобин, образуется при связывании кислорода в легких, в легочных венах его 94-98% от всего количества гемоглобина,
HbCO2 — карбогемоглобин, образуется при связывании углекислого газа в тканях, в венозной крови составляет 15-20% от всего количества гемоглобина.
Патологические формы гемоглобина
HbS — гемоглобин серповидно-клеточной анемии.
MetHb — метгемоглобин, форма гемоглобина, включающая трехвалентный ион железа вместо двухвалентного. Такая форма обычно образуется спонтанно, в этом случае ферментативных мощностей клетки хватает на его восстановление. При использовании сульфаниламидов, употреблении нитрита натрия и нитратов пищевых продуктов, при недостаточности аскорбиновой кислоты ускоряется переход Fe2+ в Fe3+. Образующийся metHb не способен связывать кислород и возникает гипоксия тканей. Для восстановления ионов железа в клинике используют аскорбиновую кислоту и метиленовую синь.
Hb-CO — карбоксигемоглобин, образуется при наличии СО (угарный газ) во вдыхаемом воздухе. Он постоянно присутствует в крови в малых концентрациях, но его доля может колебаться от условий и образа жизни. Угарный газ является активным ингибитором гем-содержащих ферментов, в частности, цитохромоксидазы 4-го комплекса дыхательной цепи.
HbA1С — гликозилированный гемоглобин. Концентрация его нарастает при хронической гипергликемии и является хорошим скрининговым показателем уровня глюкозы крови за длительный период времени.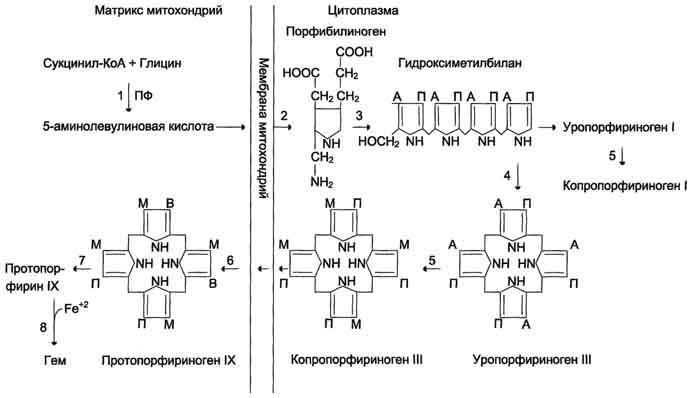
Биосинтез гема. Гем является небелковой частью многих гемопротеинов:
гемоглобин (до 85% общего количества гема организма), локализованный в эритроцитах и клетках костного мозга,
миоглобин скелетных мышц и миокарда (17%),
цитохромы дыхательной цепи и P450, цитохромоксидаза, гомогентизатоксидаза, пероксидаза, миелопероксидаза, каталаза, тиреопероксидаза и т.д. — менее 1%. Синтез гема в основном идет в предшественниках эритроцитов, клетках печени, почек, слизистой кишечника, и в остальных тканях. Первая реакция синтеза с участием δ-аминолевулинат-синтазы происходит в митохондриях. Следующая реакция при участии аминолевулинатдегидратазы (порфобилиноген-синтазы) протекает в цитозоле.Гем синтезируется во всех тканях, но с наибольшей скоростью в костном мозге и печени. В костном мозге гем необходим для синтеза гемоглобина в ретикулоцитах, в гепатоцитах — для образования цитохрома Р450.
Первая реакция синтеза гема — образование 5-аминолевулиновой кислоты из глицина и сук-цинил-КоА идёт в матриксе митохондрий, где в ЦТК образуется один из субстратов этой реакции — сукцинил-КоА. Эту реакцию катализирует пиридоксальзависимый фермент аминолевулинатсинтаза. Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму. В цитоплазме проходят промежуточные этапы синтеза гема: соединение 2 молекул 5-аминолевулиновой кислоты молекулу порфобилиногена, дезаминирование порфобилиногена с образованием гидроксиметилбилана, ферментативное превращение гидроксиметилбилана в молекулу уропор-фобилиногена III, декарбоксилирование последнего с образованием копропорфириногена III. Гидроксиметилбилан может также нефермента-тивно превращаться в уропорфириноген I, который декарбоксилируется в копропорфирино-ген I. Из цитоплазмы копропорфириноген III опять поступает в митохондрии, где проходят заключительные реакции синтеза гема. В результате двух последовательных окислительных реакций копропорфириноген III превращается в протопорфириноген IX, а протопорфириноген IX — в Протопорфирин IX. Фермент феррохела-таза, присоединяя к протопорфирину IX двухвалентное лентное железо, превращает его в гем. Источником железа для синтеза гема служит депонирующий железо белок ферритин. Синтезированный гем, соединяясь с α и β-полипепептидными цепями глобина, образует гемоглобин. Гем регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится. 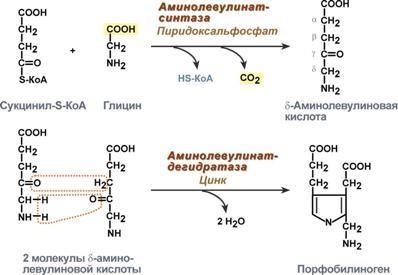
Регуляция синтеза гема
1. Скорость синтеза глобиновых цепей зависит от наличия гема, он ускоряет биосинтез «своих» белков.
2. Основным регуляторным ферментом синтеза гема является аминолевулинатсинтаза.
гем после взаимодействия с молекулой белка-репрессора формирует активный репрессорный комплекс, связывается с ДНК и подавляет транскрипцию, мРНК для фермента не образуется и синтез фермента прекращается. Также имеется отрицательный аллостерический эффект гема на фермент.
с другой стороны, достаточное количество ионов железа оказывает положительный эффект при синтезе молекулы аминолевулинатсинтазы. В клетке имеется особый железосвязывающий белок, который в отсутствии ионов железа обладает сродством к мРНК фермента и блокирует ее трансляцию в рибосоме, т.е. синтез белковой цепи. Ионы железа связываются с этим железосвязывающим белком, образуя с ним неактивный комплекс, что инициирует синтез фермента.
3. Положительным модулятором аминолевулинатсинтазы служит гипоксия тканей, которая в эритропоэтических тканях индуцирует синтез фермента.
4. В печени повышение активности аминолевулинатсинтазы вызывают соединения, усиливающие работу микросомальной системы окисления (жирорастворимые токсины, стероиды) — при этом возрастает потребление гема для образования цитохрома Р450, что снижает внутриклеточную концентрацию свободного гема. В результате происходит дерепрессия синтеза фермента.
Распад. За сутки у человека распадается около 9 г гемопротеинов, в основном это гемоглобин эритроцитов. Эритроциты живут 90-120 дней, после чего лизируются в кровеносном русле или в селезенке. При разрушении эритроцитов в кровяном русле высвобождаемый гемоглобин образует комплекс с белком-переносчиком гаптоглобином (фракция α2-глобулинов крови) и переносится в клетки ретикуло-эндотелиальной системы (РЭС) селезенки (гл образом), печени и костного мозга.
Первая реакция катаболизма гема происходит при участии NADPH-зависимого ферментативного комплекса гемоксигеназы. Ферментная сисгема локализована в мембране ЭР, в области электронтранспортных цепей микросомального окисления. Фермент катализирует расщепление связи между двумя пиррольными кольцами, содержащих винильные остатки, — таким образом, раскрывается структура кольца. В ходе реакции образуются линейный тетрапир-рол — биливердин (пигмент жёлтого цвета) и монооксид углерода (СО), который получается из углерода метениловой группы. Гем индуцирует транскрипцию гена гемоксигеназы, абсолютно специфичной по отношению к тему.
Ионы железа, освободившиеся при распаде гема, могут быть использованы для синтеза новых молекул гемоглобина или для синтеза других железосодержащих белков. Биливердин восстанавливается до билирубина NADPH-зависимым ферментом биливердинредуктазой. Билирубин образуется не только при распаде гемоглобина, не также при катаболизме других гемсодержащю белков, таких как цитохромы и миоглобин. При распаде 1 г гемоглобина образуется 35 мг билирубина, а в сутки у взрослого человека — примерно 250-350 мг билирубина. Дальнейший метаболизм билирубина происходит в печени.
В клетках РЭС гем в составе гемоглобина окисляется молекулярным кислородом. В реакциях последовательно происходит разрыв метинового мостика между 1-м и 2-м пиррольными кольцами гема с их восстановлением, отщеплением железа и белковой части и образованием оранжевого пигмента билирубина. Билирубин — токсичное, жирорастворимое вещество, способное нарушать окислительное фосфорилирование в клетках. Особенно чувствительны к нему клетки нервной ткани. Из клеток ретикуло-эндотелиальной системы билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы, в гораздо меньшем количестве — в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой. Билирубин в комплексе с альбумином называется свободный (неконъюгированный) или непрямой билирубин. Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (лигандина). В клетке протекает реакция связывания билирубина с УДФ-глюкуроновой кислотой, при этом образуются моно- и диглюкурониды. Кроме глюкуроновой кислоты, в реакцию могут вступать сульфаты, фосфаты, глюкозиды. Билирубин-глюкуронид получил название связанный (конъюгированный) или прямой билирубин. После образования билирубин-глюкурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин. Одновременно некоторое количество билирубин-глюкуронидов может попадать (особенно у взрослых) из желчи в кровь по межклеточным щелям. Таким образом, в крови в норме одновременно существуют две формы билирубина: свободный, попадающий сюда из клеток РЭС (около 80% всего количества), и связанный, попадающий из желчных протоков (до 20%). Превращение в кишечнике. В кишечнике билирубин подвергается восстановлению под действием микрофлоры до мезобилирубина и мезобилиногена (уробилиногена). Часть последних всасывается и с током крови вновь попадает в печень, где окисляется до ди- и трипирролов. При этом в здоровом организме в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами. Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена и выделяется из организма, окрашивая кал. Незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда в почки и выделяется с мочой. На воздухе стеркобилиноген и уробилиноген превращаются, соответственно, в стеркобилин и уробилин. Ситуации, при которых в крови накапливается билирубин, в зависимости от причины делятся на три вида: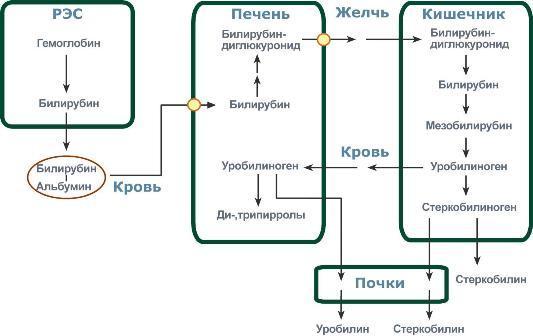
1.Гемолитические — в результате гемолиза при избыточном превращении гемоглобина в билирубин,
2.Печеночно-клеточные — когда печень не в состоянии обезвредить билирубин,
3.Механические — если билирубин не может попасть из печени в кишечник из-за механического перекрытия желчевыводящих путей.
Накопление билирубина в крови свыше 43 мкмоль/л ведет к связыванию его эластическими волокнами кожи и конъюнктивы, что проявляется в виде желтухи. Так как свободный билирубин липофилен, то он легко накапливается в подкожном жире и нервной ткани. Последнее особенно опасно для детей, особенно для новорожденнных.
Гемолитическая или надпеченочная желтуха — ускоренное образование билирубина в результате усиления внутрисосудистого гемолиза. К данному типу желтух относятся гемолитические анемии различного происхождения: врожденный сфероцитоз, серповидно-клеточная анемия, дефицит глюкозо-6-фосфатдегидрогеназы, отравление сульфаниламидами, талассемии, сепсис, лучевая болезнь, несовместимость крови. В данном случае гипербилирубинемия развивается за счет фракции непрямого билирубина. Гепатоциты усиленно переводят непрямой билирубин в связанную форму, секретируют его в желчь, в результате в кале увеличивается содержание стеркобилина, интенсивно его окрашивая. В моче возрастает содержание уробилина, билирубин отсутствует.У новорожденных гемолитическая желтуха может развиться как симптом гемолитической болезни новорожденного.
Механическая или подпеченочная желтуха развивается вследствие снижения оттока желчи при непроходимости желчного протока — желчные камни, новообразования поджелудочной железы, гельминтозы. В результате застоя желчи происходит растяжение желчных капилляров, увеличивается проницаемость их стенок. Не имеющий оттока в кишечник прямой билирубин поступает в кровь, в результате развивается гипербилирубинемия. В тяжелых случаях, вследствие переполнения гепатоцитов прямым билирубином, реакция конъюгации с глюкуроновой кислотой может нарушаться, присоединяется печеночно-клеточная желтуха (см ниже). В результате в крови увеличивается концентрация непрямого билирубина. В моче резко увеличен уровень билирубина (цвет темного пива) и снижено количество уробилина, практически отсутствует стеркобилин кала (серовато-белое окрашивание).
Паренхиматозная (печеночно-клеточная) желтуха — причиной может быть нарушение на всех трех стадиях превращения билирубина в печени: извлечение билирубина из крови печеночными клетками, его конъюгирование и секреция в желчь. Наблюдается при вирусных и других формах гепатитов, циррозе и опухолях печени, жировой дистрофии печени, при отравлении токсическими гепатотропными веществами, при врожденных патологиях. Так как нарушаются все процессы превращения билирубина в печени, гипербилирубинемия развивается за счет обеих фракций, преимущественно прямого билирубина. Концентрация его возрастает из-за нарушения секреции в желчь и увеличения проницаемости мембран клеток печени. Количество непрямого билирубина возрастает за счет функциональной недостаточности гепатоцитов и/или снижения их количества. В моче определяется билирубин (цвет крепкого черного чая), умеренно увеличена концентрация уробилина, уровень стеркобилина кала в норме или снижен.
Гемолитическая болезнь новорожденного.Причины: Несовместимость крови матери и плода по группе или по резус-фактору. Накопление гидрофобной формы билирубина в подкожном жире обуславливает желтушность кожи. Однако реальную опасность представляет накопление билирубина в сером веществе нервной ткани и ядрах ствола с развитием «ядерной желтухи» (билирубиновая энцефалопатия).
Клиническая диагностика: Проявляется сонливостью, плохим сосанием, умственной отсталостью, ригидностью затылочных мышц, тоническими судорогами, тремором конечностей, изменением рефлексов с возможным развитием глухоты и параличей.
Физиологическая (транзиторная) желтуха новорожденных. Причины:относительное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни, связанное с повышенным распадом фетального гемоглобина,абсолютное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни,дефицит лигандина,слабая активность желчевыводящих путей.Клиническая диагностика:окрашивание кожи на 3-4 день после рождения,гемолиза и анемии нет.Симптомы исчезают спустя 1-2 недели после рождения.
Желтуха недоношенных.Причины: относительное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни, связанное с повышенным распадом фетального гемоглобина,абсолютное снижение активности УДФ-глюкуронилтрансферазы в первые дни жизни,дефицит лигандина,слабая активность желчевыводящих путей.Клиническая диагностика:окрашивание кожи,гемолиза и анемии нет. Исчезает спустя 3-4 недели после рождения.
Источник