Роль холестерина в транспорте
Содержание статьи
ОБМЕН, РОЛЬ И ТРАНСПОРТ ХОЛЕСТЕРИНА
В сутки в организме синтезируется около 1 г холестерина (рис.10). Основное место синтеза – печень (до 80%), меньше синтезируется в кишечнике, коже и других тканях. С пищей поступает около 0,4 г холестерина, его источником является только пища животного происхождения. Холестерин необходим для построения всех мембран, в печени из него синтезируются желчные кислоты, в эндокринных железах – стероидные гормоны, в коже – витамин Д.
Рис.10 Холестерин
Сложный путь синтеза холестерина можно поделить на 3 этапа (рис.11). Первый этап заканчивается образованием мевалоновой кислоты. Источником для синтеза холестерина служит ацетил-КоА. Сначала из 3 молекул ацетил-КоА образуется ГМГ-КоА – общий предшественник в синтезе холестерина и кетоновых тел (однако реакции синтеза кетоновых тел происходят в митохондриях печени, а реакции синтеза холестерина – в цитозоле клеток). Затем ГМГ-КоА под действием ГМГ-КоА-редуктазы восстанавливается до мевалоновой кислоты с использованием 2 молекул НАДФН. Эта реакция является регуляторной в синтезе холестерина. Синтез холестерина тормозит сам холестерин, желчные кислоты и гормон голода глюкагон. Усиливается синтез холестерина при стрессе катехоламинами.
На втором этапе синтеза из 6 молекул мевалоновой кислоты образуется углеводород сквален, имеющий линейную структуру и состоящий из 30 атомов углерода.
На третьем этапе синтеза происходит циклизация углеводородной цепи и отщепление 3 атомов углерода, поэтому холестерин содержит 27 углеродных атомов. Холестерин является гидрофобной молекулой, поэтому транспортируется кровью только в составе разных липопротеинов.
Рис. 11 Синтез холестерина
Липопротеины – липид-белковые комплексы, предназначенные для транспорта нерастворимых в водных средах липидов по крови (рис.12). Снаружи липопротеины (ЛП) имеют гидрофильную оболочку, которая состоит из молекул белков и гидрофильных групп фосфолипидов. Внутри ЛП находятся гидрофобные части фосфолипидов, нерастворимые молекулы холестерина, его эфиров, молекулы жиров. ЛП делятся (по плотности и подвижности в электрическом поле) на 4 класса. Плотность ЛП определяется соотношением белков и липидов. Чем больше белка, тем больше плотность и тем меньше размер.
Рис.12. Строение липопротеидов
· 1 класс – хиломикроны (ХМ). Содержат 2% белка и 98% липидов, среди липидов преобладают экзогенные жиры, переносят экзогенные жиры от кишечника к органам и тканям, синтезируются в кишечнике, в крови присутствуют непостоянно – только после переваривания и всасывания жирной пищи.
· 2 класс – ЛП очень низкой плотности (ЛПОНП) или пре-b-ЛП. Белка в них 10%, липидов – 90%, среди липидов преобладают эндогенные жиры, транспортируют эндогенные жиры из печени в жировую ткань. Основное место синтеза – печень, небольшой вклад вносит тонкий кишечник.
· 3 класс – ЛП низкой плотности (ЛПНП) или b-ЛП. Белка в них 22% , липидов – 78%, среди липидов преобладает холестерин. Нагружают клетки холестерином, поэтому их называют атерогенными, т.е. способствующими развитию атеросклероза (АС). Образуются непосредственно в плазме крови из ЛПОНП под действием фермента ЛП-липазы.
· 4 класс ЛП высокой плотности (ЛПВП) или a-ЛП. Белка и липидов содержат по 50%, среди липидов преобладают фосфолипиды и холестерин. Разгружают клетки от избытка холестерина, поэтому являются антиатерогенными, т.е. препятствующими развитию АС. Основное место их синтеза – печень, небольшой вклад вносит тонкий кишечник.
Транспорт холестерина липопротеинами.
Печень является основнымместом синтеза холестерина. Холестерин, синтезированный в печени, упаковывается в ЛПОНП и в их составе секретируется в кровь. В крови на них действует ЛП-липаза, под влиянием которой ЛПОНП переходят в ЛПНП. Таким образом, ЛПНП становятся основной транспортной формой холестерина, в которой он доставляется к тканям. ЛПНП могут попадать в клетки двумя путями: рецепторным и нерецепторным захватом. Большинство клеток на своей поверхности имеют рецепторы к ЛПНП. Образовавшийся комплекс рецептор-ЛПНП эндоцитозом попадает внутрь клетки, где распадается на рецептор и ЛПНП. Из ЛПНП при участии лизосомальных ферментов освобождается холестерин. Этот холестерин используется для обновления мембран, тормозит синтез холестерина данной клеткой, а также, если количество холестерина, поступающего в клетку, превышает ее потребность, то подавляется и синтез рецепторов к ЛПНП.

Это уменьшает поток холестерина из крови в клетки, таким образом, клетки, для которых характерен рецепторный захват ЛПНП, имеют механизм, который ограждает их от избытка холестерина. Для гладкомышечных клеток сосудов и макрофагов характерен нерецепторный захват ЛПНП из крови. В эти клетки ЛПНП, а значит, и холестерин попадают диффузно, то есть, чем их больше в крови, тем больше их попадает в эти клетки. Эти разновидности клеток не имеют механизма, который ограждал бы их от избытка холестерина. В «обратном транспорте холестерина» от клеток участвуют ЛПВП. Они забирают избыток холестерина из клеток и возвращают его обратно в печень. Холестерин выводится с калом в виде желчных кислот, часть холестерина в составе желчи попадает в кишечник и также выводится с калом.
Источник
Холестерол используется как переносчик полиненасыщенных жирных кислот
Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.
Липопротеины высокой плотности
Общая характеристика
- образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника,
- в составе частицы примерно половину занимают белки, еще четверть фосфолипиды, остальное холестерин и ТАГ (50% белка, 25% ФЛ, 13% эфиров ХС и 5% свободного ХС, 7% ТАГ),
- структурным апобелком является апо А1, также содержат апоЕ и апоСII.
Функция
- Транспорт свободного ХС от тканей к печени.
- Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.
Метаболизм
1. Синтезированные в печени частицы (насцентные или первичные ЛПВП) содержат в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в ЛПВП по мере метаболизма в плазме крови.
Новосинтезированные ЛПВП выглядят на электронных микрофотографиях как двухслойные диски из двух монослоев фосфолипидов (таблеткообразная форма). Синтез апоЕ и апоС происходит главным образом в печени, в отличие от апо А-I, образующегося как в печени, так и в тонком кишечнике.
2-3. В плазме крови насцентный ЛПВП сначала превращается в ЛПВП3 (условно его можно назвать «зрелый»). В этом превращении главным является то, что ЛПВП
- забирает от клеточных мембран свободный холестерин при непосредственном контакте или при участии специфических транспортных белков,
- взаимодействуя с мембранами клеток, отдает им часть фосфолипидов из своей оболочки, доставляя таким образом полиеновые жирные кислоты в клетки,
- тесно взаимодействует с ЛПНП и ЛПОНП, получая от них свободный холестерин. В обмен ЛПВП3 отдают эфиры ХС, образованные благодаря переносу жирной кислоты от фосфатидилхолина (ФХ) на холестерин (ЛХАТ-реакция, см п.4).
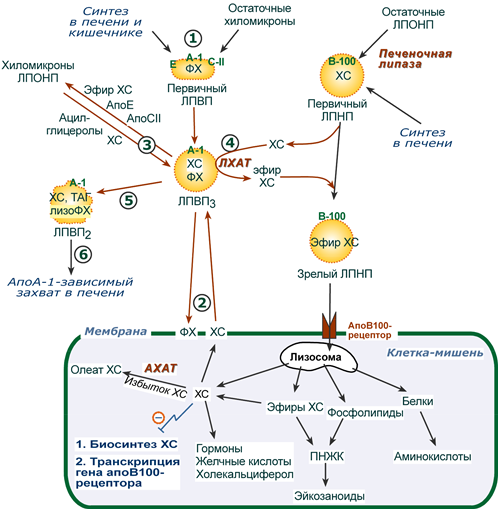
Транспорт холестерола и его эфиров в организме
(цифры соответствуют пунктам метаболизма ЛПВП по тексту)
4. Внутри ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от 2-го положения фосфатидилхолина (из оболочки самого ЛПВП) на получаемый свободный холестерин с образованием лизофосфатидилхолина (лизоФХ) и эфиров ХС. ЛизоФХ остается внутри ЛПВП, эфир холестерина отправляется в ЛПНП.
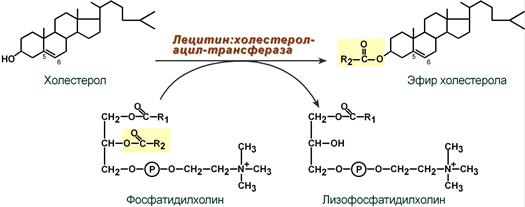
Реакция этерификации холестерола
при участии лецитин:холестерол-ацилтрансферазы
5. В результате первичный ЛПВП постепенно, через зрелую форму ЛПВП3, преобразуется в ЛПВП2 (остаточный, ремнантный). При этом происходят и дополнительные события:
- взаимодействуя с разными формами ЛПОНП и ХМ, ЛПВП получают ацил-глицеролы (МАГ, ДАГ, ТАГ), и обмениваются холестерином и его эфирами,
- ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм.
Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются.
6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается.
Липопротеины низкой плотности
Общая характеристика
- образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП,
- в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов),
- основным апобелком является апоВ-100,
- нормальное содержание в крови 3,2-4,5 г/л,
- самые атерогенные.
Функция
1. Транспорт холестерола в клетки, использующих его
- для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников),
- для превращения в холекальциферол (кожа),
- для образования желчных кислот (печень),
- для выведения в составе желчи (печень).
2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.
Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола.
Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.
Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения.
Также в мембраны всех клеток, как сказано выше (см «Метаболизм ЛПВП»), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП.
Метаболизм
1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и «выталкивание» белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый.
2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами.
3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
- ХС превращается в гормоны или включается в состав мембран,
- излишки мембранного ХС удаляются с помощью ЛПВП,
- принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов.
- при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция),
Синтез олеата холестерола при участии
ацил-SKoA-холестерол-ацилтрансферазы
На количество апоВ-100-рецепторов влияют гормоны:
- инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов,
- глюкокортикоиды уменьшают их количество.
Источник
ТЕМА 8.14. РОЛЬ ЛИПОПРОТЕИНОВ В ТРАНСПОРТЕ


Мы поможем в написании ваших работ!

Мы поможем в написании ваших работ!

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
ХОЛЕСТЕРОЛА
1. В транспорте холестерола между различными органами участвуют все типы липопротеинов, однако их функции различны. Так, холестерол, полученный с пищей (экзогенный холестерол), в клетках кишечника включается в состав хиломикронов (рис. 8.3) как в форме свободного холестерола, так и в виде эфиров, синтезированных в слизистой кишечника под действием фермента АХАТ. В крови зрелые хиломикроны подвергаются действию ЛП-липазы, которая гидролизует содержащиеся в них жиры. Образующиеся в результате хиломикроны остаточные (ремнантные частицы), содержащие холестерол, захватываются гепатоцитами.
2. В печени экзогенный холестерол вместе с эндогенным, синтезированным в этом органе, образуют общий «пул». В печени холестерол вместе с ТАГ упаковывается в ЛПОНП незрелые, в которых главным белком является апопротеин В-100 (рис. 8.37). В формировании ЛПОНП (и хиломикронов) участвует также микросомальный белок, транспортирующий ТАГ, синтезированные в печени и кишечнике, внутрь ЛПОНП и хиломикронов. Дефект этого белка приводит к наследственному заболеванию (а^-липопротеинемии). При этом заболевании нарушается формирование хиломикронов в кишечнике и
ЛПОНП в печени.
3. В крови белки — апоЕ и апоС-II переносятся с поверхности ЛПВП на ЛПОНП; ЛПОНП превращаются таким образом в зрелые и на них начинает действовать ЛП-липаза (рис. 8.37). По мере уменьшения содержания ТАГ в составе ЛПОНП они превращаются в ЛППП; ЛП-липаза продолжает действовать на ЛППП, гидролизуя жиры, и ЛППП превращаются в ЛПНП. На ЛППП действует также печеночная липаза, гидролизуя жиры в их составе. АпоС-II по мере уменьшения содержания жиров в ЛППП переносится обратно на ЛПВП. Содержание холестерола и его эфиров в ЛПНП достигает -50%, и ЛПНП захватываются по механизму эндоцитоза различными клетками, в том числе и гепатоцитами, с помощью ЛПНП-рецепторов, взаимодействующих с апоВ-100 и апо Е.
Рис. 8.37. Транспорт эндогенного холестерола из печени в периферические непеченочные ткани
Холестерол и его эфиры из печени выходят в составе ЛПОНП незрелых. После переноса апо С-II и апо Е с ЛПВП на ЛПОНП они превращаются в зрелые и подвергаются действию ЛП-липазы, находящейся на стенках капилляров. В результате ТАГ гидролизуются и удаляются из ЛПОНП, жирные кислоты и глицерол поступают в различные ткани, а ЛПОНП превращаются в ЛПНП, которые захватываются клетками через специфические ЛПНП рецепторы
4. В «обратном» транспорте холестерола, т.е. выведении избытка холестерола из тканей и крови в печень, главную роль играют ЛПВП. Они синтезируются в виде ЛПВП предшественников в печени и, в небольшом количестве, — в тонкой кишке. Эти липопротеины практически не содержат холестерола, но включают значительное количество фосфолипидов и апопротеинов Е, С-II, А-I, А-II. Незрелые ЛПВП внешне похожи на диски, состоящие из бислоя фосфолипидов, с включенными в него апопротеинами (рис. 8.38).
Рис. 8.38. «Обратный транспорт» холестерола в печень:
Апопротеины: А-I, Е, С-II; ЛХАТ — лецитинхолестеролацилтрансфераза; ЭХ — эфиры холестерола; БПЭХ — белок, переносящий эфиры холестерола; SR-B1 — «скэвенджер» рецепторы; ПЛ — печеночная липаза; ЛПЛ — липопротеинлипаза; АВС1 — АТФсвязывающий кассетный белок 1 (имеет такое название из-за своей структуры). Основные пути поступления избытка эфиров холестерола обратно в печень в составе:
• ремнантных липопротеинов, содержащих апоЕ (хиломикроны остаточные, ЛПНП и ЛППП), которые узнаются ЛПНП-рецепторами;
• из ЛПВП2, подвергающихся действию печеночной липазы на поверхности гепатоцитов, путем переноса эфиров холестерола в гепатоциты через «скэвенджер»-рецепторы
После поступления в кровь ЛПВП сначала выполняют функцию донора апоС-II и апоЕ для липопротеинов, содержащих большое количество ТАГ: ХМ и ЛПОНП. Затем ЛПВП начинают «сбор» избытка холестерола из мембран клеток и других липопротеинов крови.
Для этого к поверхности ЛПВП прикрепляется фермент — ЛХАТ- лецитинхолестеролацилтрансфераза, который активируется белком апоА-I и катализирует реакцию:
Эта реакция происходит при контакте ЛПВП с другими липопротеинами. Образовавшиеся гидрофобные эфиры холестерола погружаются в сердцевину ЛПВП, и частицы приобретают сферическую форму, увеличиваются в размерах и превращаются в ЛПВП3. В переносе холестерола из мембран клеток в ЛПВП участвуют еще несколько белков. ЛПВП могут взаимодействовать с поверхностью клеток с помощью апоА-I или апоЕ. Присутствующий в мембранах клеток белок АВС1 (АТФ-связывающией кассетный белок 1) переносит холестерол с мембраны клетки на ЛПВП, где холестерол подвергается действию ЛХАТ и в виде эфиров холестерола накапливается внутри ЛПВП3.
Далее эфиры холестерола транспортируются с ЛПВП3 на ЛПНП или ЛПОНП с помощью «белка, переносящего эфиры холестерола» (БПЭХ) или путем обмена с ТАГ, которые из ЛПОНП переносятся на ЛПВП. Последние увеличиваются в размере и превращаются в ЛПВП2. Эти частицы подвергаются действию печеночной липазы, гидролизующей ТАГ в ЛПВП2, и они превращаются опять в ЛПВП3.
Поступление эфиров холестерола, собранных с помощью ЛПВП, в печень осуществляется в основном через:
• ЛПНП-рецепторы по механизму эндоцитоза (эти рецепторы узнают апоВ-100 и апоЕ, которые имеются на ЛПНП, ремнантных ХМ и ЛПОНП);
• «скэвенджер»-рецепторы (SR-BI), когда эфиры холестерола переносятся непосредственно с ЛПВП в гепатоциты после действия на ЛПВП печеночной липазы;
• в меньшей степени эфиры холестерола поступают путем эндоцитоза ЛПВП при взаимодействии их апоЕ с рецепторами.
Таким образом, ЛПВП выполняют функцию удаления избытка холестерола из крови и тканей с последующей доставкой его в печень, поэтому ЛПВП оказывают антиатерогенное действие на организм. Благодаря этому свойству врачи часто называют холестерол, находящийся в ЛПВП — «хорошим», а холестерол в ЛПНП «плохим», так как повышение содержания ЛПНП в крови является фактором развития атеросклероза.
ЛПНП и ЛПВП, в отличие от хиломикронов (рис. 8.5), постоянно присутствуют в крови.
5. Избыток холестерола, поступивший в печень, частично превращается в желчные кислоты (рис. 8.36) и удаляется из организма с фекалиями, частично выводится с фекалиями в неизмененном виде. Другими путями из организма выводится лишь небольшое количество холестерола
(рис. 8.31).
Источник
Транспортировка холестерина
Четкая последовательность метаболических процессов в организме крайне важна для адекватного его функционирования. Транспорт холестерина производится в первую очередь с помощью липопротеинов высокой, низкой и очень низкой плотности. Некоторые источники именуют их хиломикронами. Все основные метаболические процессы происходят на мембранах эндоплазматической сети печеночных клеток, а также в митохондриях надпочечниковых желез и в клетках гонад.
Где синтезируется холестерин?
Синтез холестерина происходит в первую очередь в печени. Также его молекулы синтезируются в других органах желудочно-кишечного тракта, мужских и женских половых органах, надпочечниках. Но большее количество холестериновых молекул поступает в организм извне, в составе животной пищи. Транспорт холестерола из места его образования происходит в комплексе с липидными молекулами низкой и очень низкой плотности.
Вернуться к оглавлению
Механизм синтеза
Основные этапы биосинтеза холестерола следующие:
- Молекула стирола присоединяет к себе гидроксильные группы. Это становится возможным благодаря реакции модификации в боковой цепи.
- Происходит окисное гидроксилирование стероидов. Эти процессы катализируются энзимами монооксигеназами.
- Включение в биосинтез цитохрома p450.
- Поступление холестериновых молекул в составе желчных кислот, стероидных гормонов или холекальциферола в циркулирующее русло жидких биологических сред.
Вернуться к оглавлению
Транспортировка холестерина
Излишки холестерола, которые попадают в организм с пищей, транспортируются в жировые ткани.
Экспорт синтезированного в печени холестерола производится только в составе межмолекулярных комплексов. Транспорт холестерина в крови осуществляется липопротеинами высокой, низкой и очень низкой плотности. Эти вещества играют главенствующую роль в развитии атеросклеротических процессов в сосудистом русле. Транспортная форма холестерола является его излишком, который поступил в организм с пищей или образовался под воздействием ферментов микроорганизмов. Липопротеины захватывают его и транспортируют в жировую ткань, где липидная часть комплекса отсоединяется, а сам холестерин переходит в гепатоциты. Далее транспортировка холестерола выполняется в кишечнике, откуда он с фекалиями выводится в форме копростанола.
Вернуться к оглавлению
Как происходит регулировка уровня вещества?
Концентрацию холестериновых молекул обязательно необходимо лимитировать. Это происходит на этапах биосинтеза. Распад холестерина производится с образованием мевалоната из бета-гамма-аминомасляной кислоты. В основе этого механизма лежит принцип негативной обратной связи. Если концентрация молекул холестерола превышает граничные значения, включается его катаболизм. Ингибитором фермента, который лизирует холестериновые молекулы, может выступать как сам холестерол, так и липопротеиды низкой плотности.
Употребление в пищу большого количества холестеринсодержащих продуктов угнетает его синтез в печени. А вот безхолестериновая диета, наоборот, активирует эндогенный синтез холестероловых молекул в гепатоцитах и других органах или тканях.
Вернуться к оглавлению
Выведение холестерина
Переносимый молекулами липопротеидов низкой и очень низкой плотности, холестерол длительно циркулирует в кровеносном русле, последовательно переходя из печени в нуждающиеся ткани. После потребления незатребованные молекулы распадаются до эфиров холестерина. Из организма они выводятся преимущественно с калом, в форме копростанола. Именно их называют желчными кислотами, которые придают каловым массам характерную коричневую окраску. При заболеваниях печени, особенно при обтурации желчевыводящих путей конкрементами, фекалии обесцвечиваются, приобретая песочный оттенок. Это обусловлено тем, что в них снижается концентрация желчных кислот вместе с холестеролом.
Источник