Роль лпнп в транспорте холестерина
Содержание статьи
Холестерол используется как переносчик полиненасыщенных жирных кислот
Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.
Липопротеины высокой плотности
Общая характеристика
- образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника,
- в составе частицы примерно половину занимают белки, еще четверть фосфолипиды, остальное холестерин и ТАГ (50% белка, 25% ФЛ, 13% эфиров ХС и 5% свободного ХС, 7% ТАГ),
- структурным апобелком является апо А1, также содержат апоЕ и апоСII.
Функция
- Транспорт свободного ХС от тканей к печени.
- Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.
Метаболизм
1. Синтезированные в печени частицы (насцентные или первичные ЛПВП) содержат в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в ЛПВП по мере метаболизма в плазме крови.
Новосинтезированные ЛПВП выглядят на электронных микрофотографиях как двухслойные диски из двух монослоев фосфолипидов (таблеткообразная форма). Синтез апоЕ и апоС происходит главным образом в печени, в отличие от апо А-I, образующегося как в печени, так и в тонком кишечнике.
2-3. В плазме крови насцентный ЛПВП сначала превращается в ЛПВП3 (условно его можно назвать «зрелый»). В этом превращении главным является то, что ЛПВП
- забирает от клеточных мембран свободный холестерин при непосредственном контакте или при участии специфических транспортных белков,
- взаимодействуя с мембранами клеток, отдает им часть фосфолипидов из своей оболочки, доставляя таким образом полиеновые жирные кислоты в клетки,
- тесно взаимодействует с ЛПНП и ЛПОНП, получая от них свободный холестерин. В обмен ЛПВП3 отдают эфиры ХС, образованные благодаря переносу жирной кислоты от фосфатидилхолина (ФХ) на холестерин (ЛХАТ-реакция, см п.4).
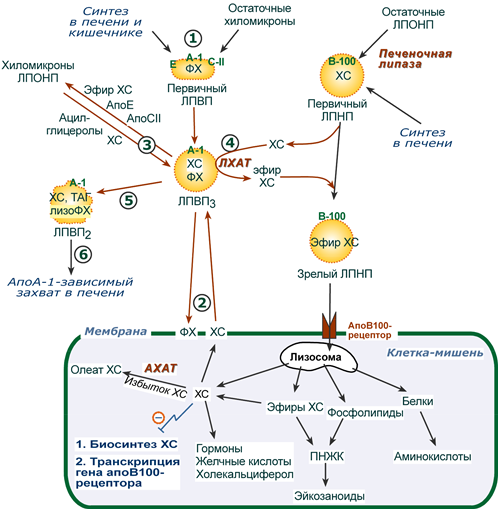
Транспорт холестерола и его эфиров в организме
(цифры соответствуют пунктам метаболизма ЛПВП по тексту)
4. Внутри ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от 2-го положения фосфатидилхолина (из оболочки самого ЛПВП) на получаемый свободный холестерин с образованием лизофосфатидилхолина (лизоФХ) и эфиров ХС. ЛизоФХ остается внутри ЛПВП, эфир холестерина отправляется в ЛПНП.
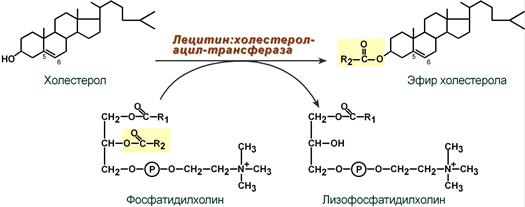
Реакция этерификации холестерола
при участии лецитин:холестерол-ацилтрансферазы
5. В результате первичный ЛПВП постепенно, через зрелую форму ЛПВП3, преобразуется в ЛПВП2 (остаточный, ремнантный). При этом происходят и дополнительные события:
- взаимодействуя с разными формами ЛПОНП и ХМ, ЛПВП получают ацил-глицеролы (МАГ, ДАГ, ТАГ), и обмениваются холестерином и его эфирами,
- ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм.
Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются.
6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается.
Липопротеины низкой плотности
Общая характеристика
- образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП,
- в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов),
- основным апобелком является апоВ-100,
- нормальное содержание в крови 3,2-4,5 г/л,
- самые атерогенные.
Функция
1. Транспорт холестерола в клетки, использующих его
- для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников),
- для превращения в холекальциферол (кожа),
- для образования желчных кислот (печень),
- для выведения в составе желчи (печень).
2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.
Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола.
Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.
Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения.
Также в мембраны всех клеток, как сказано выше (см «Метаболизм ЛПВП»), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП.
Метаболизм
1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и «выталкивание» белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый.
2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами.
3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
- ХС превращается в гормоны или включается в состав мембран,
- излишки мембранного ХС удаляются с помощью ЛПВП,
- принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов.
- при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция),
Синтез олеата холестерола при участии
ацил-SKoA-холестерол-ацилтрансферазы
На количество апоВ-100-рецепторов влияют гормоны:
- инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов,
- глюкокортикоиды уменьшают их количество.
Источник
Регуляция биосинтеза холестерина, транспорт холестерина кровью. 36. Роль ЛПНП и ЛПВП в транспорте холестерина


Устал с поисками информации? Мы тебе поможем!
Холестерол транспортируется кровью только в составе ЛП. ЛП обеспечивают поступление в ткани экзогенного холестерола, определяют потоки холестерола между органами и выведение избытка холестерола из организма.
Транспорт экзогенного холестерола.Холестерол поступает с пищей в количестве 300-500 мг/сут, в основном в виде эфиров. После гидролиза, всасывания в составе мицелл, этерификации в клетках слизистой оболочки кишечника эфиры холестерола и небольшое количество свободного холестерола включаются в состав ХМ и поступают в кровь. После удаления жиров из ХМ под действием ЛП-липазы холестерол в составе остаточных ХМ доставляется в печень. Остаточные ХМ взаимодействуют с рецепторами клеток печени и захватываются по механизму эндоцитоза. Затем ферменты лизосом гидролизуют компоненты остаточных ХМ, и в результате образуется свободный холестерол. Экзогенный холестерол, поступающий таким образом в клетки печени, может ингибировать синтез эндогенного холестерола, замедляя скорость синтеза ГМГ-КоА-редуктазы.
Транспорт эндогенного холестерола в составе ЛПОНП (пре-β-липопротеинов).Печень — основное место синтеза холестерола. Эндогенный холестерол, синтезированный из исходного субстрата ацетил-КоА, и экзогенный, поступивший в составе остаточных ХМ, образуют в печени общий фонд холестерола. В гепатоцитах триацилглицеролы и холестерол упаковываются в ЛПОНП. В их состав входят, кроме того, апопротеин В-100 и фоефолипиды. ЛПОНП сек-ретируются в кровь, где получают от ЛПВП апопротеины Е и С-IIВ крови на ЛПОНП действует ЛП-липаза, которая, как и в ХМ, активируется апоС-II гидролизует жиры до глицерола и жирных кислот. По мере уменьшения количества ТАГ в составе ЛПОНП они превращаются в ЛППП. Когда количество жиров в ЛППП уменьшается, апопротеины С-II реносятся обратно на ЛПВП. Содержание холестерола и его эфиров в ЛППП достигает 45%; часть этих липопротеинов захватывается клетками печени через рецепторы ЛПНП, которые взаимодействуют и с апоЕ и с апоВ-100.
Транспорт холестерола в составе ЛПНП. Рецепторы ЛПНП.На ЛППП, оставшиеся в крови, продолжает действовать ЛП-липаза, и они превращаются в ЛПНП, содержащие до 55% холестерола и его эфиров. Апопротеины Е и С-II реносятся обратно в ЛПВП. Поэтому основным апопротеином в ЛПНП служит апоВ-100. Апопротеин В-100 взаимодействует с рецепторами ЛПНП и таким образом определяет дальнейший путь холестерола. ЛПНП — основная транспортная форма холестерола, в которой он доставляется в ткани. Около 70% холестерола и его эфиров в крови находится в составе ЛПНП. Из крови ЛПНП поступают в печень (до 75%) и другие ткани, которые имеют на своей поверхности рецепторы ЛПНП. Рецептор ЛПНП — сложный белок, состоящий из 5 доменов и содержащий углеводную часть. Рецепторы ЛПНП синтезируются в ЭР и аппарате Гольджи, а затем экспонируются на поверхности клетки, в специальных углублениях, выстланных белком клатрином. Эти углубления называют окаймлёнными ямками. Выступающий на поверхность N-концевой домен рецептора взаимодействует с белками апоВ-100 и апоЕ; поэтому он может связывать не только ЛПНП, но и ЛППП, ЛПОНП, остаточные ХМ, содержащие эти апопротеины. Клетки тканей содержат большое количество рецепторов ЛПНП на своей поверхности: например, на одной клетке фибробласта имеется от 20 000 до 50 000 рецепторов. Из этого следует, что холестерол поступает в клетки из крови в основном в составе ЛПНП. Если количество холестерола, поступающего в клетку, превышает её потребность, то синтез рецепторов ЛПНП подавляется, что уменьшает поток холестерола из крови в клетки. При снижении концентрации свободного холестерола в клетке, наоборот, активируется синтез ГМГ-КоА-редуктазы и рецепторов ЛПНП. В регуляции синтеза рецепторов ЛПНП участвуют гормоны: инсулин и трийодтиронин (Т3), полрвые гормоны. Они увеличивают образование рецепторов ЛПНП, а глюкокортикоиды (в основном кортизол) уменьшают. Эффекты инсулина и Т3, вероятно, могут объяснить механизм гиперхолестеролемии и увеличение риска атеросклероза при сахарном диабете или гипотиреозе.
Роль ЛПВП в обмене холестерола.ЛПВП выполняют 2 основные функции: они поставляют апопротеины другим ЛП в крови и участвуют в так называемом «обратном транспорте холестерола». ЛПВП синтезируются в печени и в небольшом количестве в тонком кишечнике в виде «незрелых липопротеинов» — предшественников ЛПВП. Они имеют дисковидную форму, небольшой размер и содержат высокий процент белков и фосфолипидов. В печени в ЛПВП включаются апопротеины А, Е, С-II, фермент ЛХАТ. В крови апоС-II и апоЕ переносятся с ЛПВП на ХМ и ЛПОНП. Предшественники ЛПВП пракгически не содержат холестерола и ТАГ и в крови обогащаются холестеролом, получая его из других ЛП и мембран клеток. Для переноса холестерола в ЛПВП существует сложный механизм. На поверхности ЛПВП находится фермент ЛХАТ — лецитишхолестерол-ацилтрансфераза. Этот фермент превращает холестерол, имеющий гидроксильную группу, выступающую на поверхность липопротеинов или мембран клеток, в эфиры холестерола. Радикал жирной кислоты переносится от фосфатидилхолита (лецитина) на гидроксильную группу холестерола. Реакция активируется апопротеином A-I, входящим в состав ЛПВП. Гидрофобная молекула, эфира холестерола перемещается внутрь ЛПВП. Таким образом, частицы ЛПВП обогащаются эфирами холестерола. ЛПВП увеличиваются в размерах, из дисковидных небольших частиц превращаются в частицы сферической формы, которые называют ЛПВП3, или «зрелые ЛПВП». ЛПВП3 частично обменивают эфиры холестерола на триацилглицеролы, содержащиеся в ЛПОНП, ЛППП и ХМ. В этом переносе участвует «белок, переносящий эфиры холестерина»(он также называется aпoD). Таким образом, часть эфиров холестерола переносится на ЛПОНП, ЛППП, а ЛПВП3 за счёт накопления триацилглицеролов увеличиваются в размерах и превращаются в ЛПВП2. ЛПОНП под действием ЛП-липазы превращаются сначала в ЛППП, а затем в ЛПНП. ЛПНП и ЛППП захватываются клетками через рецепторы ЛПНП. Таким образом, холестерол из всех тканей возвращается в печень в основном в составе ЛПНП, но в этом участвуют также ЛППП и ЛПВП2. Практически весь холестерол, который должен быть выведен из организма, поступает в печень и уже из этого органа выделяется в виде производных с фекалиями. Путь возвращения холестерола в печень называют «обратным транспортом» холестерола.
37. Превращение холестерина в желчные кислоты, выведение из организма холестерина и желчных кислот.

Жёлчные кислоты синтезируются в печени из холестерола. Часть жёлчных кислот в печени подвергается реакции конъюгации — соединения с гидрофильными молекулами (глицином и таурином). Жёлчные кислоты обеспечивают эмульгирование жиров, всасывание продуктов их переваривания и некоторых гидрофобных веществ, поступающих с пищей, например жирорастворимых витаминов и холестерола. Жёлчные кислоты также всасываются, через юротную вену попадают опять в печень и многократно используются для эмульгирования жиров. Этот путь называют энтерогепатической циркуляцией жёлчных кислот.
Синтез жёлчных кислот.В организме за сутки синтезируется 200- 600 мг жёлчных кислот. Первая реакция синтеза – образование 7-α-гидроксихолестерола — является регуляторной. Фермент 7-α-гидроксилаза, катализирующий эту реакцию, ингибируется конечным продуктом — жёлчными кислотами. 7-α-Гидроксилаза представляет собой одну из форм цитохрома Р450 и использует кислород как один из субстратов. Один атом кислорода из О2 включается в гидроксильную группу в положении 7, а другой восстанавливается до воды. Последующие реакции синтеза приводят к формированию 2 видов жёлчных кислот: холевой и хенодезоксихолевой, которые называют «первичными жёлчными кислотами».
Выведение холестерола из организма.Структурная основа холестерола — кольца циклопентанпергидрофенантрена — не может быть расщеплена до СО2 и воды, как другие органические компоненты, поступающие с пищей или синтезированные в организме. Поэтому основное количество холестерола выводится в виде жёлчных кислот.
Некоторое количество жёлчных кислот выделяется в неизменённом виде, а часть подвергается действию ферментов бактерий в кишечнике. Продукты их разрушения (в основном, вторичные жёлчные кислоты) выводятся из организма.
Часть молекул холестерола в кишечнике под действием ферментов бактерий восстанавливается по двойной связи в кольце В, в результате чего образуютря 2 типа молекул — холестанол и копростанол, выводимые с фекалиями. В сутки из организма выводится от 1,0 г до 1,3 г холестерола, основная часть удаляется с фекалиями,
Дата добавления: 2016-07-29; Мы поможем в написании ваших работ!; просмотров: 2744 | Нарушение авторских прав
| Изречения для студентов
Читайте также:
Поиск на сайте:
Рекомендуемый контект:

© 2015-2021 lektsii.org — Контакты — Последнее добавление
Источник
иломикроны. ЛПОНП. ЛПНП. ЛПВП.
Хиломикроны. ЛПОНП. ЛПНП. ЛПВП.Хиломикроны (ХМ) — крупные шаровидные и легкие образования, содержащие в основном ТГ (более 90 %) и в меньшей степени эфиры ХС, поступающие с пищей и окруженные тонкой белковой оболочкой. ХМ синтезируются в тонком кишечнике, служат для переноса ТГ в первые часы после приема пищи: транспортируют пищевые жиры и ХС из кишечника в печень и периферические ткани. Уровень ХМ в крови резко увеличивается после употребления жирной пищи. Под влиянием липопротеидлипазы происходит гидролиз ТГ: из ХМ высвобождаются свободные жирные кислоты, которые, окисляясь, могут использоваться для энергетических процессов в мышцах и жировых клетках. При избыточном поступлении свободные жирные кислоты включаются в жировую ткань, где, эстерифицируясь, снова превращаются в ТГ и депонируются. ХМ, освободившиеся под влиянием липопротеидлипазы от значительного количества ТГ, образуют остаточные ХМ. Далее они попадают в печень, где захватываются гепатоцитами и разрушаются с высвобождением ХС. Параллельно печень секрети-руетЛПОНП. ЛПОНП (на их долю приходится только 15% ОХС и практически все ТГ) — главная транспортная форма эндогенных ТГ. Они доставляются к функционирующим клеткам, в жировые депо. Крупные ЛП (ЛПОНП и ХМ) имеют настолько большие размеры, что не могут проникать в стенку артерии и не являются атерогенными, но их избыток способен вызвать развитие острого панкреатита. Половина выделяемых ЛПОНП обратно захватывается печенью, а другая часть (после гидролиза ТГ под действием липопротеидлипазы) превращается в ЛП промежуточной плотности. Последние после снижения в них концентрации ТГ уплотняются и превращаются в атерогенные ЛПНП (конечный продукт этого метаболического каскада). Они — главный переносчик ХС (содержат большую часть, до 2/3, ХС плазмы крови) от места синтеза к органам-потребителям (служат там для синтеза мембран клеток, провитамина D и стероидных гормонов). В лизосомах ЛПНП распадаются и свободный ХС выходит в цитоплазму.
Более 2/3 ЛПНП попадает внутрь клетки при помощи «узнающих их» клеточных рецепторов, остальная часть — нерецепторным путем. Количество поверхностных рецепторов-«челноков», связывающих ЛПНП, меняется в зависимости от концентрации последних в крови, содержания в них ХС и потребностей клетки в ХС. Так, если в гепатоцитах (или других тканях организма) повышается потребность в ХС, то в клетках компенсаторно возрастает активность рецепторов к ЛПНП. Через них увеличивается утилизация ХС (в первую очередь, из ЛПНП), что приводит к уменьшению содержания ХСЛПНП и снижению транспорта ХС в стенку артерии (и интенсивности формирования атеросклеротических бляшек). Когда же ткани не нуждаются в дополнительных количествах ХС, то концентрация ЛПНП растет и активность рецепторов к ЛПНП снижается. Все это повышает вероятность переноса в артериальную стенку ЛПНП, где они легко модифицируются (окисление, гликация и др.), оставаясь в ней и оказывая проатерогенный эффект. Так, ЛПНП благоприятствуют коагуляции (усиливая выделения тканевого фактора — тромбопластина), дисфункции эндотелия и развитию в нем воспалительной реакции. Мелкие и плотные ЛПНП легко проникают в стенку артерии и задерживаются в ней, в последующем окисляясь свободными радикалами. Контактируя с макрофагами, ЛПНП дают толчок к развитию атеросклероза (и ИБС в последующем). Чем ниже концентрация ХСЛПНП, тем меньше риск развития атеросклероза. Поэтому именно уровень ХСЛПНП — главная мишень липиднормализующей терапии. Так, если ЛС стимулировать чувствительность и активность рецепторов ЛПНП, то это будет оказывать антиатерогенное действие, способствуя уменьшению концентрации ХСЛПНП. Наследственные факторы в половине случаев определяют вариабельность ХСЛПНП (их размеры и плотность). ЛПВП (синтезируются в печени и тонком кишечнике) — самые плотные и мелкие, по сравнению с ЛПНП содержат больше белка и фосфолипидов и меньше ХС. ЛПВП легко проникают в стенку сосуда и также легко ее покидают, не вызывая развитие атеросклероза. В норме удельный вес ХСЛПВП составляет около 20% в структуре ЛП. Основная функция ЛПВП — защита артерий от развития атеросклероза, обратный транспорт ХС из периферических тканей (удаляют его избыток из стенок сосудов. ГМК, органов и тканей), перевод ХС в другие ЛП или транспортировка в печень для дальнейшего катаболизма — последующего удаления из организма с желчью и калом (по желчевыводящим путям и кишечнику). Частицы ЛПВП также обладают и другими защитными эффектами: содержат антиоксиданты (тормозящие окисление ХСЛПНП), стабилизируют атеросклеротическую бляшку, снижают агрегацию тромбоцитов (и вероятность последующих тромбозов) и несколько повышают активность фибринолиза. Повышение уровня ХСЛПВП -вторая по значимости цель лечения дислипидемии. Чем выше уровень ЛПВП в крови и больше ХСЛПВП, тем меньше вероятность развития атеросклероза и больше возможность регресса атеросклеротических бляшек. Так, рост ХСЛПВП только на 0,03 ммоль/л коррелирует со снижением относительного риска развития ИБС на 3%. Низкому уровню ХСЛПВП могут благоприятствовать мужской пол, атерогенный образ жизни (курение, ожирение, гиподинамия, повышенное потребление углеводов), СД и высокий уровень ТГ. При атеросклерозе имеются дефекты липолиза хиломикронов и ЛПОНП, нарушения в системе обратного транспорта ХСЛПВП и метаболизма ЛП в плазме крови. С одной стороны, увеличение уровня ЛПНП (и содержания в них ХС), а с другой — понижение концентрации ЛПВП благоприятствуют формированию атеросклеротических бляшек и развитию ИБС. Показана прямая связь между повышением уровня ХСЛПНП и заболеваемостью ИБС. При очень высоких уровнях ХС ИБС может развиваться уже у молодых людей (даже если нет других ФР). Лечение, направленное на снижение уровня ХСЛПНП и повышение ХСЛПВП, может замедлить развитие ИБС. Каждая из нижеприводимых теорий атеросклероза имеет определенный базис (научное обоснование и клинические подтверждения), но ни одна из них не является всеобъемлющей и не может объяснить все механизмы формирования атеросклероза. — Также рекомендуем «Липидно-инфильтративная теория атеросклероза. Гиперлипидемии. Классификация гиперлипидемий.» Оглавление темы «Атеросклероз Причины атеросклероза.»: |
Источник
