Синтез липидов холестерина происходит в
Содержание статьи
Процесс синтеза липидов
Профилактика атеросклероза, как и терапия заболевания, напрямую связаны с контролем уровня липидных структур в организме. Особое внимание уделяется холестерину (ХС), молекула которого представляет собой липофильный спирт. Отсюда происходит непривычное на бытовом уровне, но химически корректное название вещества – холестерол. Именно окисление неиспользованных организмом липидов свободными радикалами – первый этап в последовательности формирования атеросклеротических бляшек. С другой стороны, соединения липидных структур с протеинами, создают биологические комплексы, способные очищать сосуды. Это липопротеины высокой плотности – ЛПВП. Таким образом, синтез и биосинтез липидов важен применительно к общему здоровью человека. Процесс непосредственно влияет на уровень холестерина в организме.

Что включает класс липидов
Категория объединяет жиры и подобные им вещества. На молекулярном уровне, липид формируется на двух базовых элементах: спирт и жирная кислота. Также допускается вхождение дополнительных компонентов. Подобные структуры относят к классу сложных липидов. Наибольший интерес, с точки зрения профилактики атеросклероза, привлекают следующие представители этого класса:
- Жирные спирты, а именно холестерин.
- Триглицериды.
Определенного внимания заслуживали бы жирные кислоты (ЖК), в частности полиненасыщенные – Омега-3. Вещество способствует снижению ХС. Однако организмом человека их синтез не осуществляется.
Общий принцип биосинтеза липидов
Образование ЖК и их производных начинается с цитоплазмы. Вторая часть биосинтеза – удлинение молекулярной цепи также продолжается в клетке, однако «производственная мастерская смещается» внутрь митохондрии. На каждом этапе, соединение обогащается двумя атомами C, что напоминает процесс бета-окисления, только в его обратной интерпретации.
Говоря более развернуто, в цитоплазме непосредственно и происходит синтез, например пальмитиновой кислоты. Митохондрии же, используют уже готовый «полуфабрикат», для производства полноценных жирных кислот, состоящих из 18-и и более атомов углерода. Выполнить весь биосинтез самостоятельно от «А» до «Я», митохондрии не в состоянии. Причина банальна – «низкий уровень квалификации». Возвращаясь к технической терминологии, митохондрии обладают очень низкой способностью включать меченые уксусные кислоты в длинную цепь липидных структур.

Базовый внемитохондриальный биосинтез ЖК, напротив, не имеет общих пересечений с процессом их окисления. Его механизм, требует трех компонент:
- ацетил-КоА – первичный метаболит;
- CO2 – тут без комментариев, вещество общеизвестное;
- ионов бикарбоната – HCO3-.
Метаболит представляет собой строительный фундамент. Изначально ацетил-КоА образуется именно в митохондрии. Его синтез – следствие процесса окислительного декарбоксилирования. Просочиться напрямую в цитоплазму, соединение не может в силу непроницаемости для него митохондриальной мембраны. Удается осуществить проникновение путем обходного маневра:
- Митохондриальный метаболит производит цитрат, посредством взаимодействия с оксалоацетатом.
- Для синтезированного цитрата митохондриальная мембрана прозрачна. Поэтому его молекулы с легкостью пробиваются в цитоплазму.
- Далее происходит обратная трансформация. Едва преодолев мембрану, цитрат расщепляется на исходные компоненты – ацетил-КоА и оксалоацетат.
Таким образом, метаболит передается от митохондрии. В цитоплазме непосредственного получения соединения не происходит. Альтернативный вариант переноса ацетил-КоА возможен при участии карнитина. Однако, в процессе синтеза ЖК, – это своеобразный «бронепоезд, стоящий на запасном пути». Данный канал используется значительно реже.

Заключительный этап биосинтеза
Оказавшись в цитоплазме метаболит готов к производству прекурсора ЖК – малонил-КоА. Для этого ацетил-КоА и требуется двуокись углерода. Катализатором процесс выступает фермент ацетил-КоА-карбоксилазы. Биосинтез распределяется на два периода:
- Карбоксилирование биотин-энзима. Протекает в присутствии CO2 и АТФ.
- Перенос карбоксильной группы на метаболит.
Результирующий малонил-КоА в дальнейшем быстро трансформируется в ЖК. Процесс происходит с участием определенной ферментной системы. Фактически, это комплекс взаимосвязанных ферментов. Он именуется синтетаза жирных кислот, имеет 6 различных ферментов и связующий элемент – ацилпереносящий белок (осуществляют роль, аналогичную КоА).
Разобравшись с биосинтезом липидов на общем уровне, самое время перейти к конкретным примерам.

Биосинтез триглицеридов
Фундаментальными кирпичиками процесса выступают глицерин и ЖК. Изначально формируется промежуточный продукт – глицерол-3-фосфат. Это характерно для процессов биосинтеза, происходящих в почках и стенках кишечника. Клетки органов отличаются гиперактивностью фермента глицеролкиназы, чего нельзя сказать о мышечной и жировой ткани. Тут вещество формируется при помощи гликолиза – окисления глюкозы.
Эффект особенно проявляется при истощении. Вследствие этого, образуется недостаток глюкозы, что приводит к резкому снижению производства глицерол-3-фосфата. Как результат свободные ЖК не используются на ресинтез липидов, просто покидая ткань.
Еще одним источником промежуточного синтеза глицерол-3-фосфат выступает печень. Орган может производить вещество обоими способами, с использованием как глицерина, так и глюкозы, в качестве базового соединения. Впрочем, для синтеза глицерол-3-фосфат главное, что события произошли, поскольку в дальнейшем соединение ацилируется. То есть происходит процесс введения RCO- остатка при помощи молекул ЖК (КоА производные).
Это приводит к синтезу фосфатидной кислоты. В дальнейшем от полученного соединения отщепляется остаток фосфорной кислоты. Реакция дефосфорилирования протекает с участием фосфатидатфосфатазы. Ее продуктом выступает 1,2-диглицерид. До получения триглицерида остается единственный шаг. Он состоит в этерификации. Кислотой выступает 1,2-диглицерид, заместителем спирта – фермент ацил-КоА.

Биосинтез холестерина
Ферментативный процесс образования ХС – достаточно сложная «многоходовая комбинация», насчитывающая более 35 энзиматических реакций. Очевидно, что охватить подобный объем преобразований не под силу даже Остапу Бендеру. Поэтому проще рассмотреть базовые стадии биосинтеза холестерола:
- Получение мевалоновой кислоты. Происходит в эукариоте – домене живых организмов. Требует три молекулы активного ацетата.
- Формирование сквалена. Прекурсором выступает ранее произведенная мевалоновая кислота. Изначально соединение трансформируется в активный изопреноид, из 6 молекул которого и образуется сквален.
- Синтез холестерина. Процесс осуществляется циклизацией сквалена. Синтезируется своеобразный прекурсор – ланостерин, переход которого в ХС все еще находится под изучением.
Первоначально биосинтез инициируется формированием ацетоацетил-КоА. Далее, структура подвергается конденсации с 3-ей молекулой активного ацетата. Полученное производное вещество вступает в реакцию восстановления, что и приводит к формированию мевалоната.
Следующий шаг в биосинтезе ХС – превращение мевалоната в сквален. Изначально, соединение подвергается переносу остатка фосфорной кислоты при помощи фермента АТФ. Продуктом реакции выступает 5′-пирофосфорный эфир. Впрочем, соединение не долговечно. Оно практически моментально трансформируется, в эфир мевалоната. Цепочка последующих преобразований достаточно запутана, поэтому проще ограничиться фактом. Результатом этих процессов становится образование сквалена. Реакция циклизации соединения приводит к формированию ланостерина, с последующим биосинтезом холестерола.
Остается добавить, что преимущественно процесс протекает в печени. Поэтому дисфункции органа, способны вызывать нарушения липидного баланса. При нормальной работе, печень производит ежесуточную норму холестерина, с учетом вещества, поступающего с продуктами. Этот факт еще раз опровергает распространенное заблуждение о вреде пищи с высоким содержанием холестерина. Здоровая печень, способна самостоятельно контролировать уровень вещества.
Источник
Синтез холестерола должен быть согласован с его выведением
Синтез холестерола в организме составляет примерно 0,5-0,8 г/сут, примерно 50% образуется в печени, около 15% в кишечнике. Все клетки организма способны синтезировать холестерол. Поступление с пищей составляет около 0,4 г/сут.
Единственным реальным способом выведения холестерола является желчь – до 1 г/сут.
Биосинтез холестерола
Биосинтез холестерола происходит в эндоплазматическом ретикулуме. Источником всех атомов углерода в молекуле является ацетил-SКоА, поступающий сюда из митохондрий в составе цитрата, также как при синтезе жирных кислот. При биосинтезе холестерола затрачивается 18 молекул АТФ и 13 молекул НАДФН.
Образование холестерола идет более чем в 30 реакциях, которые можно сгруппировать в несколько этапов.
1. Синтез мевалоновой кислоты.
Первые две реакции синтеза совпадают с реакциями кетогенеза, но после синтеза 3-гидрокси-3-метилглутарил-SКоА вступает в действие фермент гидроксиметил-глутарил-SКоА-редуктаза (ГМГ-SКоА-редуктаза), образующая мевалоновую кислоту.
2. Синтез изопентенилдифосфата. На этом этапе при использовании АТФ мевалоновая кислота трижды фосфорилируется. Затем промежуточный продукт декарбоксилируется и дефосфорилируется с получением изопентенилдифосфата.
3. После объединения трех молекул изопентенилдифосфата (если не считать промежуточных превращений) синтезируется фарнезилдифосфат.
4. Синтез сквалена происходит при связывания двух остатков фарнезилдифосфата.
5. После сложных реакций линейный сквален циклизуется в ланостерол.
6. Удаление лишних метильных групп, восстановление и изомеризация молекулы приводит к появлению холестерола.
Регуляция синтеза
Регуляторным ферментом является гидроксиметилглутарил-SКоА-редуктаза, активность которой может изменяться в 100 и более раз.
1. Метаболическая регуляция – по принципу обратной отрицательной связи фермент аллостерически ингибируется конечным продуктом реакции – холестеролом. Это помогает поддерживать внутриклеточное содержание холестерола постоянным.
2. Регуляция транскрипции гена ГМГ-SКоА-редуктазы (в печени) – холестерол и желчные кислоты подавляют считывание гена и уменьшают количество фермента.
3. Ковалентная модификация при гормональной регуляции:
- Инсулин, активируя протеин-фосфатазу, способствует переходу фермента в активное состояние.
Важным следствием такой регуляции является активация кетогенеза при отсутствии инсулина.
- Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму.
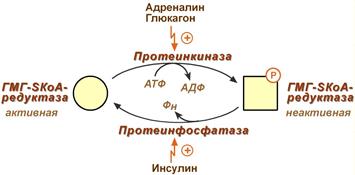
Регуляция активности гидроксиметилглутарил-S-КоА-редуктазы
Кроме указанных гормонов, на ГМГ-SКоА-редуктазу действуют эстрогены и тиреоидные гормоны (повышают активность) и глюкокортикоиды (снижают активность).
Изменение транскрипции гена ГМГ-КоА редуктазы (генетическая регуляция) осуществляется стерол-регулируемым элементом в ДНК (SREBP, sterol regulatory element-binding protein) с которым способны связываться белки — факторы SREBP. Эти факторы при достаточном количестве холестерина в клетке закреплены в мембране ЭПР. Когда уровень холестерина падает, факторы SREBP активируются под действием специфичных протеаз комплекса Гольджи, передвигаются в ядро, взаимодействуют на ДНК с участком SREBP и стимулируют биосинтез холестерина.
Скорость биосинтеза холестерола также зависит от концентрации специфического белка-переносчика, обеспечивающего связывание и транспорт гидрофобных промежуточных метаболитов синтеза.
Источник
Как происходит синтез холестерина в организме?
В организме человека происходит ежеминутно много биохимических реакций и обменных процессов. Метаболизм не останавливается ни на секунду.
Многие биохимические процессы возглавляют клетки печени, и несут за них ответственность. Основная функция клеток печени — это синтез холестерола.
От данного процесса зависит выработка стероидного типа половых гормонов, преобразование солнечной энергии в витамин Д, и транспортировка питания во все клетки организма при помощи холестериновых молекул.
В чем суть процесса выработки молекул холестерина?
Многие продукты питания наполняют организм холестерином — это продукты животного происхождения, а также транс-жиры, которые находятся в большом количестве в полуфабрикатах промышленного производства, а также в продуктах быстрого питания (фаст-фудах).
Если употреблять такие продукты безмерно, тогда концентрация в составе крови молекул холестерина станет высокой и придётся прибегать к медикаментозному решению гиперхолестеринемии.
Холестерин, который попадает в организм с продуктами питания, имеет низкую молекулярную плотность, что и привод к оседанию такого холестерина на внутренних оболочках сосудов, что провоцирует развитие холестериновой бляшки и патологии атеросклероз.
Повышение индекса холестерина в составе крови происходит не только по причине попадания его извне, но и от нарушения в процессе синтезирования молекул липопротеидов клетками печени.
Синтез холестеринак содержанию ↑
Синтез холестерола в печени
Синтез холестерола в составе организма составляет приблизительно 0,50 -0,80 грамм в сутки.
Распределяется синтез молекул холестерина в организме:
- 50,0% вырабатывается клетками печени;
- 15,0% — 20,0% — отделами тонкого кишечника;
- 10,0% — синтезируется корой надпочечников и клетками кожных покровов.
Все клетки в человеческом организме имеют способность к синтезу липопротеидов.
С продуктами питания поступает в организм молекулы холестерина до 20,0% от всего общего объема — приблизительно 0,40 грамм в сутки.
Выводится за пределы организма липопротеиды при помощи жёлчной кислоты, и в сутки утилизация молекул холестерола жёлчью — не больше, чем 1,0 грамм.
к содержанию ↑
Биосинтез липопротеидов в составе организма
Биосинтез молекул липидов происходит в эндоплазматическом отделе — ретикулуме. Основой для всех атомов молекул углерода является вещество ацетил-SКоА, которое поступает в эндоплазму из митохондрий в молекулах цитрата.
При биосинтезе молекул липопротеидов принимают участие 18 молекул АТФ, а также участниками синтеза становятся 13 молекул НАДФН.
Процесс образования холестерина проходит не менее 30 этапов и реакций в организме.
Поэтапный синтез липопротеидов можно распределить по группам:
вставить активная подсказка — уровень сахара
- Синтез мевалоновой кислоты происходит в процессе кетогенеза первых двух реакций, а после третьего этапа идёт реакция 3-гидрокси-3-метилглутарил-SКоА с молекулой ГМГ-SКоА-редуктазы. От этой реакции и происходит синтезирование мевалонат. Для этой реакции необходимо достаточного количества глюкозы в составе крови. Восполнить ее можно при помощи сладких продуктов и злаковых культур;
- Синтез изопентенилдифосфата происходит после присоединения фосфата к молекулам мевалоновой кислоты и их дегидрации;
- Синтез фарнезилдифосфат происходит после соединения трёх молекул изопентенилдифосфата;
- Синтезирование сквалена — это связывание 2-х молекул фарнезилдифосфата;
- Происходит реакция перехода сквалена в молекулу ланостерола;
- После удаления ненужных метильных групп и происходит преобразование холестерола.
к содержанию ↑
Регуляция процесса синтеза липопротеидов
Регуляторным элементом в процессе синтеза является фермент гидроксиметилглутарил-SКоА-редуктазы. Способность данного фермента изменять активность более чем в 100 раз.
Регуляция активности фермента происходи по нескольким принципам:
- Регуляция синтезирования на метаболическом уровне. Данный принцип работает «от обратного», фермент ингибируется холестеролом, что дает возможность поддерживать постоянное внутриклеточное его содержание;
- Ковалентная гормональная регуляция.
Регуляция на гормональном уровне происходит по таким этапам:
- Повышение содержания в организме гормона инсулина, активирует протеин-фосфатазу, что провоцирует увеличение активности главного фермента ГМГ-SКоА-редуктазы;
- Гормон глюкагон и гормон адреналин имеют свойства активировать элемент протеинкиназы А, которая фосфорилирует фермент ГМГ-SКоА-редуктазы и снижает их активность;
- Активность синтезирования холестерола зависит от концентрации в составе крови специального белка-транспортировщика, что своевременно связывает промежуточные реакции метаболитов.
Регуляция активности гидроксиметилглутарил-S-КоА-редуктазык содержанию ↑
Использование холестерина организмом
Синтезируемый в клетках печени холестерин, необходим организму для различных жизненно важных процессов:
- Находясь в каждой мембране клеток, молекулы холестерина укрепляют их и делают эластичными;
- При помощи липопротеинов, сосудистые оболочки увеличивают свою проницаемость, что защищает их от внешнего воздействия;
- Без помощи липопротеидов надпочечники не производят выработку стероидного типа половых гормонов;
- При помощи липидов происходит продуцирование желчной кислоты и предотвращает желчный пузырь от камнеобразования в нем;
- Липопротеиды связывают между собой клетки нейронов в спинном и в головном мозге;
- При помощи липопротеидов происходит укрепление оболочки нервных волокон;
- С помощью холестерола происходит выработка витамина Д, что помогает усваиваться кальцию и предотвращает разрушение костных тканей.
Холестерол помогает производить надпочечниками синтез таких групп гормонов:
- Группа кортикостероидов;
- Группа гормонов глюкокортикоидов;
- Группа минералокортикоидов.
Холестерол помогает производить надпочечниками синтез групп гормонов
Данные гормоны обеспечивают процессы гормонального регулирования репродуктивных органов человека.
Молекулы холестерина после синтеза в клетках печени попадают в эндокринный орган надпочечники и способствуют выработке гормонов и поддержанию баланса в гормональной сфере.
к содержанию ↑
Выработка молекул витамина Д происходит от солнечного света, который проникает в холестерин, находящийся под кожей. В этот момент и происходит синтез витамина Д, который очень важен для усваивания организмом минералов кальция.
Все виды липопротеидов, после синтеза транспортируются по организму системой кровотока.
Витамин Д может преобразовываться только липопротеидами высокой молекулярной плотности, а низкомолекулярные липиды становятся причиной развития патологии атеросклероз, потому что имеют свойства оседать на внутренних оболочках артерий в виде холестериновых бляшек, которые разрастаясь и провоцируют данную патологию.
Иногда холестериновые бляшки можно наблюдать у человека под кожными покровами на кистях рук.
Метаболизм витамина Дк содержанию ↑
Нарушения в процессе синтеза липопротеидов
Во многих обменных процессах в организме может произойти сбой и нарушение. Такие нарушения могут произойти и в липидном обмене. Причин достаточно много и они имеют экзогенную и эндогенную этиологию.
К эндогенным причинам нарушения синтеза липопротеидов относятся:
- Возраст человека. После 40 лет в организме человека происходит затухание выработки половых гормонов и нарушается гормональный фон, а также к 45 — 50 годам происходит замедление всех обменных процессов, что может внести разлад и в липидный обмен;
- Половой признак — мужчины больше подвержены накапливанию холестерина, чем женщины. Женщины до климактерического периода и менопаузы, защищены выработкой половых гормонов, от накопления липопротеинов;
- Генетическая наследственная предрасположенность. Развитие семейной гиперхолестеремии.
К экзогенным причинам липидного сбоя относятся факторы, что зависят от стиля жизни больного, а также сопутствующие патологии, способствующие нарушению в синтезе молекул холестерина:
- Никотиновая зависимость;
- Хроническая алкогольная зависимость;
- Неправильное питание может привести к повышенному содержанию в организме холестерина и накопления его не только в составе крови;
- Малоподвижный образ жизни становится причиной замедленных обменных процессов и синтеза липопротеидов;
- Гипертоническая болезнь — высокое давление в системе кровотока дает предпосылки тому, чтобы сосудистые оболочки пропитывались липидными жирами, которые впоследствии формируют холестериновую бляшку;
- Заболевание дислипидемия — это нарушение в липидном обмене. При патологии происходит дисбаланс между липопротеидами ВП, липидами НП, а также уровень содержания в составе крови триглицеридов;
- Патология ожирение;
- Сахарный диабет. При гипергликемии нарушается метаболизм и обмен липидами.
Патология ожирениек содержанию ↑
Дефицит в организме молекул полезного холестерола
Существуют патологии, которые снижают концентрацию высокомолекулярного холестерина в составе крови по причине снижения синтеза молекул ЛПВП.
Это может привести к патологиям в щитовидной железе, может значительно повлиять на уровень сахара в составе крови и спровоцировать сахарный диабет, а также стать причиной многих заболеваний системы кровотока и сердечного органа.
Последствиями низкой концентрации высокомолекулярного холестерина могут быть:
- Патология рахит, которая развивается в детском возрасте по причине сниженного синтеза витамина Д и не усвояемости молекул кальция;
- Раннее старение клеток организма. Без своевременной подачи холестерина в клеточные мембраны, происходит их разрушение и запускается процесс старения;
- Резкое снижение массы тела, которое происходит от недостаточного синтеза молекул холестерина, и нарушения в липидном обмене;
- Болезненность в мышечных тканях от недостатка в клетках мышц липидов;
- Боли в сердечном органе, что могут спровоцировать сердечный приступ.
Откорректировать индекс высокомолекулярного холестерина можно при помощи диетического питания, в состав которого входит морская рыба, различные растительные масла, а также кисломолочная продукция.
И не стоит забывать о свежих фруктах, зелени и овощах — они должны преобладать в рационе диеты.
к содержанию ↑
Фотогалерея: Недостаток полезного холестерина
к содержанию ↑
Превышение нормы липопротеидов
Если в человеческом организме происходит усиленный синтез высокомолекулярного липопротеида, тогда это также может негативно сказаться на здоровье.
Повышенная концентрация грозит развитием таких патологий:
- Развивается цирроз клеток печени;
- Риск развития гепатита;
- Увеличение массы тела;
- Нарушение во всем обмене липидов;
- Процессы воспаления в системе кровотока, а также в печеночном органе.
Также от переизбытка молекул холестерина ЛПВП и ЛПНП происходит оседание молекул на стенках артериальных оболочек, образуя холестериновые бляшки, которые влияют на движение крови в русле, по причине сужения артериального просвета.
Также от нарушения в синтезе холестерола, происходит неправильная работа желчного органа, что приводит к камнеобразованию в нем.
к содержанию ↑
Видео: Холестерин — бомба замедленного действия!
к содержанию ↑
Заключение
Синтез холестерола в печени — это очень сложный процесс, который происходит в организме постоянно и не прерываясь.
Если происходят нарушения в липидном обмене, или в процессе синтезирования липопротеидов, тогда существует высокий риск развития патологии атеросклероз, которая прогрессируя, приводит к более тяжелым заболеваниям, что могут спровоцировать преждевременную смерть.
Нарушения в липидном обмене, также влияют на работу сердечного органа и на функциональность клеток печени.
Постоянная корректировка холестерина при помощи диеты, позволит поддерживать липидный обмен в пределах нормы.
Загрузка…
Источник