Соединение гемоглобина с газами спектр поглощения
Поглощение света и цвет гемоглобина.Цвет растворенного вещества, не испускающего световые лучи, зависит от его способности поглощать падающий свет в той или иной части спектра видимого света. Как правило, каждое вещество поглощает свет лишь в определенной области спектра, тогда как свет других длин волн проходит через это вещество почти беспрепятственно. Цвет раствора вещества определяется спектральным составом прошедшего через него света. Красный цвет растворов гемоглобина (и, следовательно, крови) обусловлен тем, что это вещество относительно сильно поглощает коротковолновый свет, т. е. в синей области спектра, а большую часть длинноволнового (красного) света пропускает. При исследовании света, прошедшего через раствор оксигенированного гемоглобина, с помощью спектроскопа можно обнаружить не только полосу поглощения в синей области спектра (полосу Соре), но также две характерные темные полосы (полосы поглощения) в желтой и желто-зеленой областях спектра с максимумами при длинах волн 577 и 541 нм [11]. Дезоксигемоглобин несколько интенсивнее, чем оксигемоглобин, поглощает длинноволновые лучи и менее интенсивно — коротковолновые. В связи с этим венозная кровь выглядит темнее и имеет красный цвет с синеватым оттенком. При спектроскопическом исследовании выявляется одна широкая полоса поглощения в желто-зеленой части спектра с максимумом при длине волны 555 нм. Спектрфотометрия. Для количественного анализа абсорбционных свойств окрашенного раствора используют спектрофотометры. В этих приборах видимый свет разлагается в спектр при помощи призмы или дифракционной решетки, а затем свет очень узкой области длин волн (так называемый монохроматический свет) проходит через исследуемый раствор. Поглощение света зависит от длины волны и от свойств раствора. Для определения соотношения между интенсивностью падающего (I0) и прошедшего (I) света используется фотоэлемент. Отношение I/I0 называется пропусканием, а отношение (I0 — I)/I0 — поглощением. Полный спектр поглощения раствора получают путем последовательного измерения этих величин для разных длин волн. ГЛАВА 22. ТРАНСПОРТ ГАЗОВ КРОВИ 607
Спектры поглощения.На рис. 22.4 изображены спектры поглощения оксигемоглобина ндезоксигемоглобина. Тем участкам спектра, в которых при спектроскопии обнаруживаются темные полосы, соответствуют максимумы на кривой поглощения. Для оксигемоглобина характерны два таких максимума, а для гемоглобина — один, занимающий положение между ними. Из рисунка видно, что эти максимумы приходятся на те же длины волн, что и полосы поглощения. Точки пересечения обеих кривых поглощения, или так называемые изобестические точки, соответствуют длинам волн, при которых растворы равной концентрации Hb и НbО2 пропускают свет в одинаковой степени. Если длина волны световых лучей соответствует изобестической точке, то поглощение их гемоглобином не зависит от степени его оксигенации. Монохроматический свет такой длины волны используют в тех случаях, когда необходимо определить концентрацию гемоглобина, не подвергая его химическим модификациям (см. ниже). Если же спектрофотометрию используют для измерения насыщения гемоглобина кислородом, то, напротив, выбирают свет с такой длиной волны, при которой разница между коэффициентами поглощения оксигемоглобина и дезоксигемоглобина максимальна, т.е. 600, 577, 470 нм и т. д. (см. рис. 22.4). Закон Ламберта-Бэра. Вкачестве количественной характеристики поглощения света часто используют также экстинкцию(Е) (на рис. 22.4 отложена по правой оси ординат): О) где I0-интенсивность падающего света, а I- интенсивность прошедшего света. Экстинкцию удобно использовать в связи с тем, что она прямо про- порциональна концентрации растворенного вещества С: (2) где d-толщина слоя раствора, а ε — коэффициент экстинкции (величина, постоянная для каждого вещества). Линейная зависимость между экстинкцией, концентрацией и толщиной слоя раствора называется законом Ламберта-Бэра. Этот закон справедлив только для монохроматического света. Содержание гемоглобина в крови; среднее содержание гемоглобина в эритроците Нормальные показатели.Содержание гемоглобина в крови человека составляет в среднем 158 г/л (15.8 г/дл) у мужчин и 140 г/л (14 г/дл) у женщин. Как и практически любые биологические показатели, эта величина претерпевает определенные колебания даже у здоровых людей. Пределы колебаний определяют путем построения частотного распределениязначений для большого числа людей (рис. 22.5). С возрастом содержание гемоглобина в крови заметно меняется. В крови новорожденного оно составляет 200 г/л. причем возможны значительные индивидуальные колебания (рис. 22.5). В течение первого года жизни содержание гемоглобина снижается примерно до 115 г/л, а затем постепенно возрастает до уровня, характерного для взрослых. Высокое содержание гемоглобина в крови наблюдается не только у плода, но также у лиц, длительное время живущих в условиях высокогорья (с. 714). И в том и в другом случае повышение содержания гемоглобина необходимо для того, чтобы обеспечить нормальное снабжение тканей кислородом при пониженном парциальном давлении этого газа. Уменьшение содержания гемоглобина по сравнению с нормальным уровнем называется анемией.Как правило, диагноз анемия ставят в том случае, если содержание гемоглобина меньше 130 г/л у мужчин и 120 г/л у женщин. Измерение содержания гемоглобина.Для измерения содержания гемоглобина существует много методов, в том числе: 1) определение количества связанного О2(1 г Hb может присоединить до 1,36 мл О2); 2) анализ уровня железа в крови (содержание железа в гемоглобине составляет 0,34%); 3) колориметрия (сравнение цвета крови с цветом стандартного раствора); 4) измерение экстинкции (спектрофотометрия). При проведении рутинных определений уровня гемоглобина отдают предпочтение последнему методу, так как при использова- 6C8 ЧАСТЬ VI. ДЫХАНИЕ нии первых двух способов необходима сложная аппаратура, а метод колориметрии неточен. Спектрофотометрический анализ. Принцип метода состоит в определении содержания Hb в крови по экстинкции монохроматического света. Поскольку растворенный гемоглобин нестабилен, а экстинкция зависит от степени оксигенации, его необходимо предварительно перевести в стабильную форму. Спектрофотометрические измерения содержания гемоглобина производят следующим образом. Кровь набирают в капиллярную пипетку и затем смешивают с раствором, содержащим калий железосинеродистый (K3[Fe(CN)6]), цианистый калий (KCN) и бикарбонат натрия (NaHCO3). Под действием этих веществ эритроциты разрушаются, и гемоглобин превращается в цианметгемоглобинHbCN (содержащий трехвалентное железо), способный сохраняться в течение нескольких недель. При спектрофотометрии раствор цианметгемоглобина освещают монохроматическим светом с длиной волны 546 нм и определяют экстинкцию Е. Зная коэффициент экстинкции ε и толщину слоя раствора d, можно, исходя из закона Ламберта-Бэра [уравнение (2)], определить концентрацию раствора С непосредственно по величине экстинкции Е. Чаще предпочитают, однако, предварительно откалибровать шкалу экстинкции при помощи стандартного раствора. В настоящее время цианметгемоглобиновый метод считается наиболее точным из общепринятых способов измерения содержания гемоглобина [32]. Среднее содержание гемоглобина в эритроците. Важным диагностическим показателем, позволяющим оценить эритропоэз и провести дифференциальную диагностику различных форм анемии, служит среднее содержание гемоглобина в одном эритроците (СГЭ) (по международной классификации-mean corpuscular hemoglobin, MCH). Эта величина отражает абсолютное количество гемоглобина, содержащееся в среднем в одном эритроците. Ее находят путем деления количества гемоглобина в определенном объеме крови на число эритроцитов в том же объеме. Приведем пример расчета СГЭ. У здорового мужчины в 1 л крови содержится 158 г Hb и 5,1 млн ∙ 106 эритроцитов (1 л = 106 мкл). СГЭ равно отношению этих величин: Такая же величина СГЭ характерна и для здоровых женшин: Эритроциты с нормальным содержанием гемоглобина (26-36 пг) называют нормохромнымн. Если СГЭ патологически снижено, то эритроциты называют гипохромными, а если оно повышено — гиперхромными. Эти же термины употребляют и для обозначения различных форм анемии. Так, когда образование гемоглобина снижается в результате недостатка железа, содержание гемоглобина в расчете на эритроцит падает, и возникает гипохромная анемия. При других разновидностях анемии (например, пернициозной анемии) нарушается образование красных кровяных телец в костном мозгу, и в крови появляются деформированные эритроциты с высоким содержанием гемоглобина. В этом случае речь идет о гиперхромной анемии. После значительной кровопотери СГЭ сначала не изменяется (нормохромная анемия), а в последующем вследствие избыточной продукции эритроцитов содержание гемоглобина в них падает (гипохромная анемия). Рекомендуемые страницы: |
Источник
Лабораторная работа №22
Изучение оптических свойств различных форм гемоглобина
Каждая форма гемоглобина характеризуется определенным спектром поглощения, представляющим собой зависимость оптической плотности раствора гемоглобина от длины волны света. Наиболее интенсивной полосой в спектре поглощения гемоглобина является полоса Соре, принадлежащая порфириновой части его молекулы (рис. 5).
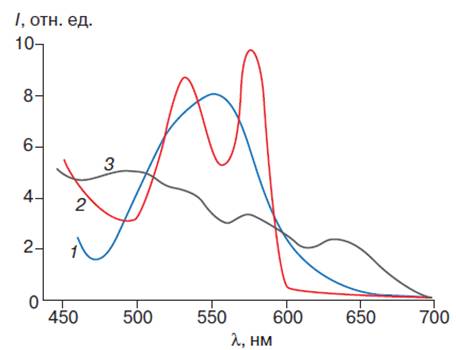
Рис. 5. Спектр поглощения производных гемоглобина. Спектры поглощения дезоксигемоглобина (1), оксигемоглобина (2) и ферригемоглобина (3)
По изменению положения и интенсивности поглощения этой полосы можно судить о структурных изменениях молекул различных форм гемоглобина (табл. 22).
Таблица 22
Спектральные характеристики различных форм гемоглобина
Формы гемоглобина | α-Полоса | β-Полоса | Полоса Соре | |||
λ, нм | ελ, М-1см-1 | λ, нм | ελ, М-1см-1 | λ, нм | ελ, М-1см-1 | |
Оксигемоглобин | 557 | 14600 | 542 | 13800 | 412 | 135000 |
Дезоксигемоглобин | 555 | 13500 | 430 | 119000 | ||
Карбоксигемоголобин | 569 | 13400 | 539 | 13400 | 419 | 191000 |
Оборудование и материалы. СФ-(46) или другой спектрофотометр, центрифуга на 9000 об/мин, центрифужные пробирки, кюветы, пенициллиновые флаконы, пипетки Пастера, прибор для получения оксида углерода, гемоглобин кристаллический, хлористый натрий, гепарин, бихромат калия, феррицианид калия, дитионит натрия.
Получение раствора оксигемоглобина. Для работы рекомендуется использовать свежеприготовленные растворы гемоглобина. Кровь берут у декапитированных животных. Цельную кровь стабилизируют гепарином, растворенным в 0,85%-ном растворе хлористого натрия. Для отделения плазмы стабилизированную кровь центрифугируйте в течение 10 мин при 3000 об/мин. Плазму крови отберите пипеткой. К эритроцитам добавьте трехкратный объем 0,85%-ного раствора хлористого натрия, осторожно при этом размешивая суспензию стеклянной палочкой. Суспензию центрифугируйте в течение 5 мин при 6000 об/мин. Промойте эритроциты 3 раза. Промытые эритроциты подвергните гемолизу дистиллированной водой в течение 20 мин. Стромы осадите центрифугированием при 9000 об/мин в течение 15 мин. В прозрачном гемолизате определите содержание гемоглобина с помощью приведенного в работе № 20 метода.
Ход анализа
Регистрация спектра поглощения оксигемоглобина. Раствор оксигемоглобина разбавьте дистиллированной водой до оптической плотности раствора, попадающей в диапазон 0,4-0,5. Снимите спектр поглощения раствора оксигемоглобина в интервале длин волн 380-600 нм (оптическая плотность раствора измеряется через каждые 5 нм).
Регистрация спектра поглощения метгемоглобина. Добавьте к раствору оксигемоглобина 1-2 капли насыщенного раствора феррицианида калия. Визуально оцените изменение окраски. Раствор метгемоглобина имеет коричневую окраску. Снимите спектр поглощения раствора гемоглобина в интервале длин волн 380-600 нм. Для компенсации светопоглощения за счет феррицианида в контроль добавьте такой же объем раствора этого вещества, какой был добавлен к раствору оксигемоглобина.
Регистрация спектра поглощения метгемоглобина. Добавьте к водному раствору оксигемоглобина несколько кристаллов дитионита натрия (Na2S2O4). Визуально оцените изменение окраски. Ярко алая окраска (цвет оксигемоглобина) переходит в синевато-красную, характерную для гемоглобина. Снимите спектр поглощения раствора в интервале длин волн 380-600 нм.
ЗАДАНИЕ
1. Представьте в графическом виде зависимость оптической плотности различных состояний гемоглобина от длины поглощаемого света (спектр поглощения), откладывая по оси ординат оптическую плотность раствора, а по оси абсцисс соответствующие длины волн.
2. Найдите минимумы и максимумы поглощения гемоглобинов и сделайте вывод.
Источник
Гемоглобин. Гемостаз. Факторы, поддерживающие кровь в жидком состоянии.
— перенос кислорода. Гемоглобин присоединяет кислород при высоком порциальном давлении(в легких). В молекуле гемоглобина имеется 4 гема, каждый из которых может присоединить молекулу кислорода. Оксигенация- присоединение кислорода к гемоглобину, т.к. не происходит процесс изменения валентности железа. В тканях, где низкое парциальное давление гемоглобин отдает кислород — дезоксикинация. Соединение гемоглобина и кислорода называется оксигемоглобин. Процесс оксигенации идет ступенчато.
Hb4+O2=Hb4O2
Hb4O2+O2=Hb4O4
Hb4O4+O2= HbO6
Hb4O2+O2= Hb4O8
В ходе оксигенации процесс присоединения кислорода возрастает.
Кооперативный эффект — молекулы кислорода в конце присоединяются в 500 раз быстрее. 1 г гемоглобина присоединяет 1,34 мл O2.
100% насыщение крови гемоглобином — максимальное процентное(объемное) насыщение
20мл на 100мл крови. На самом деле гемоглобин насыщается на 96-98%.
Присоединение кислорода также зависит от pH, от количества CO2, 2,3-дифософглицерат(продукт неполного окисления глюкозы). При накоплении его гемоглобин начинает легче отдавать кислород.
Метгемоглобин, в котором железо становится 3х валентным(при действии сильных окислителей-феррицианид калия, нитраты, бертолетовая соль, фенацитин) Он не может отдавать кислород. Метгемоглобин способен связывать синилистую кислоту и др. связи, поэтому при отравлении этими веществами в организм вводят метгемоглобин.
Карбоксигемоглобин(соединение Hb с CO) угарный газ присоединяется в гемоглобине к железу, но сродство гемоглобина к угарному газу выше в 300 раз, чем к кислороду. Если в воздухе больше 0,1 % угарного газа, то гемоглобин связывается с угарным газом. 60% связано с угарным газом(смерть). Угарный газ содержится в выхлопных газах, в печах, образуется при курении.
Помощь пострадавшим — отравление угарным газом начинается незаметно. Сам человек не может двигаться, необходим его вынос из этого помещения и обеспечение дыхания желательно газовым баллоном с 95% кислорода и 5 % углекислого газа. Гемоглобин может присоединяться углекислый газ — карбгемоглобин. Соединение происходит с белковой частью. Акцептором являются аминные части(NH2) — R-NH2+CO2=RNHCOOH.
Это соединение способно удалять углекислый газ. Соединение гемоглобина с разными газами обладает разными спектрами поглощения. Восстановленный гемоглобин имеет одну широкую полосу желто-зеленой части спектра. У оксигемоглобина образуется 2 полосы в желто-зеленой части спектра. Метгемоглобин имеет 4 полосы — 2 в желто-зеленой, в красной и в синей. Карбоксигемоглобин имеет 2 полосы в желто-зеленой части спектра, но это соединение можно отличить от оксигемоглобина путем добавления восстановителя. Поскольку карбоксигемоглобин соединение прочное, то добавление восстановителя не добавляет полос.
Гемоглобин выполняет важную функцию в поддержании нормального уровня pH. При отдаче кислорода в тканях гемоглобин присоединяет протон. В легких протон водорода отдается для образования угольной кислоты. При действии на гемоглобин сильных кислот или щелочей образуются соединения с кристаллической формой и эти соединения являются основанием для подтверждения крови. Гемины, гемохромогены. В синтезе парфирина(пиррольного кольца) принимают участие глицин и янтарная кислота. Глобин образуется из аминокислот путем синтеза белка. В эритроцитах, которые завершают свой жизненный цикл происходит и распад гемоглобина. При этом гемм отделяется от белковой части. От гемма отеляется железа, а из остатков гемма образуются желчные пигменты(например билирубин, который затем будет захватываться печеночными клетками) Внутри гепатоцитов происходит соединение гемоглобина с глюкуроновой кислотой. Билирубин гюкуронит выводится в желчные капилляры. С желчбю попадает в кишечник, где подвергается окислению, где переходит в урабиллин, который всасывается в кровь. Часть остается в кишечники и выводится с каловыми массами(их окраска — стеркобиллины). Уррабиллин придает окраску моче и снова захватывается печеночными клетками.
Свертывание крови(гемостаз)
Выполнение функции крови возможно при транспорте ее по сосудам. Повреждение сосудов могло бы вызвать кровотечение. Кровь может выполнять свои функции в жидком состоянии. Кровь может образовывать тромб. Это перекроет кровоток и приведет к закупорке сосудов. Вызывает их омертвление — инфаркт, некроз-последяствия внутрисосудистого тромба. Для нормальной функции системы кровообращения она должна обладать жидким и свойствами, но при повреждениях — свертывание. Гемостаз — ряд последовательных реакций, которые прекращают, либо уменьшают кроветечение. К этим реакциям относится —
- Сдавление и сужение поврежденных сосудов
- Формирование пластиночного тромба
- Свертывание крови, образование кровяного сгустка.
- Ретракция тромба и его лизис(растворение)
Первая реакция — сдавление и сужения — происходит за счет сокращения мышечных элементов, за счет выделения химических веществ. Эндотелиальные клетки(в капилярах) склеиваются и закрывают просвет. В более крупных клетках с гладкомышечными элементами происходит деполяризация. Сами ткани могут реагировать и сдавливать сосуд. Область в районе глаз имеет очень слабые элементы. Очень хорошо сдавливаются сосуду во время родов. Сужение сосудов вызывает — серотонин, адреналин, фибринопептид В, тромбоксан А2. Вот эта первичная реакция улучшает кровотечение. Образование пластиночного тромба(связан с функцией тромбоцитов) Тромбоциты представляют безъядерные элементы, имеют форму плоскую. Диаметр — 2-4 мкм, толщин — 0,6-1,2 мкм, объем 6-9фемтол. Количество 150-400*10 в 9 л. Образуются из мегакариоцитов путем отшнуровывания. Продолжительность жизни — 8-10 дней. Электронная микроскопия тромбоцитов позволила установить, что эти клетки имеют непростое строение, несмотря на их малый размер. Снаружи тромбоцит покрыт тромботической мембраной с гликопротеинами. Гликопротеины образую рецепторы, способные взаимодействовать друг с другом. Мембрана тромбоцитов имеет впячивание, которые увеличивают площадь. В этих мембранах — канальци для выделения веществ изнутри. Фосфомембраны очень важны. Пластиночный фактор из фосфолипидов мембраны. Под мембраной имеются плотные трубочки — остатки саркоплазматического ретикула с кальцием. Под мембраной также имеются микротрубочки и нити актина , миозина, которые поддерживают форму тромбоцитов. Внутри тромбоцитов имеются митохондрии и плотные темные гранулы и альфа гранулы — светлые. В тромбоцитах отличают 2 типа гранул, содержащие тельца.
В плотных — АДФ, серотони, ионы кальция
Светлые(альфа) — фибриноген, фактор Виллебранда, плазменный фактор 5, антигепариновый фактор, пластинчатый фактор, бета-тромбоглобулин, тромбоспондин и пластинчатый фактор роста.
Пластинки также имеют лизосомы и гранулы с гликогеном.
При повреждении сосудов пластинки принимают участие в поцессах агрегации и образовании пластиночного тромба. Эта реакция обусловленная рядом свойств, присущим пластинке — При повреждении сосудов обнажаются субэндотелиальные белки — адгезия(способность прилипать к эти белкам за счет рецепторов на пластинке. Адгезии способствует также фактор Виллебранка). Кроме свойства адгезии тромбоциты обладают способностью изменять свою форму и — выделять активные вещества(Тромбоксан А2, серотонин, АДФ,фосфолипиды мембраны -пластинчатый фактор 3, выделяется тромбин — свертывание — тромбин), характерна также агрегация(склеивание друг с другом). Эти процессы приводят к образованию пластиночного тромба, который способен вызвать остановку кровотечение. Важную роль в этих реакциях играет образование простогландинов. Из фосфолипилов мембран — образуется арахидоновая кислота(под действием фосфолипазы А2), — Простогландины 1 и 2(под действием циклооксигеназы). Впервые образованы в предстательной железе у мужчин. — Превращаются в тромбоксан А2, который подавляет аденилатциклазу и увеличивает содержание ионов кальция — происходит агрегация(склеивание пластинки). В эндотелии сосудов образуется простоциклин — он активирует аденилатциклазу, снижает кальций, это тормозит агрегацию. Применение аспирина — уменьшает образование тромбоксана А2, не затрагивая простациклин.
Факторы свертывания, которые приводят к формированию тромба. Сущность процесса свертывания крови состоит в превращении растворимого белка плазмы фибриногена в нерастворимый фибрин под действием протеазы тромбина. Это финал свертывания крови. Для того, чтобы это произошло необходимо действие свертывающей системы крови, которая включает в себя факторы свертывания крови и они подразделяются на плазменные(13 факторов) и есть пластиночные факторы. В свертывающую систему входят также антифакторы. Все факторы находятся в неактивном состоянии. Кроме свертывающей имеется фибринолитическая система — растворение образовавшегося тромба. Плазменные факторы свертывания крови —
1. Фибриноген, является единицей полимера фибрина с концентрации 3000 мг/л
2. Протромбин 1000 — Протеаза
3. Тканевой тромбопластин — кофактор(выделяется при повреждении клеток)
4. Ионизированный кальций 100 — кофактор
5. Проакцелерин 10 — кофактор(активная форма — акцелерин)
7. Проконвертин 0,5 — протеаза
8. Антигемофилический глобулин А 0,1 — кофактор. Соединен с фактором Виллибринга
9. Кристмас фактор 5 — протеаза
10. Фактор Стюарта-Проувера 10 — протеаза
11. Плазменный предшественник тромбопластина(фактор Розенталя) 5 — протеаза. Его отсутствие приводит к гемофилии типа С
12. Фактор Хагемана 40 — протеазы. С него начинаются процессы свертывания
13. Фибринстабилизирующий фактор 10 — трансамидазой
Без номеров
-Прекалликреин(фактор Флечера) 35 — протеаза
-Кининоген с высоким фактором МВ(фактор Фицжеральда.) — 80 — кофактор
-фосфолипиды тромбоцитов
Выделяют контактные факторы — 12,11, прекалликреин, кининоген с высоким молекулярным весом. Эти факторы активируются при контакте с поврежденной поверхностью.
Витамин К-зависимые факторы — 2,7,9,10, белок С и белок S
Фибриноеновая группа факторов 5,8,13. Факторы которые исчезают после образования фибрина. Свертывание крови является системой каскадных реакций, в ходе которых происходит поэтапное включение факторов свертывания крови
Система свертывания крови активируется 2мя путями — внутренней и внешний.
Внутренняя система активации крови связана с факторами находящимися в плазме крови. Начинается с 12 фактора Хагемана из неактивной формы переходит в активную форму. Этот поцесс может быть ускорен. Он действует на преекалликреин, переходит в каликринин, в присутствии каниногена. Следущюим этапом активируется 11 активный фактор и переводит его в активную форму. Далее воздействие на 9й фактор и под действием ионов кальция переводит его в активную форму, далее влияние на 10 фактор, при этом необходим 8 и 3го пластинчатого факторы — происходит образование активного 10го.
Внешняя система связана с освобождением 3го плазменного фактора. Включается при повреждении клеток. ОН взаимодействует с 7м фактором и ионами кальция и переводит его в 7ой активный фактор. Далее влияние на 10й и переводит его в активную форму. Здесь происходит соединение 2х путей внешней и внутренней системы. 7ой активный фактор может влиять на 3й внутренней системы. Активация 11го фактора возможна под действием тромбоцита. Тромбоциты могут прямо активировать 11ый фактор. И внутренняя и внешняя система заканчивается активацией 10го фактора, который оказывает влияние на протромбин(2ой фактор) и переводит его в активную форму — тромбин. На первом этапе процесс идет медленно. Ускоряет 3ий и 5ый фактор — в роли катализатора, способствует превращения протромбина в тромбин.
Образовавшийся тромбин активирует 13й фактор, но его предназначение — действие на фибриноген и превращать фибриноген в фибрин. Тромбин расщепляет связи в фибриногене и при этом образуется фибрин — мономер и еще 2 фибрина пептида А и Б. Мономеры фибрина взаимодействуют друг с другом и в присутствии кальция а также пластиночного 4ого фактора фибрин мономеры и соединяются в фибрин полимер, который на первом этапе представляет собой рыхлые соединения. Под действием 13го фактора образуются нити фибрина(связи ковалентные), которые формируют густую сеть. Образуется сгусток — тромб, который будет подвергаться сжатию, рефракции. Кроме тромба из крови образуется еще и жидкая часть — сыворотка крови — жидкая часть после процесса свертывания. В сыворотке крови отсутствует фибриноген и некоторые факторы свертывания крови. Происходит окончательная остановка кровотечения. Барьерная — тромб предупреждает попадание в рану токсинов и микробов. Тромб стягивает края раны и создает благоприятную среду для восстановления поврежденных клеток. На поверхности образуются корочки.
Факторы, поддерживающие кровь в жидком состоянии.
К числу таких факторов-ингибиторы факторов свертывания крови, которые предупреждают начало реакции свертывания крови. Большое значение имеет гладкая стенка кровеносных сосудов, эндотелий кровеносных сосудов покрыт тонкой пленкой из гепарина, который является антикоагулянтом. Инактивация продуктов, которые образуются в ходе свертывания крови — тромбин(10мл достаточно для того чтобы свернулась вся кровь в организме). В крови существуют механизмы, которые предупреждают такое действие тромбина. Фагоцитарная функция печени и некоторых других органов, которые способны поглощать тромбопластин 9,10 и 11 факторы. Снижение концентрации факторов свертывания крови осуществляется путем постоянного кровотока. Все это тормозит образование тромбина. Уже образовавшийся тромбин поглощается нитями фибрина, которые образуются в ходе свертывания крови(они абсорбируют тромбин). Фибрин — это антитромбин 1. Другой антитробин 3 — инактивирует образовавшийся тромбин и его активность увеличивается при совместном действии гепарина. Этот комплекс инактивирует 9, 10, 11, 12 факторы. Образовавшийся тромбин связывается с тромбомодулином(находится на клетках эндотелия). В результате этого комплекс тромбомодулин-тромбин способствует превращению белка С в активный белок(форму). Совместно с белком С действует белок S. Они инактивируют 5 и 8 факторы свертывания крови. Для своего образования эти белки(C и S) требуют поступления витамина К. Через активацию белка С в крови открывается фибринолитическая система, которая предназначена для растворения образовавшегося и выполнившего свою задачу тромба. В фибринолитическую систему входят факторы, активирующие и тормозящие эту систему. Для того, чтобы осуществился процесс растворения крови, необходима активация плазминогена. Активаторами плазминогена являются тканевой активатор плазминогена, который тоже находится в неактивном состоянии и плазминоген может активировать 12 активный фактор, калликреин, высокомолекулярный кининоген и ферменты урокиназа и стрептокиназа.
Для активации тканевого активатора плазминогена необходимо взаимодействие тромбина с тромбомодулином, которые являются активатором белка С, а активированный белок С активирует тканевой активатор плазминогена и он переводит плазминоген в плазмин. Плазмин обеспечивает лизис фибрина(нерастворимые нити превращает в растворимые)
Физическая нагрузка, эмоциональные факторы приводит к активации плазминогена. При родах иногда в матке тоже может активироваться большое количество тромбина, это состояние может приводить к угрожающим маточным кроветечениям. Большие количества плазмина могут действовать на фибриноген, уменьшая его содержание в плазме. Повышенное содержание плазмина в венозной крови, что тоже способствует кровотоку. В венозных сосудах есть условия для растворения тромба. В настоящее время используются препараты активаторы плазминогена. Это важно при инфаркте миокарда, что предупредит омертвление участка. В клинической практике используются препараты, которые назначаются для предупреждения свертывания крови — антикоагулянты, при этом антикоагулянты делятся на группу прямого действия и непрямого действия. В первую группу(прямого) относятся соли лимонной и щавелевой кислот — лимоннокислый натрий и ионощавеливый натрий, которые связывают ионы кальция. Восстановить можно добавив хлористый калий. Гирудин(пиявки) является антитромбином, способен инактивировать тромбин, поэтому пиявки широко применяются в лечебных целях. Гепарин назначают также в качестве препарата, для предупреждения свертывания крови. Гепарин также входит в состав многочисленных мазей и кремов.
К антикоагулянтом непрямого действия относятся антагонисты витамина К(в частности препараты, которые получаются из клевера — дикумарин). При введении дикумарина в организм нарушается синтез витамин К зависимых факторов(2,7,9,10). У детей, когда микрофлора недостаточно развита процессы свертывания крови.
Источник