Структурная формула эфира холестерина
Содержание статьи
формула (структурная, химическая) и биохимия процесса
Холестерин – это жизненно необходимое соединение для организма. Он является субстратом для гормона прогестерона, эстрогена, тестостерона, гормонов надпочечников (альдостерона, кортизола), участвует в одном из направлений метаболизма витамина Д, а также используется для построения мембран и клеточных стенок.
Холестерол, с точки зрения биохимии, — это органический липофильный спирт, который не растворяется в воде. Рассмотрим, чем характерна химическая формула холестерина и какие особенности и стадии выделяют в процессе его биосинтеза.

Формула и строение холестерина
Холестерин относится к группе стероидов. Является одним из главных стероидов в макроорганизме человека, определяет активность обмена липидов. По своей структуре это твердое кристаллическое бесцветное вещество, не растворяющееся в воде. Лабораторной единицей измерения в периферической крови является ммоль/л.
Химическая формула (она же брутто-формула) холестерина — C27H46O.
Молекулярная масса — около 387 г/моль.
Структурная форма выглядит следующим образом:

Структурная формула холестерола с нумерацией атомов в молекуле
Одна из основных особенностей молекулы холестерола – способность связываться с другими соединениями, образовывая комплексы молекул. Такими соединениями могут быть кислоты, амины, протеины, холекальциферол (предшественник витамина Д3), соли и прочие. Данное свойство обусловлено характерным строением молекулы холестерола и его высокой активностью в процессах биохимии.
Биосинтез холестерина
Весь холестерин в человеческом макроорганизме подразделяется на экзогенный и эндогенный. Экзогенный составляет около 20% от общего показателя и поступает в организм с продуктами питания. Эндогенный холестерол синтезируется непосредственно в организме. Его производство синхронно происходит в двух локализациях. В кишечнике специфическими клетками энтероцитами формируется около 15% вещества, а порядка 50% эндогенного холестерина вырабатывается в печени, где в дальнейшем связывается с белками, образует комплексы в виде липопротеидов и выходит в периферический кровоток. Небольшая часть также отправляется на синтез триглицеридов – эфиров жирных кислот и глицерина, которые соединяются с холестеролом.
Синтез холестерола – сложный и энергозатратный процесс. Необходимо больше 30 последовательных реакций липидной трансформации, чтобы в результате образовалась холестериновая молекула. Схематически, все эти превращения можно сгруппировать в шесть стадий процесса синтеза холестерола.
- Биосинтез мевалоната. Состоит из трех реакций. Первые две из них являются реакциями кетогенеза, а третью реакцию катализирует фермент ГМГ-SКоА редуктаза, под действие которой образуется первый предшественник холестерина – мевалоновая кислота. Механизм действия большинства гиполипидемических препаратов, в особенности статинов, направлен именно на это звено биосинтеза. Путем воздействие на ферментативную активность редуктаз, можно частично управлять холестериновой трансформацией.
- Биосинтез изопентенилпирофосфата. Три фосфатных остатка присоединяются к полученной мевалоновой кислоте. После этого она проходит процессы декарбоксилирования и дегидрирования.
- На третьем этапе происходит слияние трех изопентенилпирофосфатов, которые превращаются в фарнезилдифосфат.
- Из 2-х остатков фарнезилдифосфата образуется новая молекула – сквален.
- Линейный сквален проходит ряд реакций циклизации и трансформируется в ланостерол.
- От ланостерина отщепляются избыточные метильные группы, соединение проходит ступень изомеризации и восстановления, в результате которых образуется молекула холестерина.

Кроме активного фермента ГМГ-КоА редуктазы, в реакциях биосинтеза принимают участие инсулин, глюкагон, адреналин и специальный белок-переносчик, который связывает метаболиты на разных этапах.
Эфиры холестерола
Эстерификация холестерина – это процесс связывания с ним жирных кислот. Запускается он либо для переноса молекулы холестерола, либо для трансформации его в активную форму.
В данных превращениях важную роль играет лецитин – он присоединяется к молекуле холестерина и под действием фермента лецитин-холестерол-ацил-трансферазы образует эфиры лизолейцин и холестерид. Таким образом, реакция эстерификации – это процесс, направленный на снижение количество свободного холестерола в кровотоке. Полученные эфиры тропны к «хорошим» липопротеидов высокой плотности и легко к ним присоединяются. Образование эфиров холестерина – часть защитного антиатеросклеротического механизма.
Холестерин – очень важное для макроорганизма соединение, которое принимает не только участие в обмене липидов, но и в процессах транcформации биологически активных веществ и синтезе мембран клеток. Молекула данного вещества проходит сложный цикл превращений из более чем 30 реакций, которые регулируются и контролируются ферментативной и гуморальной системами.
Изменения в одном из звеньев биосинтеза может стать индикатором патологии со стороны внутренних органов и систем – печени, щитовидной и поджелудочной желез. Следует проводить профилактические обследования и скрининговые липидограммы, чтобы вовремя выявить патологический процесс.
Источник
ХОЛЕСТЕРИН — Большая Медицинская Энциклопедия
ХОЛЕСТЕРИН (греческий chole желчь + stereos твердый; синоним холестерол) — 3-β-гидроксихолест-5-ен, C27H46O, важнейший в биологическом отношении представитель стеринов. Холестерин является источником образования в организме млекопитающих желчных кислот (см.), кортикостероидов (см.), половых гормонов (см.), витамина D3 (см. Кальциферолы.), таким образом, физиологическая функция холестерина чрезвычайно многообразна. Холестерину отводят одну из главных ролей в развитии атеросклероза (см.), в соответствии с современной точкой зрения гиперхолестеринемия (см.) относится к ведущим этиологическим факторам его развития. Однако корреляция между содержанием холестерина в крови и степенью выраженности атеросклероза у человека обнаруживается не всегда. В патологии человека устойчивую гиперхолестеринемию обычно связывают с длительным нарушением холестеринового обмена (см.), в том числе генетически обусловленным. Повышение концентрации холестерина в крови обычно наблюдают при сахарном диабете, гипотиреозе, подагре, ожирении, гипертонической болезни, при некоторых заболеваниях печени, остром нарушении мозгового кровообращения и др. Однако генез гиперхолестеринемии при всех этих патологических состояниях неодинаков. Пониженное содержание холестерина отмечают при ряде инфекционных болезней, острых и хронических заболеваниях кишечника, гипертиреозе, выраженной сердечной недостаточности с застоем крови в печени и др. (см. Гипохолестеринемия).
Холестерин был описан в 1789 году французским химиком Фуркруа (A. F. Fourcroy) как главный составной компонент желчных камней человека. В 1816 году другой французский химик Шеврель (М. E. Chevreul) впервые назвал открытое Фуркруа соединение холестерином. Строение холестерина было окончательно установлено в 30-х годов 20 века, тогда же был осуществлен и его полный химический синтез.
Молекулярный вес (масса) холестерина составляет 386,66; его молекула состоит из четырех циклов, жестко связанных между собой и образующих циклопентанпергидрофенантреновое ядро, и алифатической цени при 17-м углеродном атоме (C17), обладающей небольшой подвижностью. В положении C3 молекулы холестерина имеется гидроксильная группа, а в положении C5—C6 двойная связь. Все шестиуглеродные циклы холестерина находятся в конфигурации кресла и в транс-сочленении, между собой. Общая длина молекулы холестерина 2,2 нм, площадь поверхности около 3,8 нм2.

Из безводных растворителей холестерин кристаллизуется в виде бесцветных игл, а из водного спирта — в виде жемчужных пластинок (моногидрат холестерина);t°пл 149,5—150°, относительная плотность d418 1,052, удельное вращение [a]D —39° (в хлороформе). Холестерин нерастворим в воде (при 20° в 100 мл воды растворяется всего лишь 80—150 мкг холестерина), однако он относительно легко растворяется в ацетоне, спирте, эфире и других органических растворителях. Холестерин хорошо растворим в животных и растительных жирах (маслах), а также в смеси полярных и неполярных органических растворителей.
Из химических свойств холестерина важное биологическое значение имеет его способность образовывать сложные эфиры с кислотами. Большая часть эфиров холестерина в организме человека и других млекопитающих образована высшими жирными кислотами (см.), содержащими в своей цепи 16—20 углеродных атомов. Гидроксильная группа в молекуле холестерина может окисляться в кетогруппу, что происходит, например, при образовании стероидных гормонов (см.). Благодаря подвижности водородного атома при С7 легко образуются окисленные продукты холестерина: 7-гидрокси- и 7-кетохолестерины. Один из них 7-альфа-гидроксихолестерин является важнейшим промежуточным продуктом на пути окисления холестерина в желчные кислоты в печени.
Другим важным химическим свойством холестерина, широко используемым для его аналитического определения, является его способность образовывать интенсивно окрашенные продукты при взаимодействии с сильными кислотами (см. Кислоты и основания) в неводных растворителях: с серной кислотой в уксусном ангидриде или в смеси уксусная кислота — хлороформ (см. Либерманна — Бурхарда реакция), с серной кислотой в хлороформе (реакция Сальковского), с хлористым цинком и хлористым ацетилом в хлороформе (реакция Чучаева), с хлорным железом и серной кислотой в уксусной кислоте (реакция Липшютца). Окрашенные продукты образует как сам холестерин, так и его эфиры, а также и другие стерины, содержащие в 5 —6-м положении двойную связь. Особенностью холестерина является его способность к образованию малорастворимых комплексов с различными кислотами, например, щавелевой, трихлоруксусной, и неорганическими солями — хлористым кальцием, хлористым литием и особенно с полиеновыми антибиотиками (см.) и растительными сапонинами (см.). Комплексообразование холестерина при взаимодействии с полиеновыми антибиотиками лежит в основе действия последних на дрожжи и дрожжеподобные организмы, содержащие в своей оболочке стерины (см.). Образование комплекса с дигитонином используется для раздельного определения свободного (неэтерифицированного) и этерифицированного холестерина: этот комплекс образует только свободный холестерин.
В теле взрослого человека, по данным химического анализа, находится около 140 г холестерина (примерно 0,2% веса тела); по данным радио-изотопных исследований, содержание холестерина значительно выше (200—350 г). В отдельных органах и тканях человека содержатся следующие количества холестерина (в мг на 1 г сырой ткани): кора надпочечников — 100; мозг и нервная ткань — 20; сосудистая стенка — 5; печень, почки, селезенка, костный мозг, кожа — 3; соединительная ткань — 2; скелетная мышца — 1. Неэтерифицированный холестерин преимущественно входит в состав клеточных мембран и в миелиновые оболочки. Ткани мозга, желчь и эритроциты содержат только неэтерифицированный холестерин; в скелетных мышцах содержится 93% неэтерифицированного и 7% этерифицированного холестерина, а надпочечники, напротив, содержат 83% этерифицированного и 17% неэтерифицированного холестерина. В плазме крови человека примерно две трети холестерина этерифицировано.
Каждая клетка в организме млекопитающих содержит холестерин и нуждается в нем для поддержания формы (так называемая функция клеточного «скелета»). Входя в состав клеточных мембран, неэтерифицированный холестерин вместе с фосфолипидами (см. Фосфатиды) обеспечивает избирательную проницаемость клеточной мембраны для веществ, входящих в клетку и выходящих из нее. Вместе с фосфолипидами холестерин регулирует активность мембранно-связанных ферментов путем изменения вязкости мембраны и модификации вторичной структуры ферментов.
Холестерин образует комплексы с некоторыми белками, особенно с теми, молекулы которых содержат большое количество остатков аргинина (см.) и лизина (см.). В присутствии фосфолипидов способность холестерина образовывать комплексы с белками возрастает. С некоторыми фосфолипидами, например, с лецитином (см.), холестерин непосредственно образует комплексы, которые в водной среде дают мицеллярные растворы; при обработке таких растворов ультразвуком получаются липосомы. Характерно, что в животном организме всюду, где встречается холестерин, ему сопутствуют фосфолипиды. Эфиры холестерина находятся внутри клетки и могут рассматриваться как его запасная форма. Их гидролиз по мере надобности осуществляется при участии лизосомной холестеринэстеразы (см.).
Содержание холестерина в плазме крови человека зависит от возраста: наиболее низко оно у новорожденных (65 — 70 мг/ 100 мл), к 1 году жизни концентрация холестерина увеличивается более чем вдвое и достигает примерно 150 мг/100 мл, к 7—8 годам содержание холестерина в плазме крови возрастает всего лишь на 10—15 мг/100 мл, оставаясь постоянным до 13—14 лет, после чего несколько снижается. С 18 — 20 лет наступает постепенное, но неуклонное повышение концентрации холестерина в плазме крови до некоторой постоянной величины, продолжающееся до 50 лет у мужчин и до 60—65 лет у женщин. В высокоразвитых странах Европы и Америки, а также в Австралии средняя концентрация холестерина в плазме крови мужчин 40—60 лет составляет 205—220 мг/100 мл, а. в плазме крови женщин того же возраста 195 — 235 мг/’100 мл.
Содержание холестерина в эритроцитах составляет 120 —140 мг/100 мл и у здоровых людей не зависит от его концентрации в плазме крови.
Установлено, что в плазме крови человека и животных весь холестерин находится в составе липопротеидных комплексов (см. Липопротеиды), с помощью к-рых и осуществляется его транспорт. У взрослого человека примерно 67 — 70% холестерина плазмы крови находится в составе липопротеидов низкой плотности (ЛПНП), 9 — 10% — в составе липопротеидов очень низкой плотности (ЛПОНП) и 20 — 24% — в составе липопротеидов высокой плотности (ЛПВГ1). Сходное распределение характерно и для животных , восприимчивых к развитию атеросклероза, — обезьян, свиней, кроликов, морских свинок, голубей и др. Напротив, у животных, устойчивых к развитию атеросклероза,— собак, кошек, сусликов, норок, песцов, енотов и др., большая часть холестерина плазмы крови находится в ЛПВП, обладающих антиатерогенным действием.
Другие внеклеточные жидкости содержат следующие количества холестерина (мг/100 мл): желчь — 390; плазма спермы — 80; секрет предстательной железы — 80; лимфа — 25; молоко — 20; синовиальная жидкость — 7; слюна — 5; цереброспинальная жидкость — 0,4; моча — 0,2.
Для количественного определения холестерина в плазме (сыворотке) крови используют методы, основанные на приведенных выше цветных реакциях (предложено свыше 400 вариантов таких методов). Наиболее часто используются методы, основанные на реакции Либерманна — Бурхарда и реакции Липшютца. Методы определения холестерина подразделяются на одноступенчатые — без предварительного экстрагирования холестерина из плазмы (сыворотки) крови — и многоступенчатые, включающие экстрагирование холестерина, а в ряде методов омыление (см.) эфиров холестерина, осаждение неэтерифицированного холестерина дигитонином и затем уже проведение цветной реакции. К одноступенчатым методам относится ускоренный метод Ильки (см. Ильки метод), а также метод Мирского — Товарека, основанный на образовании холестерином окрашенного продукта в растворе ледяной уксусной кислоты и уксусного ангидрида при добавлении серной и сульфосалициловой кислот. Одноступенчатые методы просты в исполнении, но дают завышенные результаты. Из многоступенчатых методов в клин, практике широко применяется метод Абелль и сотр. (см. Абелля метод), включающий предварительное экстрагирование холестерина из плазмы (сыворотки) петролейным эфиром, методы Левченко и Зигельгардта — Смирновой, при которых холестерин экстрагирует-с я хлороформом, микрометод Покровского (см. Покровского микрометоды), предусматривающий использование для экстрагирования спиртоэфирной смеси. К этой группе методов относятся также метод Раппопорта — Энгельберга и метод Григо. Одновременное определение общего и свободного холестерина проводится с помощью многоступенчатых методов с использованием дигитонина для осаждения свободного холестерина (см. Балаховского метод). Автоматические методы определения холестерина на приборах Technicon, Abbot и др. тоже основаны на образовании холестерином окрашенных продуктов.
Для определения холестерина применяют также ферментативный метод, основанный на окислении холестерина в присутствии холестериноксидазы (холестеролоксидазы; КФ 1.1.3.6) и определении количества образующейся перекиси водорода, а также газохроматографическое определение (см. Хроматография). Эффективное разделение холестерина и его эфиров достигается с помощью хроматографических методов, в частности хроматографии в тонком слое.
В целом определение холестерина различными методами дает неоднозначные результаты. Арбитражным является метод Абелль и сотр.
В клинике стало принятым рассчитывать величину отношения холестерина атерогенных липопротеидов к холестерину антиатерогенных липопротеидов. Одно из таких отношений — так называемый холестериновый коэффициент атерогенности — рассчитывается на основании определения концентраций общего холестерина и холестерина липопротеидов высокой плотности:
К = (Х — Х*ЛПВП) / Х*ЛПВП
где X — концентрация холестерина, Х*ЛПВП — концентрация холестерина липопротеидов высокой плотности. Это отношение является идеальным у новорожденных (не более 1), у лиц 20—30 лет его величина колеблется от 2 до 2,8, у лиц старше 30 лет без клинических признаков атеросклероза она находится в пределах 3—3,5, а у лиц с ишемической болезнью сердца превышает 4, достигая нередко 5—6 и выше. Этот коэффициент как показатель развития атеросклероза является более чувствительным, чем холестерин-лецитиновый показатель (отношение концентрации холестерина к концентрации лецитина в плазме крови), который одно время широко применялся в клинике.
Библиогр.: Биохимические методы исследования в клинике, под ред. А. А. Покровского, сА 18, М., 1969; Физер Л и Физер М. Стероиды, пер. с англ., М., 1964; Chevreul М. Е. Note sur le sucre de diabetes, Ann. Chim. (Paris), t. 95, p. 319, 1815; My ant N. The biology of cholesterol and related steroids, L., 1981
A. H. Климов, Д. В. Иоффе.
Источник
Холестерин
Холестерин
Холестерин
или холестерол – это стероид, характерный
только для животных организмов. Относится
к классу стеринов (стерилов). Для стеринов
характерно наличие гидроксильной группы
в положении 3, а также боковой цепи в
положении 17. У холестерина – все кольца
находятся в транс-положении; кроме того,
он имеет двойную связь между 5-м и 6-м
углеродными атомами. Следовательно,
холестерин является ненасыщенным
спиртом:
Ядро,
образованное гидрированным фенантреном
(кольца А, В и С) и циклопентаном (кольцо
D). Циклопентанпергидрофенантрен (общая
структурная основа стероидов)
Кольцевая
структура холестерина отличается
значительной жесткостью, тогда как
боковая цепь – относительной подвижностью.
Итак, холестерин содержит спиртовую
гидроксильную группу при С-3 и разветвленную
алифатическую цепь из 8 атомов углерода
при С-17. Химическое название холестерина
3-гидрокси-5,6-холестен. Гидроксильная
группа при С-3 может быть этерифицирована
высшей жирной кислотой, при этом
образуются эфиры холестерина (холестериды)
В
печени синтезируется более 50% холестерола,
в тонком кишечнике — 15- 20%, остальной
холестерол синтезируется в коже, коре
надпочечников, половых железах. В
цитоплазме холестерин находится
преимущественно в виде эфиров с жирными
кислотами, образующих вакуоли. В плазме
крови как неэтерифицированный, так и
этерифицированный холестерин
транспортируется в составе липопротеинов.
В сутки в организме синтезируется около
1 г холестерола; с пищей поступает 300-500
мг. Он является компонентом клеточных
мембран, предшественником при синтезе
желчных кислот, стероидных гормонов,
витамина D.
История открытия.
В 1769 году Пулетье
де ла Саль получил из желчных
камней плотное белое вещество
(«жировоск»),
обладавшее свойствами жиров.
В чистом виде холестерин был выделен
химиком, членом национального Конвента
и министром просвещения Антуаном
Фуркруа в 1789 году. В 1815 годуМишель
Шеврёль, тоже выделивший это соединение,
назвал его холестерином («холе» —
желчь, «стерин» — жирный). В 1859 году
Марселен
Бертло доказал, что холестерин
принадлежит к классу спиртов, после
чего французы переименовали холестерин
в «холестерол». В ряде языков (русском,
немецком, венгерском и др.) сохранилось
старое название — холестерин.
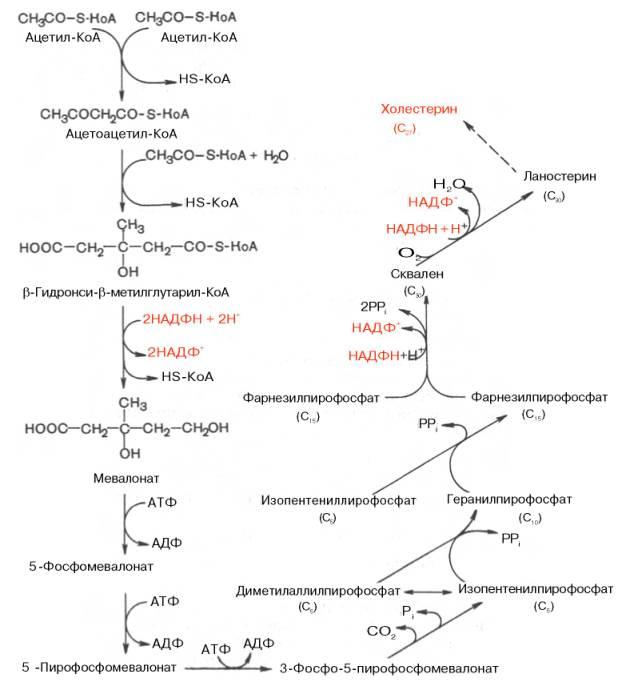
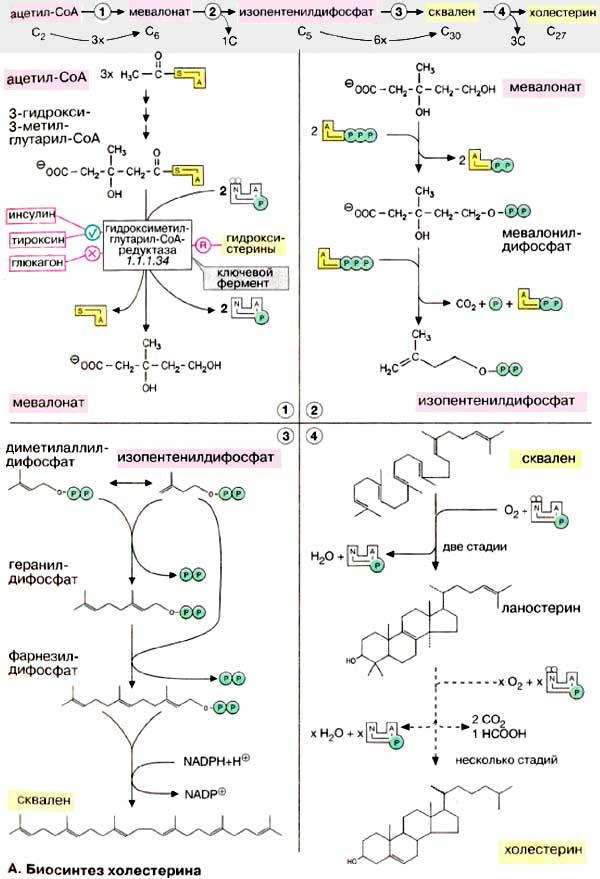
Синтез холестерина
начинается с ацетил-КоА. Биосинтез
холестерина можно разделить на четыре
этапа. На первом этапе (1) из трех молекул
ацетил-КоА образуется мевалонат (С6). На
втором этапе (2) мевалонат превращается
в «активный изопрен», изопентенилдифосфат.
На третьем этапе (3) шесть молекул изопрена
полимеризуются с образованием сквалена
(С30). Наконец, сквален циклизуется с
отщеплением трех атомов углерода и
превращается в холестерин (4). На схеме
представлены только наиболее важные
промежуточные продукты биосинтеза.
1.
Образование мевалоната. Превращение
ацетил-КоА в ацетоацетил-КоА и затем в
З-гидрокси-З-метилглутарил-КоА (3-ГМГ-КоА)
соответствует пути биосинтеза кетоновых
тел (подробно см. рис. 305), однако этот
процесс происходит не в митохондриях,
а в эндоплазматическом ретикулуме (ЭР).
3-ГМГ-КоА восстанавливается с отщеплением
кофермента А с участием 3-ГМГ-КоА-редуктазы,
ключевого фермента биосинтеза холестерину
(см. ниже). На этом важном этапе путем
репрессии биосинтеза фермента (эффекторы:
гидроксистерины), а также за счет
взаимопревращения молекулы фермента
(эффекторы: гормоны) осуществляется
регуляция биосинтеза холестерина.
Например, фосфорилированная редуктаза
представляет собой неактивную форму
фермента; инсулин и тироксин стимулируют
фермент, глюкагон тормозит; холестерин,
поступающий с пищей, также подавляет
3-ГМГ-КоА-редуктазу.
2.
Образование изопентенилдифосфата.
Мевалонат за счет декарбоксилирования
с потреблением АТФ превращается в
изопентенилдифосфат, который и является
тем структурным элементом, из которого
строятся все изопреноиды.
3.
Образование сквалена. Изопентенилдифосфат
подвергается изомеризации с образованием
диметилаллилдифосфата. Обе С5-молекулы
конденсируются в геранилдифосфат и в
результате присоединения следующей
молекулы изопентенилдифосфата образуют
фарнезилдифосфат. При димеризации
последнего по типу «голова к голове»
образуется сквален. Фарнезилдифосфат
является также исходным соединением
для синтеза других полиизопреноидов,
таких, как долихол и убихинон.
4.
Образование холестерина. Сквален,
линейный изопреноид, циклизуется с
потреблением кислорода в ланостерин,
С30-стерин, от которого на последующих
стадиях, катализируемых цитохромом
Р450, отщепляются три метильные группы,
вследствие чего образуется конечный
продукт — холестерин. Описанный путь
биосинтеза локализован в гладком ЭР.
Синтез идет за счет энергии, освобождающейся
при расщеплении производных кофермента
А и энергетически богатых фосфатов.
Восстановителем при образовании
мевалоната и сквалена, а также на
последних стадиях биосинтеза холестерина
является НАДФН + Η+. Для этого пути
характерно то, что промежуточные
метаболиты можно подразделить на три
группы: производные кофермента А,
дифосфаты и высоко липофильные соединения
(от сквалена до холестерина), связанные
с переносчиками стеринов.
.
Этерификация
холестерола.
В некоторых тканях гидроксильная группа
холестерола этерифицируется с образованием
более гидрофобных молекул — эфиров
холестерола. Реакция катализируется
внутриклеточным ферментом АХАТ (ацилКоА:
холестеролаиилтрансферазой). Реакция
этерификации происходит также в крови
в ЛПВП, где находится фермент ЛХАТ
(лецитин: холестеролацилтрансфераза).
Эфиры холестерола — форма, в которой они
депонируются в клетках или транспортируются
кровью. В крови около 75% холестерола
находится в виде эфиров.
Используемая
литература
Березов.
Коровкин.
Северин
https://www.xumuk.ru/biochem/174.html
https://biokhimija.ru/lipidny-obmen/cholesterin.html
https://ru.wikipedia.org/wiki/%D0%A5%D0%BE%D0%BB%D0%B5%D1%81%D1%82%D0%B5%D1%80%D0%B8%D0%BD
Соседние файлы в предмете Биохимия
- #
- #
- #
- #
- #
- #
- #
Источник