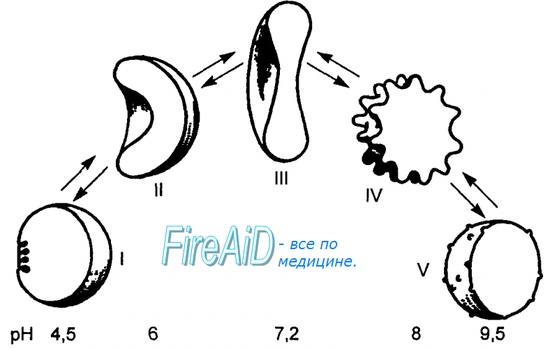
Связывание углекислого газа гемоглобином
Содержание статьи
родство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.
Оглавление темы «Вентиляция легких. Перфузия легких кровью.»: Сродство гемоглобина к кислороду. Изменение сродства гемоглобина к кислороду. Эффект Бора.Молекула гемоглобина может находиться в двух формах — напряженной и расслабленной. Расслабленная форма гемоглобина имеет свойство насыщаться кислородом в 70 раз быстрее, чем напряженная. Изменение фракций напряженной и расслабленной формы в общем количестве гемоглобина в крови обусловливает S-образный вид кривой диссоциации оксигемоглобина, а следовательно, так называемое сродство гемоглобина к кислороду. Если вероятность перехода от напряженной формы гемоглобина к расслабленной больше, то возрастает сродство гемоглобина к кислороду, и наоборот. Вероятность образования указанных фракций гемоглобина изменяется в большую или меньшую сторону под влиянием нескольких факторов. Основной фактор — это связывание кислорода с геминовой фуппой молекулы гемоглобина. При этом чем больше геминовых фупп гемоглобина связывают кислород в эритроцитах, тем более легким становится переход молекулы гемоглобина к расслабленной форме и тем выше их сродство к кислороду. Поэтому при низком Р02, что имеет место в метаболически активных тканях, сродство гемоглобина к кислороду ниже, а при высоком Р02 — выше. Как только гемоглобин захватывает кислород, повышается его сродство к кислороду и молекула гемоглобина становится насыщенной при связывании с четырьмя молекулами кислорода.
Когда эритроциты, содержащие гемоглобин, достигают тканей, то кислород из эритроцитов диффундирует в клетки. В мышцах он поступает в своеобразного депо кислорода — в молекулы миоглобина, из которого кислород используется в биологическом окислении мышц. Диффузия кислорода из гемоглобина эритроцитов в ткани обусловлена низким Р02 в тканях — 35 мм рт. ст. Внутри клеток тканей напряжение кислорода, необходимое для поддержания нормального метаболизма, составляет еще меньшую величину — не более 1 кПа. Поэтому кислород путем диффузии из капилляров достигает метаболически активных клеток. Некоторые ткани приспособлены к низкому содержанию Р02 в капиллярах крови, что компенсируется высокой плотностью капилляров на единицу объема тканей. Например, в скелетной и сердечной мышцах Р02 в капиллярах может снизиться чрезвычайно быстро во время сокращения. В мышечных клетках содержится белок миоглобин, который имеет более высокое сродство к кислороду, чем гемоглобин. Миоглобин интенсивно насыщается кислородом и способствует его диффузии из крови в скелетную и сердечную мышцы, где он обусловливает процессы биологического окисления. Эти ткани способны экстрагировать до 70 % кислорода из крови, проходящей через них, что обусловлено снижением сродства гемоглобина к кислороду под влиянием температуры тканей и рН. Эффект рН и температуры на сродство гемоглобина к кислороду. Молекулы гемоглобина способны реагировать с ионами водорода, в результате этой реакции происходит снижение сродства гемоглобина к кислороду. При насыщении гемоглобина менее 100 % низкое рН понижает связывание кислорода с гемоглобином — кривая диссоциации оксигемоглобина смещается вправо по оси х. Это изменение свойства гемоглобина под влиянием ионов водорода называется эффектом Бора. Метаболически активные ткани продуцируют кислоты, такую как молочная, и С02. Если рН плазмы крови снижается от 7,4 в норме до 7,2, что имеет место при сокращении мыщц, то концентрация кислорода в ней будет возрастать вследствие эффекта Бора. Например, при постоянном рН 7,4 кровь отдавала бы порядка 45 % кислорода, т. е. насыщение гемоглобина кислородом снижалось до 55 %. Однако когда рН снижается до 7,2, кривая диссоциации смещается по оси х вправо. В результате насыщение гемоглобина кислородом падает до 40 %, т. е. кровь может отдавать в тканях до 60 % кислорода, что на 1/з больше, чем при постоянном рН.
Метаболически активные ткани повышают продукцию тепла. Повышение температуры тканей при физической работе изменяет соотношение фракций гемоглобина в эритроцитах и вызывает смещение кривой диссоциации оксигемоглобина вправо вдоль оси х. В результате большее количество кислорода будет освобождаться из гемоглобина эритроцитов и поступать в ткани. Эффект 2,3-дифосфоглицерата (2,3-ДФГ) на сродство гемоглобина к кислороду. При некоторых физиологических состояниях, например при понижении Р02 в крови ниже нормы (гипоксия) в результате пребывания человека на большой высоте над уровнем моря, снабжение тканей кислородом становится недостаточным. При гипоксии может понижаться сродство гемоглобина к кислороду вследствие увеличения содержания в эритроцитах 2,3-ДФГ. В отличие от эффекта Бора, уменьшение сродства гемоглобина к кислороду под влиянием 2,3-ДФГ не является обратимым в капиллярах легких. Однако при движении крови через капилляры легких эффект 2,3-ДФГ на снижение образования оксигемоглобина в эритроцитах (плоская часть кривой диссоциации оксигемоглобина) выражен в меньшей степени, чем отдача кислорода под влиянием 2,3-ДФГ в тканях (наклонная часть кривой), что обусловливает нормальное кислородное снабжение тканей. — Также рекомендуем «Углекислый газ. Транспорт углекислого газа.» |
Источник
Связывание гемоглобина с оксидом углерода
Оксид углерода (угарный газ, СО) обладает гораздо большим сродством к гемоглобину, чем кислород. Даже при крайне низких парциальных давлениях СО гемоглобин превращается в карбоксигемоглобин: Нb+СО Þ НbСО. Равновесие этой реакции значительно смещено вправо, поэтому кривая диссоциации карбоксигемоглобина имеет очень крутой наклон. Высокое сродство оксида углерода к гемоглобину обусловлено тем, что СО диссоциирует от НЬ гораздо медленнее, чем О2. Максимально эффективная концентрация для СО составляет 30 частей на миллион, что соответствует 0,003 объемных %. В артериальной крови человека, пребывающего достаточно долго в среде с таким содержанием СО, на долю НЬСО приходится около 5% общего содержания гемоглобина. Парциальные давления СО и О2, при которых содержание соответственно НbСО и НbО2 составляет по 5%, соотносятся как 1:350. Иными словами, в данных пределах парциальных давлений сродство Нb к СО примерно в 35O раз выше, чем к О2.
Токсичность оксида углерода обусловлена именно высоким сродством этого соединения к гемоглобину. СО представляет собой газ без цвета и запаха, образующийся при неполном сгорании органических веществ. Иногда он входит в состав бытового газа; кроме того, он выделяется при работе двигателей внутреннего сгорания. Даже при низких концентрациях СО вытесняет кислород из соединения с гемоглобином, при этом последний теряет способность к переносу О2. В норме на долю НbСО приходится лишь 1% общего количества гемоглобина в крови; у курильщиков же к вечеру она достигает 20%. Об опасности, которую угарный газ представляет для автомобилистов, говорит тот факт, что на дорогах с особенно интенсивным движением содержание СО в воздухе достигает 3-10 ч. При такой концентрации СО шахтерам положено надевать дыхательные аппараты.
Токсичность угарного газа обусловлена не только блокированием гемоглобина, но и другим эффектом. Когда часть гемоглобина превращается в НbСО, кривая диссоциации оксигемоглобина (для гемоглобина, еще не блокированного СО) сдвигается влево и может в итоге приобретать форму гиперболы. В результате происходит еще большее снижение напряжения О2 в тканевых капиллярах.
При тяжелом отравлении угарным газом, отличительным признаком которого служит вишнево-красная окраска крови, жизнь пострадавшего можно спасти путем немедленного применения искусственного дыхания, по возможности с чистым кислородом. При этом напряжение кислорода в крови увеличивается, и О2 частично вытесняет СО из связи с гемоглобином. Рекомендуется также переливание большого количества крови, так как при этом в кровь пострадавшего поступает гемоглобин, способный переносить кислород.
Перенос СО2 кровью. Формы транспорта СО2.
Диоксид углерода (СО2, углекислый газ) ― конечный продукт окислительного метаболизма в клетках ― переносится с кровью к легким и удаляется через них во внешнюю среду. Подобно кислороду, диоксид углерода может переноситься как в физически растворенном виде, так и в составе химических соединений. Химическое связывание СО2 ―более сложный процесс по сравнению со связыванием кислорода. Это обусловлено тем, что механизм, отвечающий за транспорт СО2, должен одновременно обеспечивать поддержание постоянства кислотно-щелочного равновесия крови и тем самым внутренней среды организма в целом.
Связывание СО2. Напряжение СО2 в артериальной крови, поступающей в тканевые капилляры, составляет 40 мм рт.ст. (5,3 кПа). В клетках же, расположенных около этих капилляров, напряжение СО2 значительно выше, так как углекислый газ постоянно образуется в процессе метаболизма. В связи с этим физически растворенный СО2 диффундирует по градиенту напряжения из тканей в капилляры. Здесь некоторое количество углекислого газа остается в растворенном состоянии, но большая часть СО2 претерпевает ряд химических превращений. Прежде всего, происходит гидратация молекул СО2 с образованием угольной кислоты, сразу же диссоциирующей на ион бикарбоната и протон:
В плазме крови эта реакция протекает очень медленно; в эритроците же она ускорена примерно в 10 тыс. раз. Это связано с действием фермента карбоангидразы. Поскольку этот фермент присутствует только в эритроцитах, практически все молекулы СО2, участвующие в реакции гидратации, должны сначала проникнуть в эритроциты.
Роль разных форм СО2 в газообмене. В крови, поступающей к тканям, напряжение СО2 составляет 40 мм рт.ст. Проходя через них, кровь насыщается углекислым газом, и напряжение его в оттекающей из тканей крови достигает в среднем 46 мм рт.ст. При этом 1 л крови поглощает примерно 1,8 ммоль СО2. Около 12% этого количества остается в физически растворенном виде или в форме недиссоциированной угольной кислоты, 11% образует карбаминовое соединение с гемоглобином, 27% транспортируется в виде бикарбоната в эритроцитах, а остальное количество ― около 50% ― растворено в виде НСО3¯ в плазме. При прохождении крови через легкие СО2 высвобождается из этих четырех форм в таком же соотношении.
Сатурационные кривые СО2
Зависимость содержания СО2 от его напряжения. Общее содержание диоксида углерода в крови складывается из концентраций физически растворенного и форм химически связанного СО2 ― угольной кислоты, карбамата и бикарбоната. Большая часть СО2 присутствует внутри и вне эритроцитов в форме бикарбоната. При повышении РСО2 содержание всех этих форм СО2 увеличивается.
Связь между концентрацией в крови и парциальным давлением СО2 описывается сатурационной кривой, сходной с кривой диссоциации оксигемоглобина. Зависимость связывания СО2 от степени оксигенации гемоглобина называют эффектом Христиансена-Дугласа-Холдена «или кратко эффектом Холдена.
Существует принципиальная разница между сатурационными кривыми связывания СО2 и кривыми диссоциации оксигемоглобина. Кривые диссоциации НbО2 асимптотически приближаются к максимуму, а связывание СО2 не достигает насыщения. По мере увеличения парциального давления СО2 количество связанного СО2 постоянно возрастает, так как образование бикарбоната в крови практически не лимитировано.
Физиологическое значение эффекта Христиансена-Дугласа-Холдена. При рассмотрении процессов поступления СО2 в кровь из тканей и его высвобождения в легких следует помнить о том, что эти процессы происходят одновременно с обменом О2. Изменения в насыщении гемоглобина кислородом влияют на связывание СО2 кровью и тем самым на его обмен.
К тканевым капиллярам обычно притекает полностью оксигенированная кровь. По мере того как кровь проходит через капилляры и кислород выходит из нее в ткани, способность крови поглощать СО2 увеличивается. Таким образом, эффект Христиансена-Дугласа-Холдена способствует поглощению СО2 кровью в тканях. В легких происходят обратные процессы. В результате того, что в кровь поступает кислород, ее сродство к углекислому газу снижается, и тем самым облегчается диффузия СО2 в альвеолы. Итак, мы убедились в том, что как при поступлении СО2 в кровь из тканей, так и при выделении его в легких эффект Христиансена-Дугласа-Холдена способствует диффузионному обмену этого газа.
Источник
Транспорт углекислого газа кровью
Из венозной крови можно извлечь 55—58 об.%
углекислого газа. Большая часть СО2, извлекаемого из
крови, происходит из имеющихся в плазме и эритроцитах солей угольной кислоты и
только около 2,5 об.% углекислого газа растворено и около 4—5об.% находится в
соединении с гемоглобином в виде карбогемоглобина.
Образованно угольной кислоты из углекислого газа происходит в эритроцитах,
где содержится фермент карбоангидраза, являющийся мощным катализатором,
ускоряющим реакцию гидратации СО2.
Карбоангидраза. Существование этого
фермента предполагал еще И. М. Сеченов, но открыт он был лишь в 1932 г.
Мелдрумом и Рафтоном.
Связывание углекислого газа кровью в капиллярах большого круга.
Углекислый газ, образующийся в тканях, диффундирует в кровь кровеносных
капилляров, так как напряжение СО2 в тканях значительно превышает его
напряжение в артериальной крови. Растворяющийся в плазме СО2
диффундирует внутрь эритроцита, где под влиянием карбоангидразы он мгновенно
превращается в угольную кислоту,
Согласно расчетам, активность карбоангидразы в эритроцитах такова, что
реакция гидратации углекислоты ускоряется в 1500—2000 раз. Так как весь
углекислый газ внутри эритроцита превращается в угольную кислоту, то напряжение
СО2 внутри эритроцита близко к нулю, поэтому все новые и новые
количества СО2 поступают внутрь эритроцита. В связи с образованием
угольной кислоты из СО3 в эритроците концентрация ионов
НСО3′ возрастает, и они начинают диффундировать в плазму. Это
возможно потому, что поверхностная мембрана эритроцита проницаема для анионов.
Для катионов мембрана эритроцита практически непроницаема. Взамен ионов
НСО3′ в эритроциты входит ион хлора. Переход ионов хлора из плазмы
внутрь эритроцита освобождает в плазме ионы натрия, которые связывают
поступающие нз эритроцита ионы НСО3, образуя NaHCО3
Химический анализ плазмы венозной крови показывает значительное увеличение в ней
бикарбоната.
Накопление внутри эритроцита анионов приводит к повышению осмотического
давления внутри эритроцита, а это вызывает переход воды из плазмы через
поверхностную мембрану эритроцита. В результате объем эритроцитов в капиллярах
большого круга увеличивается. При исследовании с помощью гематокрнта
установлено, что эритроциты занимают 40% объема артериальной крови и 40,4%
объема венозной крови. Из этого следует, что объем эритроцитов венозной крови
больше, чем эритроцитом артериальной, что объясняется проникновением в них
воды.
Одновременно с поступлением СО2 внутрь эритроцита и образованием в
нем угольной кислоты происходит отдача кислорода оксигемоглобином и превращение
его в редуцированный гемоглобин. Последний является значительно менее
диссоциирующей кислотой, чем оксигемоглобин и угольная кислота. Поэтому при
превращении оксигемоглобина в гемоглобин Н2СО3 вытесняет
из гемоглобина ионы калия и, соединяясь с ними, образует калиевую соль
бикарбоната.
Освобождающийся Н˙ ион угольной кислоты связывается гемоглобином. Так как
редуцированный гемоглобин является малодиссоциированной кислотой, то при этом не
происходит закисления крови и разница рН венозной и артериальной крови крайне
невелика. Происходящую в эритроцитах тканевых капилляров реакцию можно
представить следующим образом:
КНbO2 + Н2СO3= HHb +
O2 + КНСO3
Из изложенного следует, что оксигемоглобин, превращаясь в гемоглобин и
отдавая связанные им основания углекислоте, способствует образованию бикарбоната
и транспорту в таком виде углекислоты. Кроме того, гкмоглобин образует
химическое соединение с СО2 — карбогемоглобин. Наличие в крови
соединения гемоглобина с углекислым газом было установлено путем следующего
опыта. Если к цельной крови прибавить цианистый калий, который полностью
инактивирует карбоангидразу, то оказывается, что эритроциты такой крови
связывают больше СО2, чем плазма. Отсюда был сделан вывод, что
связывание СО2 эритроцитами после инактивирования карбоангидразы
объясняется наличием в эритроцитах соединения гемоглобина с СО2. В
дальнейшем выяснилось, что СО2 присоединяется к аминной группе
гемоглобина, образуя так называемую карбаминовую связь.
Реакция образования карбогемоглобина может идти в одну или другую сторону в
зависимости от напряжения углекислого газа в крови. Хотя небольшая часть всего
количества углекислого газа, которое может быть извлечено из крови, находится в
соединении с гемоглобином (8—10%), однако роль этого соединения в транспорте
углекислоты кровью достаточно велика. Примерно 25—30% углекислого газа,
поглощаемого кровью в капиллярах большого круга, вступает в соединение с
гемоглобином, образуя карбогемоглобин.
Отдача СО2 кровью в легочных капиллярах. Вследствие более низкого
парциального давления СО2 в альвеолярном воздухе по сравнению с
напряжением его в венозной крови углекислый газ переходит путем диффузии из
крови легочных капилляров в альвеолярный воздух. Напряжение СО2 в
крови падает.
Одновременно с этим вследствие более высокого парциального давления ННb + O2 + КНСO3= Освободившаяся из своей связи с основаниями угольная кислота Так как в легочных капиллярах уменьшается в эритроцитах концентрация Схематически все эти процессы приведены на рис. 57. Рис. 57. Схема процессов, происходящих в эритроците при поглощении |
Кривые диссоциации соединений угольной кислоты в крови. Как мы уже
говорили, свыше 85% углекислого газа, которое может быть извлечено из крови
подкислении ее, освобождается в результате расщепления бикарбонатов (калия в
эритроцитах и натрия в плазме).
Связывание углекислого газа и отдача его кровью зависят от его парциального
напряжения. Можно построить кривые диссоциации соединений углекислоты в крови,
подобные кривым диссоциации оксигемоглобина. Для этого по оси ординат
откладывают объемные проценты связанного кровью углекислого газа, а по оси
абсцисс— парциальные напряжения углекислого газа. Нижняя кривая на рис. 58
показывает связывание углекислого газа артериальной кровью, гемоглобин
которой почти полностью насыщен кислородом. Верхняя кривая показывает связывание
кислого газа венозной кровью.
Различие в высоте этих кривых зависит от того, что артериальная кровь, Рис. 58. Кривые поглощения углекислого газа кровью |
Точка А на нижней кривой на рис. 58 соответствует напряжению
кислоты, равному 40 мм рт. ст., т. е. тому напряжению, которое фактически
имеется в артериальной крови. При таком напряжении связано 52 об.%
СО2. Точка V на верхней кривой соответствует напряжению кислого газа
46 мм рт. ст., т. е. фактически имеющемуся в венозной крови. Как видно из
кривой, при таком напряжении венозная кровь связывает 58 об.% углекислого газа.
Линия AV, соединяющая верхнюю и нижнюю кривую, соответствует тем изменениям
способности связывать углекислый газ, которые происходят при превращении
артериальной крови в венозную или, наоборот, венозной крови в артериальную.
Венозная кровь благодаря тому, что содержащийся в ней гемоглобин переходит в
оксигемоглобин, в капиллярах легких отдает около 6 об.% СО2. Если бы
в легких гемоглобин не превращался в оксигемоглобин, то, как видно из кривой,
венозная кровь при имеющемся в альвеолах парциальном давлении углекислого газа,
равном 40 мм рт. ст.. связывала бы 54 об.% СО2, следовательно, отдала
бы не 6, а только 4об.%. Равным образом, если бы артериальная кровь в капиллярах
большого круга не отдавала своего кислорода, т. е. если бы гемоглобин ее
оставался насыщенным кислородом, то эта артериальная кровь при парциальпом
давлении углекислого газа, имеющемся в капиллярах тканей тела, смогла бы связат
не 58 об.% СО2, а лишь 55 об.%.
Таким образом, переход гемоглобина в оксигемоглобин в легких и
оксигемоглобина в гемоглобин в тканях тела способствует поглощению и отдаче
примерно 3—4 об.% углекислого газа из тех 6 об.%, которые поглощает кровь в
тканях и отдает в легких. Около 25—30% выделяемого в легких углекислого газа
переносится карбогемоглобином.
Из всего сказанного вытекает, что в механизме транспорта и кислорода, и
углекислого газа кровью важнейшая роль принадлежит эритроцитам, в которых
содержатся гемоглобин и карбоангидраза.
Источник