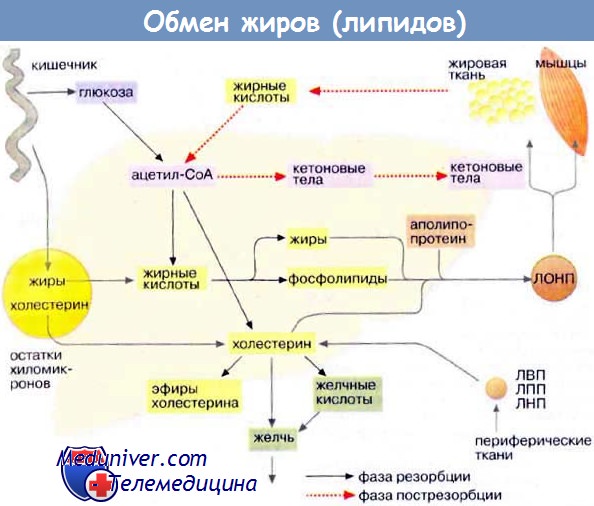
Транспорт холестерина и липидов
Содержание статьи
Холестерол используется как переносчик полиненасыщенных жирных кислот
Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.
Липопротеины высокой плотности
Общая характеристика
- образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника,
- в составе частицы примерно половину занимают белки, еще четверть фосфолипиды, остальное холестерин и ТАГ (50% белка, 25% ФЛ, 13% эфиров ХС и 5% свободного ХС, 7% ТАГ),
- структурным апобелком является апо А1, также содержат апоЕ и апоСII.
Функция
- Транспорт свободного ХС от тканей к печени.
- Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.
Метаболизм
1. Синтезированные в печени частицы (насцентные или первичные ЛПВП) содержат в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в ЛПВП по мере метаболизма в плазме крови.
Новосинтезированные ЛПВП выглядят на электронных микрофотографиях как двухслойные диски из двух монослоев фосфолипидов (таблеткообразная форма). Синтез апоЕ и апоС происходит главным образом в печени, в отличие от апо А-I, образующегося как в печени, так и в тонком кишечнике.
2-3. В плазме крови насцентный ЛПВП сначала превращается в ЛПВП3 (условно его можно назвать «зрелый»). В этом превращении главным является то, что ЛПВП
- забирает от клеточных мембран свободный холестерин при непосредственном контакте или при участии специфических транспортных белков,
- взаимодействуя с мембранами клеток, отдает им часть фосфолипидов из своей оболочки, доставляя таким образом полиеновые жирные кислоты в клетки,
- тесно взаимодействует с ЛПНП и ЛПОНП, получая от них свободный холестерин. В обмен ЛПВП3 отдают эфиры ХС, образованные благодаря переносу жирной кислоты от фосфатидилхолина (ФХ) на холестерин (ЛХАТ-реакция, см п.4).
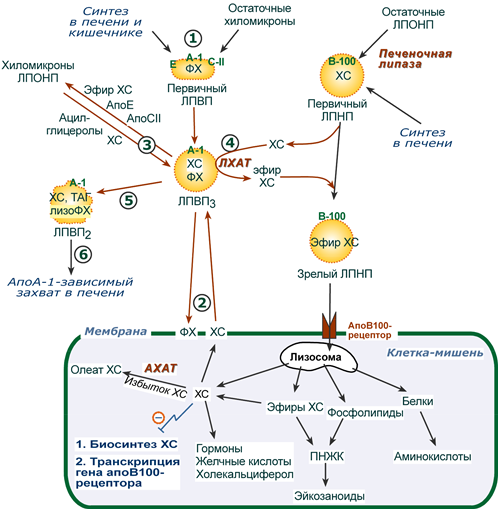
Транспорт холестерола и его эфиров в организме
(цифры соответствуют пунктам метаболизма ЛПВП по тексту)
4. Внутри ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от 2-го положения фосфатидилхолина (из оболочки самого ЛПВП) на получаемый свободный холестерин с образованием лизофосфатидилхолина (лизоФХ) и эфиров ХС. ЛизоФХ остается внутри ЛПВП, эфир холестерина отправляется в ЛПНП.
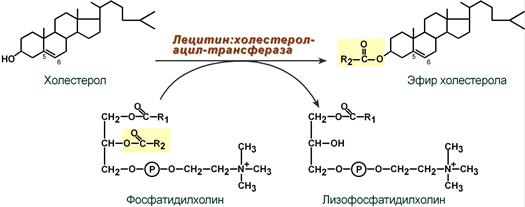
Реакция этерификации холестерола
при участии лецитин:холестерол-ацилтрансферазы
5. В результате первичный ЛПВП постепенно, через зрелую форму ЛПВП3, преобразуется в ЛПВП2 (остаточный, ремнантный). При этом происходят и дополнительные события:
- взаимодействуя с разными формами ЛПОНП и ХМ, ЛПВП получают ацил-глицеролы (МАГ, ДАГ, ТАГ), и обмениваются холестерином и его эфирами,
- ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм.
Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются.
6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается.
Липопротеины низкой плотности
Общая характеристика
- образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП,
- в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов),
- основным апобелком является апоВ-100,
- нормальное содержание в крови 3,2-4,5 г/л,
- самые атерогенные.
Функция
1. Транспорт холестерола в клетки, использующих его
- для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников),
- для превращения в холекальциферол (кожа),
- для образования желчных кислот (печень),
- для выведения в составе желчи (печень).
2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.
Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола.
Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.
Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения.
Также в мембраны всех клеток, как сказано выше (см «Метаболизм ЛПВП»), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП.
Метаболизм
1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и «выталкивание» белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый.
2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами.
3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
- ХС превращается в гормоны или включается в состав мембран,
- излишки мембранного ХС удаляются с помощью ЛПВП,
- принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов.
- при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция),
Синтез олеата холестерола при участии
ацил-SKoA-холестерол-ацилтрансферазы
На количество апоВ-100-рецепторов влияют гормоны:
- инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов,
- глюкокортикоиды уменьшают их количество.
Источник
ОБМЕН, РОЛЬ И ТРАНСПОРТ ХОЛЕСТЕРИНА — Студопедия
В сутки в организме синтезируется около 1 г холестерина (рис.10). Основное место синтеза – печень (до 80%), меньше синтезируется в кишечнике, коже и других тканях. С пищей поступает около 0,4 г холестерина, его источником является только пища животного происхождения. Холестерин необходим для построения всех мембран, в печени из него синтезируются желчные кислоты, в эндокринных железах – стероидные гормоны, в коже – витамин Д.
Рис.10 Холестерин
Сложный путь синтеза холестерина можно поделить на 3 этапа (рис.11). Первый этап заканчивается образованием мевалоновой кислоты. Источником для синтеза холестерина служит ацетил-КоА. Сначала из 3 молекул ацетил-КоА образуется ГМГ-КоА – общий предшественник в синтезе холестерина и кетоновых тел (однако реакции синтеза кетоновых тел происходят в митохондриях печени, а реакции синтеза холестерина – в цитозоле клеток). Затем ГМГ-КоА под действием ГМГ-КоА-редуктазы восстанавливается до мевалоновой кислоты с использованием 2 молекул НАДФН. Эта реакция является регуляторной в синтезе холестерина. Синтез холестерина тормозит сам холестерин, желчные кислоты и гормон голода глюкагон. Усиливается синтез холестерина при стрессе катехоламинами.
На втором этапе синтеза из 6 молекул мевалоновой кислоты образуется углеводород сквален, имеющий линейную структуру и состоящий из 30 атомов углерода.
На третьем этапе синтеза происходит циклизация углеводородной цепи и отщепление 3 атомов углерода, поэтому холестерин содержит 27 углеродных атомов. Холестерин является гидрофобной молекулой, поэтому транспортируется кровью только в составе разных липопротеинов.
Рис. 11 Синтез холестерина
Липопротеины – липид-белковые комплексы, предназначенные для транспорта нерастворимых в водных средах липидов по крови (рис.12). Снаружи липопротеины (ЛП) имеют гидрофильную оболочку, которая состоит из молекул белков и гидрофильных групп фосфолипидов. Внутри ЛП находятся гидрофобные части фосфолипидов, нерастворимые молекулы холестерина, его эфиров, молекулы жиров. ЛП делятся (по плотности и подвижности в электрическом поле) на 4 класса. Плотность ЛП определяется соотношением белков и липидов. Чем больше белка, тем больше плотность и тем меньше размер.
Рис.12. Строение липопротеидов
· 1 класс – хиломикроны (ХМ). Содержат 2% белка и 98% липидов, среди липидов преобладают экзогенные жиры, переносят экзогенные жиры от кишечника к органам и тканям, синтезируются в кишечнике, в крови присутствуют непостоянно – только после переваривания и всасывания жирной пищи.
· 2 класс – ЛП очень низкой плотности (ЛПОНП) или пре-b-ЛП. Белка в них 10%, липидов – 90%, среди липидов преобладают эндогенные жиры, транспортируют эндогенные жиры из печени в жировую ткань. Основное место синтеза – печень, небольшой вклад вносит тонкий кишечник.
· 3 класс – ЛП низкой плотности (ЛПНП) или b-ЛП. Белка в них 22% , липидов – 78%, среди липидов преобладает холестерин. Нагружают клетки холестерином, поэтому их называют атерогенными, т.е. способствующими развитию атеросклероза (АС). Образуются непосредственно в плазме крови из ЛПОНП под действием фермента ЛП-липазы.
· 4 класс ЛП высокой плотности (ЛПВП) или a-ЛП. Белка и липидов содержат по 50%, среди липидов преобладают фосфолипиды и холестерин. Разгружают клетки от избытка холестерина, поэтому являются антиатерогенными, т.е. препятствующими развитию АС. Основное место их синтеза – печень, небольшой вклад вносит тонкий кишечник.
Транспорт холестерина липопротеинами.
Печень является основнымместом синтеза холестерина. Холестерин, синтезированный в печени, упаковывается в ЛПОНП и в их составе секретируется в кровь. В крови на них действует ЛП-липаза, под влиянием которой ЛПОНП переходят в ЛПНП. Таким образом, ЛПНП становятся основной транспортной формой холестерина, в которой он доставляется к тканям. ЛПНП могут попадать в клетки двумя путями: рецепторным и нерецепторным захватом. Большинство клеток на своей поверхности имеют рецепторы к ЛПНП. Образовавшийся комплекс рецептор-ЛПНП эндоцитозом попадает внутрь клетки, где распадается на рецептор и ЛПНП. Из ЛПНП при участии лизосомальных ферментов освобождается холестерин. Этот холестерин используется для обновления мембран, тормозит синтез холестерина данной клеткой, а также, если количество холестерина, поступающего в клетку, превышает ее потребность, то подавляется и синтез рецепторов к ЛПНП.
Это уменьшает поток холестерина из крови в клетки, таким образом, клетки, для которых характерен рецепторный захват ЛПНП, имеют механизм, который ограждает их от избытка холестерина. Для гладкомышечных клеток сосудов и макрофагов характерен нерецепторный захват ЛПНП из крови. В эти клетки ЛПНП, а значит, и холестерин попадают диффузно, то есть, чем их больше в крови, тем больше их попадает в эти клетки. Эти разновидности клеток не имеют механизма, который ограждал бы их от избытка холестерина. В «обратном транспорте холестерина» от клеток участвуют ЛПВП. Они забирают избыток холестерина из клеток и возвращают его обратно в печень. Холестерин выводится с калом в виде желчных кислот, часть холестерина в составе желчи попадает в кишечник и также выводится с калом.
Источник
Транспорт липидов
Жиры гидрофобны, поэтому существуют специальные механизмы их транспорта в крови. Свободные (неэстерифицированные) жирные кислоты переносятся кровью в виде комплексов с альбуминами. Холестерол, его эфиры, триацилглицеролы, фосфолипиды транспортируются в составе липопротеинов.
Липопротеины являются молекулярными комплексами, состоящими из липидов и белков.
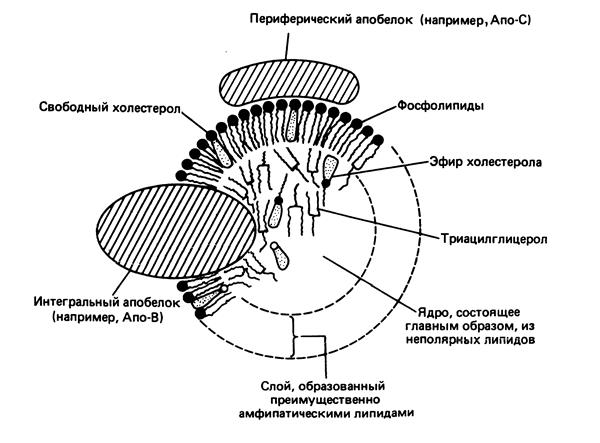
Рис. 10.2. Строение липопротеина
Существует несколько классов липопротеинов (ЛП), но всех их объединяют следующие особенности: 1) поверхностный слой липопротеинов состоит из фосфолипидов, свободного холестерола и белков; 2) каждый липопротеин содержит особый набор поверхностных белков — аполипопротеинов (апо), которые обозначаются буквами латинского алфавита (А,В,С); 3) сердцевина (ядро) липопротеина состоит из гидрофобных триацилглицеролов, эфиров холестерола (рис. 10.2 ).
Аполипопротеины выполняют следующие функции: 1) являются структурными компонентами липопротеинов; 2) участвуют в узнавании и взаимодействии с рецепторами мембран; 3) активируют ферменты метаболизма липопротеинов.
Липопротеины подразделяются на 4 основные класса в зависимости от плотности (определяемой с помощью ультрацентрифугирования) и электрофоретической подвижности (табл. 10.1).
Таблица 10.1.
Классификация липопротеинов по методу разделения
| Класс | Ультрацентрифугирование | Электрофорез |
| Хиломикроны | Хиломикроны | Хиломикроны |
| Липопротеины очень низкой плотности | ЛПОНП (VLDL) | пре-b-ЛП |
| Липопротеины низкой плотности | ЛПНП (LDL) | b-ЛП |
| Липопротеины высокой плотности | ЛПВП (HDL) | a-ЛП |
Основные параметры и состав липопротеинов представлен в табл. 10.2.
Хиломикроны (ХМ) – самые крупные частицы. ХМ синтезируются в слизистой кишечника и участвуют в экзогенном транспорте пищевых липидов к различным тканям. Основным липидом являются триацилглицеролы.
ЛПОНПсинтезируются в печени. Основным липидом являются триацилглицеролы. Основная функция – транспорт эндогенных липидов из печени в периферические ткани.
ЛПНП образуются в кровеносном русле из ЛПОНП. Содержат много холестерола (основной транспортер холестерола), который транспортируется в периферические ткани.
ЛПВП образуются в печени, содержат много фосфолипидов и белков; у этих ЛП компоненты оболочки преобладают над сердцевиной.
Таблица 10.2
Состав липопротеинов
| Липопротеины | Молекулярная массы, Да | Диаметр, нм | Состав, % | |||
| белок | ТГ | ФЛ | ХС | |||
| Хиломикроны | 1-10 млн. | 100-1000 | 1-2 | 88-90 | 4-7 | 5-6 |
| ЛПОНП | 5-100 тыс. | 30-90 | 7-10 | 50-56 | 20-23 | |
| ЛПНП | 2-4 млн. | 20-25 | 20-21 | 10-13 | 21-24 | 45-47 |
| ЛПВП | 200-400 тыс. | 10-15 | 35-50 | 5-8 | 30-43 | 20-35 |
ТГ – триацилглицеролы, ФЛ – фосфолипиды. ХС — холестерол
Различают экзогенный (транспорт пищевых липидов) и эндогенный (транспорт липидов, синтезированных в организме) транспорт.
Экзогенный транспорт. Продукты переваривания липидов всасываются в клетки слизистой оболочки кишечника в составе мицелл. Жирные кислоты с числом углеродных атомов <12 всасываются в кровь и по воротной вене транспортируются в печень. Длинноцепочечные жирные кислоты (С >12) в клетках кишечника реэстерифицируются в триацилглицеролы, которые по составу напоминают пищевые жиры. Полученные триацилглицеролы вместе с фосфолипидами, холестеролом и белками (2%) образуют хиломикроны. Хиломикроны содержат апопротеин В48 и апоА.
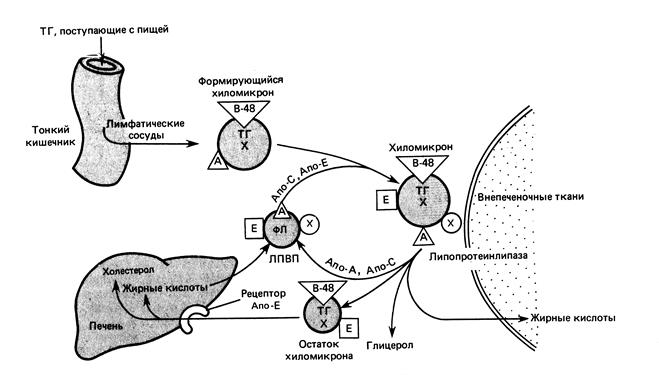
Рис. 10.3. Экзогенный транспорт липидов (по Марри Р. и др., 2004)
Хиломикроны поступают в лимфу. В крови встречаются с частицами ЛПВП, содержащими апоЕ и апоС. Хиломикроны отдают апоА частицам ЛПВП, а взамен приобретают апоЕ и апоС. Один из аполипопротеинов группы С — апоСII — служит активатором фермента липопротеинлипазы (ЛПЛ). Этот фермент синтезируется и секретируется жировой и мышечной тканями, клетками молочных желез. Секретируемый фермент прикрепляется к плазматической мембране эндотелиальных клеток капилляров тех тканей, где он синтезировался. АпоСII, находящийся на поверхности ХМ, активирует ЛПЛ. Она гидролизирует триацилглицеролы в составе ХМ до глицерола и жирных кислот. Эти жирные кислоты либо поступают в клетки жировой и мышечной ткани, либо соединяются с альбуминами плазмы. В результате действия ЛПЛ хиломикроны резко уменьшаются в размерах и их называют ремнанты (остаток). Ремнанты ХМ рецепторным путем захватываются печенью (рис. 10.3).
Эндогенный транспорт. В клетках печени ресинтезируются триацилглицеролы и фосфолипиды, которые характерны для данного организма. Они включаются в состав ЛПОНП. В состав ЛПОНП входят апоВ100 и апоС. Это основная транспортная форма триацилглицеролов. В другой класс липопротеинов, образуемых в печени — ЛПВП входят холестерол, фосфолипиды, апоА. Эти частицы плоские и их называют — насцентные ЛПВП. (В их ядре нет гидрофобных молекул). Эти ЛПВП играют большую роль в обратном транспорте холестерола из клеток периферических тканей в печень.
В капиллярах жировой и мышечной тканей апоСII ЛПОНП активирует ЛПЛ, которая катализирует гидролиз триацилглицеролов ЛПОНП и превращает их в ЛППП (липопротеины промежуточной плотности). ЛППП под действием синтезированной в печени циркулирующей печеночной триацилглицероллипазы, теряют еще часть триацилглицеролов и превращаются в ЛПНП. Основным липидом ЛПНП становится холестерол, который в составе ЛПНП переносится к клеткам всех тканей. Следовательно, ЛПНП образуются непосредственно в сосудистом русле (рис. 10.4).
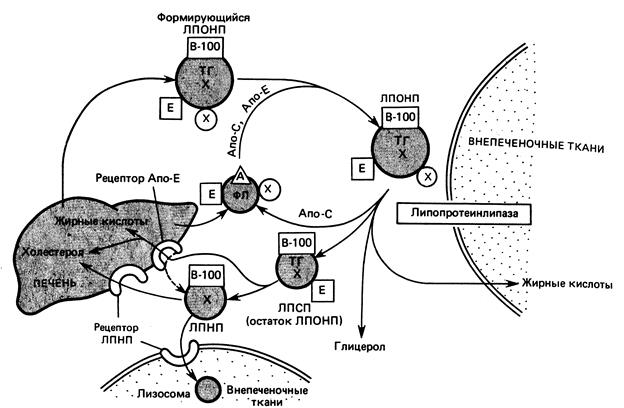
Рис. 10.4. Эндогенный транспорт липидов (по Марри Р. и др., 2004)
Итак, в результате экзогенного и эндогенного транспорта в капиллярах жировой и мышечной тканей освобождаются жирные кислоты и глицерол. Жирные кислоты связываются с альбуминами и транспортируются к тканям-потребителям.
Источник
етаболизм жиров в организме. Транспорт липидов
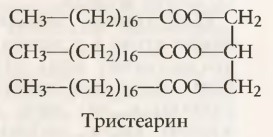
Метаболизм жиров в организме. Транспорт липидовНекоторые химические вещества, входящие в состав пищи и тканей тела, классифицируют как липиды. К ним относят: (1) нейтральные жиры, известные как триглицериды; (2) фосфолипиды; (3) холестерол; (4) некоторые другие вещества, менее важные. Основной частью химической структуры триглицеридов и фосфолипидов являются жирные кислоты, представляющие собой простые углеводородные органические кислоты с длинной цепочкой. Так, типичная жирная кислота — пальмитиновая, она может быть представлена как СН3(СН2)14СООН. Холестерол не содержит жирных кислот, но его стерольное ядро образовано частью молекулы жирной кислоты, что обусловливает его физические и химические свойства, характерные для вещества, относящегося к липидам. Организм использует триглицериды главным образом в качестве источника энергии для различных метаболических процессов, что функционально роднит их с углеводами. Однако некоторые липиды, особенно холестерол, фосфолипиды и небольшая часть триглицеридов, используются организмом в формировании мембран и прочих структурных компонентов клеток, т.е. выполняют пластические функции. а) Основа химического строения триглицеридов (нейтральных жиров). Поскольку в данных статьях по физиологии на сайте по большей части рассматриваются вопросы, связанные с использованием триглицеридов в качестве источника энергии, необходимо создать представление о химической структуре этих веществ.
Обратите внимание, что 3 молекулы жирных кислот с длинной цепочкой связаны с 1 молекулой глицерола, образуя типичную структуру триглицерида. В образовании триглицеридов в организме человека чаще всего участвуют три жирные кислоты: (1) стеариновая кислота (см. формулу тристеарина), которая включает цепочку из 18 углеродных фрагментов с полностью насыщенными водородом связями; (2) олеиновая кислота, также состоящая из 18-углеродной цепочки, но имеющей одну двойную связь в середине цепочки; (3) пальмитиновая кислота, включающая 16 атомов углерода с полностью насыщенными связями. б) Транспорт липидов в жидких средах организма. Транспорт триглицеридов и других липидов из желудочно-кишечного тракта посредством лимфы. Хиломикроны. Почти все жиры, присутствующие в пище, за исключением жиров, содержащих жирные кислоты с короткой цепочкой, всасываются из кишечника в лимфу. Во время пищеварения большинство триглицеридов расщепляются до моноглицеридов и жирных кислот. Затем во время прохождения через эпителиоциты кишечника моноглицериды и жирные кислоты ресинтезируются в новые молекулы триглицеридов, которые попадают в лимфу в виде мелкодисперсных капелек, названных хиломикронами. Диаметр хиломикронов колеблется от 0,08 до 0,6 мкм. Небольшие количества апопротеина В абсорбируются на наружной поверхности хиломикронов. Часть молекулы белка, оставшаяся свободной, выступает в водную фазу, что увеличивает суспензионную стабильность хиломикронов в лимфе и препятствует их прилипанию к стенкам лимфатических сосудов. Большая часть холестерола и фосфолипидов, всасываемых из желудочно-кишечного тракта, входит в состав хиломикронов. Таким образом, хиломикроны состоят главным образом из триглицеридов, а также содержат 9% фосфолипидов, 3% холестерола и около 1% апопротеина В. Образующиеся хиломикроны затем транспортируются вверх по грудному протоку и вместе с лимфой попадают в кровеносную систему в области впадения яремной и подключичной вен.
в) Извлечение хиломикронов из крови. Почти через час после приема пищи, содержащей большое количество жира, концентрация хиломикронов в плазме может увеличиться и составить от 1 до 2% общего количества плазмы. Из-за больших размеров хиломикронов плазма становится мутной и иногда желтой, но поскольку период полураспада хиломикронов составляет меньше 1 ч, плазма вновь становится прозрачной через несколько часов. Жиры, содержащиеся в хиломикронах, извлекаются следующим образом. 1. Триглицериды хиломикронов гидролизуются липопротеинлипазой. Жиры хранятся в клетках жировой ткани и клетках печени. Большая часть хиломикронов извлекается из циркулирующей крови во время прохождения по капиллярам жировой ткани или печени. Как жировая ткань, так и печень содержат большое количество фермента липопротеинлипазы. Этот фермент особенно активен в эндотелии капилляров, где он гидролизует триглицериды хиломикронов, когда те контактируют с эндотелием капиллярной стенки, что приводит к высвобождению жирных кислот и глицерола. Жирные кислоты, обладая способностью проникать через мембраны клеток, легко диффундируют через мембраны адипоцитов жировой ткани в клетки печени. Оказавшись внутри клеток, жирные кислоты вновь превращаются в триглицериды, взаимодействуя с глицеролом, образующимся в результате метаболических процессов в клетках, выполняющих функции депонирования (что будет рассмотрено далее). Липопротеин-липаза вызывает также гидролиз фосфолипидов, что, в свою очередь, приводит к выделению жирных кислот, преобразующихся в триглицериды и депонирующихся, как уже обсуждалось. — Также рекомендуем «Свободные жирные кислоты. Транспорт свободных жирных кислот» Оглавление темы «Синтез АТФ. Обмен глюкозы и жиров»: |
Источник