Транспорт и выделение холестерина
Содержание статьи
Холестерол используется как переносчик полиненасыщенных жирных кислот
Транспорт холестерола и его эфиров осуществляется липопротеинами низкой и высокой плотности.
Липопротеины высокой плотности
Общая характеристика
- образуются в печени de novo, в плазме крови при распаде хиломикронов, некоторое количество в стенке кишечника,
- в составе частицы примерно половину занимают белки, еще четверть фосфолипиды, остальное холестерин и ТАГ (50% белка, 25% ФЛ, 13% эфиров ХС и 5% свободного ХС, 7% ТАГ),
- структурным апобелком является апо А1, также содержат апоЕ и апоСII.
Функция
- Транспорт свободного ХС от тканей к печени.
- Фосфолипиды ЛПВП являются источником полиеновых кислот для синтеза клеточных фосфолипидов и эйкозаноидов.
Метаболизм
1. Синтезированные в печени частицы (насцентные или первичные ЛПВП) содержат в основном фосфолипиды и апобелки. Остальные липидные компоненты накапливаются в ЛПВП по мере метаболизма в плазме крови.
Новосинтезированные ЛПВП выглядят на электронных микрофотографиях как двухслойные диски из двух монослоев фосфолипидов (таблеткообразная форма). Синтез апоЕ и апоС происходит главным образом в печени, в отличие от апо А-I, образующегося как в печени, так и в тонком кишечнике.
2-3. В плазме крови насцентный ЛПВП сначала превращается в ЛПВП3 (условно его можно назвать «зрелый»). В этом превращении главным является то, что ЛПВП
- забирает от клеточных мембран свободный холестерин при непосредственном контакте или при участии специфических транспортных белков,
- взаимодействуя с мембранами клеток, отдает им часть фосфолипидов из своей оболочки, доставляя таким образом полиеновые жирные кислоты в клетки,
- тесно взаимодействует с ЛПНП и ЛПОНП, получая от них свободный холестерин. В обмен ЛПВП3 отдают эфиры ХС, образованные благодаря переносу жирной кислоты от фосфатидилхолина (ФХ) на холестерин (ЛХАТ-реакция, см п.4).
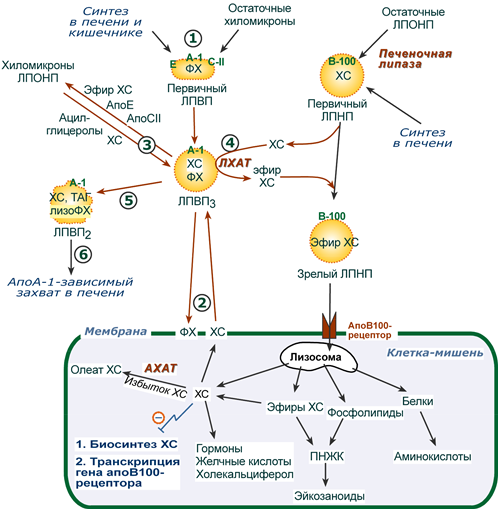
Транспорт холестерола и его эфиров в организме
(цифры соответствуют пунктам метаболизма ЛПВП по тексту)
4. Внутри ЛПВП активно протекает реакция при участии лецитин:холестерол-ацилтрансферазы (ЛХАТ-реакция). В этой реакции остаток полиненасыщенной жирной кислоты переносится от 2-го положения фосфатидилхолина (из оболочки самого ЛПВП) на получаемый свободный холестерин с образованием лизофосфатидилхолина (лизоФХ) и эфиров ХС. ЛизоФХ остается внутри ЛПВП, эфир холестерина отправляется в ЛПНП.
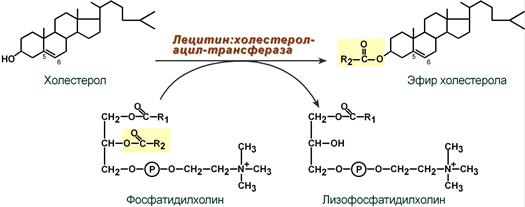
Реакция этерификации холестерола
при участии лецитин:холестерол-ацилтрансферазы
5. В результате первичный ЛПВП постепенно, через зрелую форму ЛПВП3, преобразуется в ЛПВП2 (остаточный, ремнантный). При этом происходят и дополнительные события:
- взаимодействуя с разными формами ЛПОНП и ХМ, ЛПВП получают ацил-глицеролы (МАГ, ДАГ, ТАГ), и обмениваются холестерином и его эфирами,
- ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм.
Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются.
6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается.
Липопротеины низкой плотности
Общая характеристика
- образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП,
- в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов),
- основным апобелком является апоВ-100,
- нормальное содержание в крови 3,2-4,5 г/л,
- самые атерогенные.
Функция
1. Транспорт холестерола в клетки, использующих его
- для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников),
- для превращения в холекальциферол (кожа),
- для образования желчных кислот (печень),
- для выведения в составе желчи (печень).
2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза.
Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола.
Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет.
Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения.
Также в мембраны всех клеток, как сказано выше (см «Метаболизм ЛПВП»), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП.
Метаболизм
1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и «выталкивание» белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый.
2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами.
3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры.
- ХС превращается в гормоны или включается в состав мембран,
- излишки мембранного ХС удаляются с помощью ЛПВП,
- принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов.
- при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция),
Синтез олеата холестерола при участии
ацил-SKoA-холестерол-ацилтрансферазы
На количество апоВ-100-рецепторов влияют гормоны:
- инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов,
- глюкокортикоиды уменьшают их количество.
Источник
ОБМЕН, РОЛЬ И ТРАНСПОРТ ХОЛЕСТЕРИНА — Студопедия
В сутки в организме синтезируется около 1 г холестерина (рис.10). Основное место синтеза – печень (до 80%), меньше синтезируется в кишечнике, коже и других тканях. С пищей поступает около 0,4 г холестерина, его источником является только пища животного происхождения. Холестерин необходим для построения всех мембран, в печени из него синтезируются желчные кислоты, в эндокринных железах – стероидные гормоны, в коже – витамин Д.
Рис.10 Холестерин
Сложный путь синтеза холестерина можно поделить на 3 этапа (рис.11). Первый этап заканчивается образованием мевалоновой кислоты. Источником для синтеза холестерина служит ацетил-КоА. Сначала из 3 молекул ацетил-КоА образуется ГМГ-КоА – общий предшественник в синтезе холестерина и кетоновых тел (однако реакции синтеза кетоновых тел происходят в митохондриях печени, а реакции синтеза холестерина – в цитозоле клеток). Затем ГМГ-КоА под действием ГМГ-КоА-редуктазы восстанавливается до мевалоновой кислоты с использованием 2 молекул НАДФН. Эта реакция является регуляторной в синтезе холестерина. Синтез холестерина тормозит сам холестерин, желчные кислоты и гормон голода глюкагон. Усиливается синтез холестерина при стрессе катехоламинами.
На втором этапе синтеза из 6 молекул мевалоновой кислоты образуется углеводород сквален, имеющий линейную структуру и состоящий из 30 атомов углерода.
На третьем этапе синтеза происходит циклизация углеводородной цепи и отщепление 3 атомов углерода, поэтому холестерин содержит 27 углеродных атомов. Холестерин является гидрофобной молекулой, поэтому транспортируется кровью только в составе разных липопротеинов.
Рис. 11 Синтез холестерина
Липопротеины – липид-белковые комплексы, предназначенные для транспорта нерастворимых в водных средах липидов по крови (рис.12). Снаружи липопротеины (ЛП) имеют гидрофильную оболочку, которая состоит из молекул белков и гидрофильных групп фосфолипидов. Внутри ЛП находятся гидрофобные части фосфолипидов, нерастворимые молекулы холестерина, его эфиров, молекулы жиров. ЛП делятся (по плотности и подвижности в электрическом поле) на 4 класса. Плотность ЛП определяется соотношением белков и липидов. Чем больше белка, тем больше плотность и тем меньше размер.
Рис.12. Строение липопротеидов
· 1 класс – хиломикроны (ХМ). Содержат 2% белка и 98% липидов, среди липидов преобладают экзогенные жиры, переносят экзогенные жиры от кишечника к органам и тканям, синтезируются в кишечнике, в крови присутствуют непостоянно – только после переваривания и всасывания жирной пищи.
· 2 класс – ЛП очень низкой плотности (ЛПОНП) или пре-b-ЛП. Белка в них 10%, липидов – 90%, среди липидов преобладают эндогенные жиры, транспортируют эндогенные жиры из печени в жировую ткань. Основное место синтеза – печень, небольшой вклад вносит тонкий кишечник.
· 3 класс – ЛП низкой плотности (ЛПНП) или b-ЛП. Белка в них 22% , липидов – 78%, среди липидов преобладает холестерин. Нагружают клетки холестерином, поэтому их называют атерогенными, т.е. способствующими развитию атеросклероза (АС). Образуются непосредственно в плазме крови из ЛПОНП под действием фермента ЛП-липазы.
· 4 класс ЛП высокой плотности (ЛПВП) или a-ЛП. Белка и липидов содержат по 50%, среди липидов преобладают фосфолипиды и холестерин. Разгружают клетки от избытка холестерина, поэтому являются антиатерогенными, т.е. препятствующими развитию АС. Основное место их синтеза – печень, небольшой вклад вносит тонкий кишечник.
Транспорт холестерина липопротеинами.
Печень является основнымместом синтеза холестерина. Холестерин, синтезированный в печени, упаковывается в ЛПОНП и в их составе секретируется в кровь. В крови на них действует ЛП-липаза, под влиянием которой ЛПОНП переходят в ЛПНП. Таким образом, ЛПНП становятся основной транспортной формой холестерина, в которой он доставляется к тканям. ЛПНП могут попадать в клетки двумя путями: рецепторным и нерецепторным захватом. Большинство клеток на своей поверхности имеют рецепторы к ЛПНП. Образовавшийся комплекс рецептор-ЛПНП эндоцитозом попадает внутрь клетки, где распадается на рецептор и ЛПНП. Из ЛПНП при участии лизосомальных ферментов освобождается холестерин. Этот холестерин используется для обновления мембран, тормозит синтез холестерина данной клеткой, а также, если количество холестерина, поступающего в клетку, превышает ее потребность, то подавляется и синтез рецепторов к ЛПНП.
Это уменьшает поток холестерина из крови в клетки, таким образом, клетки, для которых характерен рецепторный захват ЛПНП, имеют механизм, который ограждает их от избытка холестерина. Для гладкомышечных клеток сосудов и макрофагов характерен нерецепторный захват ЛПНП из крови. В эти клетки ЛПНП, а значит, и холестерин попадают диффузно, то есть, чем их больше в крови, тем больше их попадает в эти клетки. Эти разновидности клеток не имеют механизма, который ограждал бы их от избытка холестерина. В «обратном транспорте холестерина» от клеток участвуют ЛПВП. Они забирают избыток холестерина из клеток и возвращают его обратно в печень. Холестерин выводится с калом в виде желчных кислот, часть холестерина в составе желчи попадает в кишечник и также выводится с калом.
Источник
Транспорт холестерина и как происходит регулировка уровня?
Четкая последовательность метаболических процессов в организме крайне важна для адекватного его функционирования. Транспорт холестерина производится в первую очередь с помощью липопротеинов высокой, низкой и очень низкой плотности. Некоторые источники именуют их хиломикронами. Все основные метаболические процессы происходят на мембранах эндоплазматической сети печеночных клеток, а также в митохондриях надпочечниковых желез и в клетках гонад.
Где синтезируется холестерин?
Синтез холестерина происходит в первую очередь в печени. Также его молекулы синтезируются в других органах желудочно-кишечного тракта, мужских и женских половых органах, надпочечниках. Но большее количество холестериновых молекул поступает в организм извне, в составе животной пищи. Транспорт холестерола из места его образования происходит в комплексе с липидными молекулами низкой и очень низкой плотности.
Вернуться к оглавлению
Механизм синтеза
Основные этапы биосинтеза холестерола следующие:
- Молекула стирола присоединяет к себе гидроксильные группы. Это становится возможным благодаря реакции модификации в боковой цепи.
- Происходит окисное гидроксилирование стероидов. Эти процессы катализируются энзимами монооксигеназами.
- Включение в биосинтез цитохрома p450.
- Поступление холестериновых молекул в составе желчных кислот, стероидных гормонов или холекальциферола в циркулирующее русло жидких биологических сред.
Вернуться к оглавлению
Транспортировка холестерина
Излишки холестерола, которые попадают в организм с пищей, транспортируются в жировые ткани.
Экспорт синтезированного в печени холестерола производится только в составе межмолекулярных комплексов. Транспорт холестерина в крови осуществляется липопротеинами высокой, низкой и очень низкой плотности. Эти вещества играют главенствующую роль в развитии атеросклеротических процессов в сосудистом русле. Транспортная форма холестерола является его излишком, который поступил в организм с пищей или образовался под воздействием ферментов микроорганизмов. Липопротеины захватывают его и транспортируют в жировую ткань, где липидная часть комплекса отсоединяется, а сам холестерин переходит в гепатоциты. Далее транспортировка холестерола выполняется в кишечнике, откуда он с фекалиями выводится в форме копростанола.
Вернуться к оглавлению
Как происходит регулировка уровня вещества?
Концентрацию холестериновых молекул обязательно необходимо лимитировать. Это происходит на этапах биосинтеза. Распад холестерина производится с образованием мевалоната из бета-гамма-аминомасляной кислоты. В основе этого механизма лежит принцип негативной обратной связи. Если концентрация молекул холестерола превышает граничные значения, включается его катаболизм. Ингибитором фермента, который лизирует холестериновые молекулы, может выступать как сам холестерол, так и липопротеиды низкой плотности.
Употребление в пищу большого количества холестеринсодержащих продуктов угнетает его синтез в печени. А вот безхолестериновая диета, наоборот, активирует эндогенный синтез холестероловых молекул в гепатоцитах и других органах или тканях.
Вернуться к оглавлению
Выведение холестерина
Переносимый молекулами липопротеидов низкой и очень низкой плотности, холестерол длительно циркулирует в кровеносном русле, последовательно переходя из печени в нуждающиеся ткани. После потребления незатребованные молекулы распадаются до эфиров холестерина. Из организма они выводятся преимущественно с калом, в форме копростанола. Именно их называют желчными кислотами, которые придают каловым массам характерную коричневую окраску. При заболеваниях печени, особенно при обтурации желчевыводящих путей конкрементами, фекалии обесцвечиваются, приобретая песочный оттенок. Это обусловлено тем, что в них снижается концентрация желчных кислот вместе с холестеролом.
Источник
ХОЛЕСТЕРИНОВЫЙ ОБМЕН — Большая Медицинская Энциклопедия
ХОЛЕСТЕРИНОВЫЙ ОБМЕН (греческий chole желчь + stereos твердый) — совокупность реакций биосинтеза холестерина (см.) и его распада в организме человека и животных. В организме человека за сутки около 500 мг холестерина окисляется в желчные кислоты, примерно такое же количество стеринов экскретируется с фекалиями, около 100 мг выделяется с кожным салом, небольшое количество холестерина (около 40 мг) используется для образования кортикоидных и половых гормонов, а также витамина D3, 1—2 мг холестерина выводится с мочой. У кормящих женщин с грудным молоком выделяется 100— 200 мг холестерина в сутки. Эти потери восполняются за счет синтеза холестерина в организме (у взрослого человека в сутки около 700—1000 мг) и поступления его с пищей (300— 500 мг). Холестерин, а также часть холестерина, поступившего в просвет кишечника с желчью, всасывается в тонкой кишке в форме жировых мицелл (см. Жировой обмен). Эфиры холестерина предварительно гидролизуются при действии холестеринэстеразы (см.) панкреатического и кишечного соков. В стенке тонкой кишки холестерин используется для образования хиломикронов (см. Липопротеиды), в составе которых он поступает сначала в лимфатическую систему, а затем в кровяное русло.
В капиллярах жировой и некоторых других тканей в результате воздействия на хиломикроны липопротеид-липазы образуются частицы, обогащенные эфирами холестерина и фосфолипидами, получившие название ремнантных (остаточных) частиц. Эти частицы задерживаются в печени, где подвергаются распаду. Освободившийся при этом холестерин наряду с холестерином, синтезированным в печени, образует так называемый общий пул печеночного холестерина, который используется по мере необходимости для образования липопротеидов (см.).
Установлено, что у человека и некоторых животных липопротеиды низкой плотности транспортируют холестерин в органы и ткани, причем захват липоиротеидных частиц клетками этих органов и тканей осуществляется при участии специфических рецепторов. Холестерин, доставленный в клетку в составе липопротеидных частиц, идет на покрытие потребностей клетки (образование мембран при делении клетки, синтез стероидных гормонов и др.). Избыточная часть неэтерифицированного (свободного) холестерина превращается в его эфиры при действии содержащегося в клетке фермента — холестеролацилтрансферазы (КФ 2.3.1.26). Обратный транспорт неэтерифицированного холестерина из различных органов и тканей в печень осуществляется липопротеидами высокой плотности, причем в кровяном русле происходит этерификация захваченного холестерина при участии лецитина и фермента холестерин-лецитин — ацилтрансферазы (КФ 2.3.1.43). Доставленный таким путем в печень холестерин идет на образование желчных кислот (см.).
Синтез холестерина

Общая схема биосинтеза холестерина
Синтез холестерина осуществляется в клетках почти всех органов и тканей, однако в значительных количествах он образуется в печени (80%), стенке тонкой кишки (10%) и коже (5%). К. Блох, Ф. Линен и др. показали основные реакции биосинтеза холестерина (их не менее 30). Сложный процесс биосинтеза холестерина можно разделить на три стадии: 1) биосинтез мевалоновой кислоты; 2) образование сквалена из мевалоновой кислоты; 3) циклизация сквалена и образование холестерина (см. схему).
Считают, что главным источником образования мевалоновой кислоты в печени является ацетил-КоА, а в мышечной ткани — лейцин. И то и другое соединения в результате ряда энзиматических реакций образуют бета-гидрокси-бета-метилглутарил-КоА (ГМГ-КоА), который затем восстанавливается в мевалоновую кислоту. В последнее время показано, что в синтез мевалоновой кислоты в печени может включаться и малонил-КоА.
Реакцией, определяющей скорость биосинтеза холестерина в целом, является восстановление ГМГ-КоА в мевалоновую кислоту; этот процесс катализирует фермент НАДФ-Н2-зависимая ГМГ-КоА-редуктаза (КФ 1.1.1.34). Именно этот фермент подвержен воздействиям со стороны ряда факторов. Так, активность ГМГ-КоА-редуктазы повышается (или содержание ее в печени возрастает) и скорость синтеза холестерина в целом увеличивается при действии ионизирующего излучения, введении тиреоидных гормонов, поверхностно-активных веществ, холестирамина, а также при гипофизэктомии. Угнетение синтеза холестерина отмечается при голодании, тиреоидэктомии и при поступлении в организм пищевого холестерина. Последний угнетает активность (или синтез) фермента ГМГ-КоА-редуктазы.
Синтез холестерина в стенке тонкой кишки регулируется исключительно концентрацией желчных кислот. Так, отсутствие их в кишечнике при наличии наружного желчного свища ведет к повышению синтеза холестерина в тонкой кишке в 5—10 раз.
На второй стадии синтеза происходит фосфорилирование мевалоновой кислоты при участии АТФ и образование нескольких фосфорилированные промежуточных продуктов (см. Фосфорилирование). При декарбоксилировании одного из них образуется изопентенил-пирофосфат, часть которого превращается в диметилаллил-пирофосфат. Взаимодействие этих двух соединений приводит к образованию димера — геранил-пирофосфата, содержащего 10 атомов углерода. Геранил-пирофосфат конденсируется с новой молекулой изопентенил-пирофосфата и образует тример — фарнезил-пирофосфат, содержащий 15 атомов углерода. Эта реакция идет с отщеплением молекулы пирофосфата. Затем две молекулы фарнезил-пирофосфата конденсируются, теряя каждая свой пирофосфат, и образуют гексамер сквален, содержащий 30 атомов углерода.
Третья стадия синтеза включает окислительную циклизацию сквалена, сопровождающуюся миграцией двойных связей и образованием первого циклического соединения — ланостерина. Ланостерин уже имеет гидроксильную группу в положении 3 и три лишние (по сравнению с холестерином) метильные группы. Дальнейшее превращение ланосте-рина может совершаться двумя путями, причем и в том и в другом случае промежуточными продуктами являются соединения стериновой природы. Более доказанным считается путь через 24, 25-дигидроланостерин и ряд других стеринов, включая 7-дигидрохолестерин, служащий непосредственным предшественником холестерина. Другой возможный путь — превращение ланостерина в зимостерин, а затем в десмостерин, из которого при восстановлении образуется холестерин.
Если суммировать общий итог всех реакций биосинтеза холестерина, то он может быть представлен в следующем виде:
18CH3CO-S-KoA + 10(H+) + 1/2O2 —> C27H46O + 9CO2 + 18KoA-SH. Источником углерода холестерина является ацетил-КоА (им может быть также малонил-КоА и лейцин), источником водорода — вода и никотин-амида дениндинуклеотидфосфат, а источником кислорода — молекулярный кислород.
Начиная со сквалена и кончая холестерином все промежуточные продукты биосинтеза нерастворимы в водной среде, поэтому они участвуют в конечных реакциях биосинтеза холестерина в связанном со сквален или стеринпереносящими белками состоянии. Это позволяет им растворяться в цитоплазме клетки и создает условия для протекания соответствующих реакций. Холестерин-переносящий белок обеспечивает также перемещение стеринов внутри клетки, что имеет важное значение для вхождения его в мембрану клетки, а также для транспорта в клеточные системы, осуществляющие катаболизм холестерина.
Катаболизм холестерина протекает в печени (окисление его в желчные кислоты), в надпочечниках и плаценте (образование из холестерина стероидных гормонов), в тестикулярной ткани и яичниках (образование половых гормонов). При биосинтезе холестерина в коже на завершающей стадии образуется небольшое количество 7-дегидрохолестерина. Под влиянием УФ-лучей он превращается в витамин D3.
Своеобразные превращения претерпевает холестерин в толстой кишке. Речь идет о той части пищевого холестерина или холестерина, поступившего в кишечник с желчью, которая не подверглась всасыванию. Под влиянием микробной флоры толстой кишки происходит восстановление холестерина и образование так наз. нейтральных стеринов. Главным их представителем является копростерин. Экспериментальные исследования, проведенные с использованием радиоизотопных и других методов, показали, что скорость обновления холестерина в различных органах и тканях неодинакова; наиболее высока она в надпочечниках и печени и чрезвычайно низка в мозге взрослых животных.
Патология холестеринового обмена
Нарушения холестеринового обмена обычно связаны с дисбалансом между количеством синтезируемого в организме и поступающего с пищей холестерина, с одной стороны, и количеством холестерина, подвергающегося катаболизму,— с другой. Эти нарушения проявляются в изменении уровня холестерина в плазме крови, которые классифицируются как гиперхолестеринемия или гипохолестеринемия (для взрослого населения высокоразвитых стран величины выше 270 мг/100 мл и ниже 150 мг/100 мл соответственно).
Гиперхолестеринемия может быть первичной (наследственной или алиментарной) и вторичной, обусловленной различными заболеваниями. Наследственная (семейная) гиперхолестеринемия характеризуется высоким уровнем холестерина и липопротеидов низкой плотности (ЛПНГЛ в плазме крови. При гомозиготной гиперхолестеринемии уровень холестеринемии может достигать 700— 800 мг/100 мл, а при гетерозиготной — 300—500 мг/100 мл. В основе наследственной гиперхолестеринемии лежит генетически обусловленное отсутствие (у гомозигот) или недостаток (у гетерозигот) специфических рецепторов к липопротеидам низкой плотности у клеток, вследствие чего резко снижается захват и последующий катаболизм этих богатых холестерином липопротеидов клетками паренхиматозных органов и тканей. В результате пониженного захвата и снижения катаболизма липопротеидов низкой плотности развивается гиперхолестеринемия (см.). Последняя приводит к раннему развитию атеросклероза (см.) и его клинических проявлений — ишемической болезни сердца (см.), преходящей ишемии мозга (см. Инсульт) и др. Особенно тяжело протекает атеросклероз при гомозиготной форме; у таких больных часто наблюдается ксантоматоз (см.), липоидная дуга роговицы (отложение холестерина в роговицу глаз), инфаркт миокарда в юношеском возрасте.
Распространенность гомозиготной формы гиперхолестеринемии невелика (примерно один случай на 1 млн. жителей). Чаще встречается гетерозиготная форма — один случай на 500 жителей.
Алиментарная гиперхолестеринемия характеризуется повышенным уровнем холестерина в плазме крови вследствие длительного потребления больших количеств пищи, богатой холестерином (куриные желтки, икра, печень, животные жиры и др.). Алиментарная гиперхолестеринемия той или иной степени выраженности характерна для жителей высокоразвитых индустриальных стран. Согласно популяционным исследованиям имеется прямая зависимость между уровнем холестерина в крови и распространенностью ишемической болезни сердца.
В эксперименте на различных животных (кролики, морские свинки, обезьяны) показано, что введение массивных доз холестерина с пищей приводит к резко выраженной гиперхолестеринемии и быстрому развитию атеросклероза. Экспериментальные модели гиперхолестеринемии и атеросклероза, впервые предложенные H. Н. Аничковым и С. С. Халатовым (1913), широко используются в научных исследованиях.
Вторичная гиперхолестеринемия встречается при гипотиреозе (см.), сахарном диабете (см. Диабет сахарный), нефротическом синдроме (см.), подагре (см.) и др. и нередко сопровождается развитием атеросклероза (см. Гиперхолестеринемия).
Выделяют первичную и вторичную гипохолестеринемию. Первичная гипохолестеринемия характерна для наследственного заболевания — абеталипопротеинемии (см.). При этой болезни отмечается почти полное отсутствие в плазме крови липопротеидов низкой плотности (у гомозигот) или значительное их снижение (у гетерозигот). Уровень общего холестерина не превышает 75 мг/ 100 мл. Гомозиготная форма болезни протекает исключительно тяжело. В основе абеталипопротеинемии лежит генетически обусловленное нарушение синтеза апопротеина В — главного белка липопротеидов низкой плотности.
Вторичные гипохолестеринемии наблюдаются при кахексии, гипертиреоидизме, аддисоновой болезни и паренхиматозных заболеваниях печени, при ряде инфекционных болезней и интоксикациях (см. Гипохолестеринемия). При недостаточной активности в плазме крови фермента лецитин — холестерин -ацилтрансферазы, или ЛХАТ (наследственная ЛXАТ-недостаточность), ответственного за этерификацию холестерина плазмы, наблюдается накопление неэтерифицированного холестерина в мембранах эритроцитов и клетках почек, печени, селезенки, костного мозга, роговицы глаза. Резко снижается доля этерифицированного холестерина в плазме крови и одновременно повышается уровень неэтерифицированного холестерина и лецитина. У больных с наследственной ЛXAT-недостаточностыо стенки артерий и капилляров подвержены деструктивным изменениям, что связано с отложением в них липидов. Наиболее тяжелые изменения происходят в сосудах почечных клубочков, что приводит к развитию почечной недостаточности (см.).
Одним из распространенных нарушений холестериновый обмен. является образование желчных камней, основной составной частью которых является холестерин (см. Желчнокаменная болезнь). Образование желчных камней происходит вследствие выкристаллизовывания холестерина при относительно высокой его концентрации в желчи и относительно низкой концентрации в ней желчных кислот и фосфолипидов, обладающих способностью растворять холестерин. Исследования показали, что имеется прямая связь между уровнем холестерина в плазме крови и распространенностью холестероза (см.) и желчнокаменной болезни.
Библиогр.: Климов А. Н, и Н икульчева Н. Г. Липопротеиды, дислипопротеидемии и атеросклероз, Л., 1984; Полякова Э. Д. Пути биосинтеза холестерина в печени и их регуляция, в кн.: Липиды, структура,биосинтез, превращения и функции, под ред. С. Е. Северина, с. 131, М., 1977;она же, Регуляция содержания холестерина в клетке, в кн.: Биохимия липидов и их роль в обмене веществ, под ред.С. Е. Северина, с. 120, М., 1981; Финагин Л. К. Обмен холестерина и его регуляция, Киев, 1980; Lipids and lipidoses, ed. by G. Schettler, B.— Heidelberg, 1967; Sodhi H. S., Kudchod-k a r B. J. a. Mason D. T. Clinical methods in study of cholesterol metabolism, Basel a. o., 1979.
A. H. Климов
Источник