В мышцах содержится выполняющий функции аналогичные гемоглобину
Содержание статьи
МИОГЛОБИН
МИОГЛОБИН (myoglobinum; греч, mys, my [os] мышца + лат. globus шарик; Mgb; син.: миогемоглобин, мышечный гемоглобин) — сложный белок красного цвета, относящийся к хромопротеидам; содержится в красных мышцах животных различных классов и видов. Основной функцией М. является накопление кислорода, поступающего в процессе дыхания в мышцы из крови и отдача кислорода по мере необходимости в нем (см. Газообмен).
Факторами, определяющими различия в содержании М., являются видовая принадлежность животных (см. табл.), особенности условий их существования, образ жизни, тип мышцы, степень ее активности, а также трофические влияния нервной системы. Очень высокое содержание М. (до 16-40 г на 100 г высушенной ткани) характерно для водных животных. Значительные количества М. содержатся в красных мышцах нек-рых беспозвоночных (моллюски), в гладких мышцах мускульного желудка птиц, в гладкой мускулатуре бронхов, сосудов, стенок кишечника, а также в паренхиматозных органах, причем последние участвуют в процессах синтеза (печень), распада (селезенка) и выделения пигмента. Однако еще не доказано, что пигмент, выделенный из паренхиматозных органов, идентичен М.
Таблица. Содержание миоглобина в сердечных и скелетных мышцах человека и некоторых классов позвоночных животных (в г на 100 г высушенной ткани)
Класс животных; человек | Мышцы сердца | Скелетные мышцы |
Рыбы | 0,2-0,5 | 0, 1-0,4 |
Амфибии | 0, 1-0, 6 | 0 -0,1 |
Рептилии | 0, 8-2, 6 | 0,2-2,4 |
Птицы: | ||
домашние | 1, 0-2,0 | 0,9-1,8 |
дикие | 2,1-6, 5 | 0, 7-5, 3 |
Млекопитающие: | ||
домашние | 0, 9-4, 4 | 0,2-8, 5 |
дикие | 1,1-6,2 | 0,02-5,13 |
Человек | 1,5 | 1,4-3,9 |
В крови и моче М. в норме отсутствует. Поэтому его появление в этих биол, жидкостях является признаком заболеваний, сопряженных с деструкцией тканей (инфаркт миокарда, травматические повреждения мышц, генетически обусловленная прогрессивная мышечная дистрофия и т. д.). Определение уровня М. в плазме крови может служить критерием обширности деструкции, динамики процесса и эффективности лечебных мероприятий.
Мол. вес (масса) М. составляет в среднем 17 500, содержание железа 0,34%, Изоэлектрическая точка находится при pH 6,99. М. характеризуется большой растворимостью и высокой устойчивостью к действию щелочей.

Схематическое изображение молекулы миоглобина: цифрами отмечен каждый десятый аминокислотный остаток; светлые кружки — остатки пролина (Про), часто совпадающие с поворотом полипептидной цепи. В виде диска изображена группа гема; буквами С и N обозначены концевые участки цепи, содержащие соответственно свободные карбокси- и аминогруппы.
Изучена третичная структура М. и построена пространственная модель его молекулы (рис.). М. состоит из простого белка- глобина, представляющего собой одну полипептидную цепь, в состав к-рой входит 153 аминокислотных остатка, и простетической (небелковой) группы — гема (железопротопорфириновый комплекс, или протогем). Полипептидная цепь глобина М. на 77% представлена альфа-спиральными участками (всего 8 спиралей), к-рые перемежаются с участками неупорядоченной структуры, расположенными в области четырех изгибов полипептидной цепи. Все полярные группы, образованные лизином, аргинином, глутамином, аспарагином, гистидином, треонином, тирозином и триптофаном, находятся на поверхности и соединены с молекулами воды, а неполярные остатки сконцентрированы в центре. Поэтому молекула М. компактна и устойчива к изменениям pH и ионной силы р-ра.
По своим свойствам глобин М. близок к альбуминам. Гем М. расположен в углублении, находящемся на определенном изгибе полипептидной цепи вблизи поверхности молекулы. Это делает гем более доступным различным воздействиям. Одной координационной связью (пятой) гем соединен с гистидиновым остатком альфа-спирали, а шестая координационная связь железа гема может быть занята водой, кислородом, окисью углерода или другими соединениями. При взаимодействии с кислородом (оксигенации) в глобине молекулы М. не происходит структурных изменений. Пигмент мышц не способен соединяться с двуокисью углерода (CO2).
Доказано существование двух конформеров (А и В) нативного состояния М., к-рые отличаются по своим свойствам и структуре. Переход конформера А в конформер В протекает при повышении температуры от 20 до 40° и отражается на активности гема. Высокотемпературный конформер В является менее реакционноспособным.
М. человека и животных имеет неодинаковую форму кристаллов: тонкие, игловидные, собранные в пучки (человек), ромбические таблички (рогатый скот) и др. М. подобно гемоглобину (см.) образует различные производные, отличающиеся друг от друга по спектрам поглощения. При соединении с кислородом М. превращается в оксимиоглобин (MgbO2), в к-ром железо гема является двухвалентным. С помощью метода дифракции рентгеновских лучей показано, что оксигенация М. сопровождается пространственным смещением железа от середины порфиринового кольца по направлению к проксимальному гистидину (F-8) полипептидной цепи на 0,033 нм. В гемоглобине же оксигенация вызывает гораздо большее смещение атома железа (0,04- 0,05 нм) и изменения в четвертичной структуре всей молекулы пигмента крови.
Вдыхание животными воздуха, содержащего окись углерода в повышающихся концентрациях (0,01-0,2%), приводит не только к увеличению содержания карбоксигемоглобина в крови, но и к связыванию окиси углерода миоглобином с образованием карбоксимиоглобина (MgbCO), железо гема к-рого также находится в двухвалентном состоянии. Когда количество карбоксигемоглобина в крови достигает 60%, содержание карбоксимиоглобина в скелетных мышцах составляет 10-50%, а в мышце сердца — от 6 до 44%. MgbCO обнаружен и в мышцах людей, погибших от отравления: угарным газом. Воздействие на М. окислителей обусловливает возникновение метмиоглобина (метMgb). Превращение М. в метMgb при окислении происходит очень легко и при одинаковых условиях в 12-14 раз превышает скорость образовании метгемоглобина. В то же время в мышцах животных эта реакция после внутривенного вливания окисляющих ядов протекает более медленно, чем окисление гемоглобина.
Максимумы полос поглощения М. и его производных расположены при следующих значениях длин волн: для MgbO2 — 582, 542, 415 нм; для Mgb — 602, 560, 436 нм; для MgbCO — 585, 542, 423 нм; для метMgb — 630, 500, 409 нм. Известный другие производные пигмента: сульфмиоглобин, нитроксимиоглобин, цианмиоглобин и т. д. В реакциях сопряженного окисления М. переходит в зеленый пигмент — вердомиоглобин, а при более глубоком распаде — в желчные пигменты (см.).
Биосинтез М. происходит в мышцах со значительно меньшей скоростью по сравнению с гемоглобином. После введения животным меченого железа оно обнаруживается в гемоглобине уже спустя 6-8 дней, а в М. только через месяц. Продолжительность существования М. составляет 80 дней. В процессе эмбриогенеза М. раньше всего появляется в мышце сердца.
В мышцах позвоночных М. локализуется в саркоплазме на уровне диска А и связан электростатически с наружной мембраной митохондрий или саркоплазматического ретикулума (см. Мышечная ткань).
Создаваемый с помощью М. резерв кислорода в мышцах прежде всего определяется концентрацией в них пигмента и его способностью подвергаться оксигенации и деоксигенации. М. поддерживает постоянный уровень оксигенации во время мышечного сокращения, создавая определенный градиент напряжения кислорода между капиллярами и мышечными клетками, обеспечивая, т. о., возможность его утилизации при усилении окислительных процессов в работающих мышцах. Благодаря высокому сродству к кислороду полунасыщение им М. происходит менее чем за 0,1 сек. (при pO2 = 3,3 мм рт. ст.). При pO2, равном 5 мм рт. ст. (минимальное для деятельности цитохромоксидазы), диссоциирует до 40% оксимиоглобина, повышая, т. о., количество кислорода, растворенного в саркоплазме. М. участвует в молекулярном механизме его транспорта в клетку путем создания градиента и ускорения диффузии. Не исключена возможность непосредственного переноса кислорода М. при поступательном движении молекулы пигмента. Благодаря наличию пероксидазных свойств М. обладает ферментативной активностью. Доказана возможность включения М. в работу фосфорилирующей дыхательной цепи в качестве акцептора электронов от восстановленных коферментов пиридинового типа (НАД-H и в меньшей степени НАДФ-Н).
Существующие методы количественной оценки содержания М. включают электрофорез (см.) и ионообменную хроматографию (см.). Разделение М. и гемоглобина достигается благодаря их различной растворимости в 3 М фосфатном буфере при pH 6,6 (гемоглобин при этом значении pH нерастворим). Спектрофотометрическая регистрация количества М. основана на разнице в светопоглощении карбокси- и цианметсоединений М. и гемоглобина в видимой части спектра (см. Спектрофотометрия). Предложены также гистохимические методы определения М., основанные на бензидин-пероксидазной активности пигмента. Они позволяют с достаточной достоверностью выявлять М. в мышечной ткани и устанавливать закономерности в локализации и распределении М. в норме и их изменения при различных патол, состояниях.
Миоглобин в судебно-медицинском отношении
Миоглобин в судебно-медицинском отношении имеет значение в случаях прижизненного поражения скелетных мышц, сопровождающегося высвобождением М. При этом М. накапливается в плазме крови. При концентрации, превышающей 30 мг%, развивается миоглобинурия (см.), к-рая наряду с шоковым и коматозным состоянием, интоксикацией и пр. служит патогенетическим фактором развития миоглобинурийного нефроза (см. Нефротический синдром). Повреждение мышц, сочетающееся с обширными гематомами или внутрисосудистым гемолизом, кроме того, ведет к возникновению гемоглобинемии (см.), приводящей в последующем к миоглобинурии и миоглобинурийному нефрозу. Т. о., миоглобинемия и обусловленные ею процессы служат экспертным критерием поражения скелетной мускулатуры и доказательством его прижизненности.
Миоглобинемия может иметь место при механической травме (одномоментная травма обширных мышечных массивов, так наз. краш-синдром, или синдром раздавливания), отравлении миолитическими ядами, в т. ч. пищевыми (токсический миозит), при нарушении артериального или венозного кровообращения в конечностях (тромбоз или тромбоэмболия крупных артерий, тромбоз вен, синдром жгута, состояние после реплантации конечностей), при длительном пребывании человека в одной и той же позе (позиционное сдавление), при ожогах, обморожениях, при судорожных состояниях (эпилепсия, столбняк и т. д.).
Наличие и содержание М. в крови и моче устанавливают спектрофотометрическим способом или при помощи электрофореза. Для дифференциации пигментов в моче применяют пробу с сульфатом аммония, при к-рой в осадке мочи, содержащем миоглобиновые шлаки, на фильтре наблюдается характерное окрашивание .
Библиография: Атанасов Б. П. Модели конформеров нативного состояния миоглобина, Молек. биол., т. 4, в. 3, с. 348, 1970, библиогр. ; Верболович П. А. и Верболович В. П. Миоглобин и использование кислорода в животном организме, в кн.: Полярографическое определение кислорода в биол, объектах, под ред. В.А. Березовского, с. 123, Киев, 1974, библиогр.; Свадковский Б. С. Острый пигментный нефроз и его судебно-медицинская оценка, М., 1974, библиогр.; Троицкая О. В. Миоглобин, его химическое строение и функции в организме, Вопр, мед. хим., т. 17, в. 5, с. 451, 1971, библиогр.; Murray J. D. On the role of myoglobin in muscle respiration, J. theor. Biol., v. 47, p. 115, 1974, bibliogr.; Wittenberg J. B. Myoglobin — facilitated oxygen diffusion, role of myoglobin in oxygen entry into muscle, Physiol. Rev., v. 50, p. 559, 1970, bibliogr.
П. А. Верболович, В. П. Верболович; М. В. Кисин (суд.-мед.).
Источник
Миоглобин скелетных мышц
Дано определение миоглобина и описаны его структура и функции. Приведены данные о концентрации миоглобина в скелетных мышцах человека и животных, а также в плазме крови человека. Приведен сравнительный анализ гемоглобина и миоглобина.
Определение
Миоглобин (Mb) — белок, который связывает кислород в скелетных мышцах и миокарде (сердечной мышце) почти всех млекопитающих, в том числе и человека. Молекулярная масса миоглобина — 17,2 кДа (1Да=1,66 10-24 г.).
Структура миоглобина
Первичная структура миоглобина представлена одной полипептидной цепью, состоящей из 146-154 аминокислотных остатков. Вторичная структура — α-спираль. Третичная структура миоглобина представлена свернутой в шар α-спиралью (глобулой) и небелковой частью — гемом (рис.1). Присутствие гема придает миоглобину красный цвет. В геме имеется железо, которое связывает кислород. В 1957 году Джон Кендрю посредством рентгеновской кристаллографии впервые определил пространственное расположение полипептидной цепи в молекуле белка миоглобина, а в 1959 году установил его детальное строение, подтвердив наличие в нём α-спиралей, которое еще в 1951 году предсказал Лайнус Полинг.
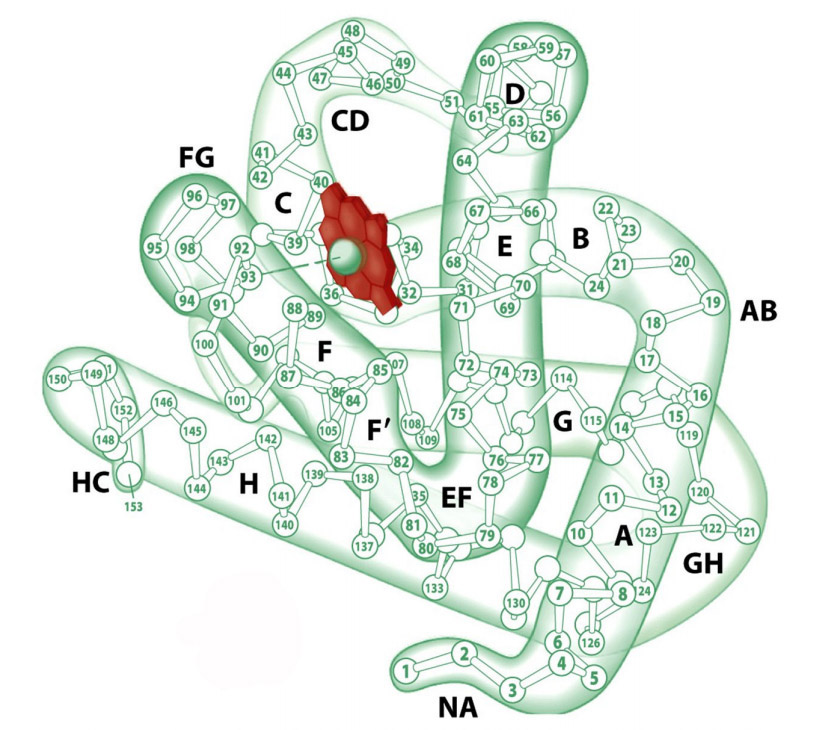
Рис.1. Структура миоглобина. Красным цветом выделен гем (illustration I. Geis)
Функции миоглобина
В мышечных волокнах миоглобин выполняет следующие функции:
- Депонирует кислород. Мышцы, поглощая кислород из крови, накапливают его в мышечных волокнах в вида оксимиоглобина. Таким образом создается резерв миоглобина, который используется для усиления окислительных процессов при тяжелой физической работе. Депонирование происходит в период покоя, расход в момент сокращения мышц. Однако емкость этого депо невелика. Оно может обеспечить снабжение кислородом скелетные мышцы в течение 8 с, а миокард в течение 15-20 с (Стародуб Р.Ф., Коробов В.Н., Назаренко В.И., 1992).
- Переносит кислород от плазматической мембраны к митохондриям. Тем самым обеспечивая функционирование тканевого дыхания.
- Связывает и освобождает оксид азота (NO) — одну из главных сигнальных молекул, играющих критическую роль в контроле поглощения кислорода, вазодилятации (расширения) сосудов и защиты мышечных волокон от активных форм кислорода (Кулева Н.В., Красовская И.Е., 2016).
Более подробно строение и функции мышц описаны в моих книгах
Концентрация миоглобина в мышечных волокнах
В мышечных волокнах скелетных мышц человека концентрация миоглобина составляет 0,4-0,5 мM (0,25 мг на 1 г ткани). Миоглобин присутствует во всех типах мышечных волокон, однако в разных концентрациях. В мышечных волокнах типа I его концентрация в 1,5 раза выше, чем в мышечных волокнах типа IIB. Именно поэтому мышечные волокна типа I имеют более красную окраску по сравнению с мышечными волокнами типа II. У морских млекопитающих концентрация миоглобина в мышечных волокнах может достигать 3,8 мM. Установлена значительная корреляция между концентрацией миоглобина в мышцах морских животных и глубиной ныряния. Установлено также, что концентрация миоглобина в мышечных волокнах коррелирует с объемной плотностью митохондрий и плотностью кровеносных капилляров.
Концентрация миоглобина в крови
В обычных условиях концентрация миоглобина в крови настолько низка (100 нг/мл), что он не определяется лабораторными методами. Однако при сильных повреждениях мышечных волокон скелетных мышц (краш-синдроме, синдроме позиционной ишемии) миоглобин может попасть в кровь. Так как молекулы миоглобина достаточно крупные, они могут закупоривать канальцы почек и приводить к их некрозу. В результате возникает острая почечная недостаточность и тканевая гипоксия. Это может привести к смерти человека.
При тяжелых силовых и аэробных тренировках (например при марафонском беге), также происходит частичное повреждение мышечных волокон скелетных мышц и миоглобин поступает в кровь.
При остром инфаркте миокарда концентрация миоглобина в крови повышается через 2-4 часа. Поэтому его относят к неспецифическим маркерам этого заболевания (Тереньев А.А., 2016).
Гемоглобин и миоглобин
Миоглобин похож на гемоглобин (Hb) — кислородсвязывающий белок в эритроцитах крови. Гемоглобин осуществляет транспорт кислорода от легких к тканям (в том числе и мышцам), а миоглобин — депонирование и транспорт кислорода внутри мышечных волокон. Структура гемоглобина более сложная, чем миоглобина. Молекула гемоглобина состоит из четырех полипептидных цепочек и гема, а молекула миоглобина — из одной полипепдиной цепочки и гема. Молекулярная масса гемоглобина человека 66,8 кДа. Миоглобин человека обладает большим сродством к кислороду, чем гемоглобин, и способен связывать до 14% от общего количества кислорода в организме.
Литература
- Кулева Н.В., Красовская И.Е. Новая роль миоглобина в функционировании сердечной и скелетной мышц // Молекулярная биофизика, 2016.- Т. 61., Вып. 5.- С. 861-864.
- Стародуб Р.Ф., Коробов В.Н., Назаренко В.И. Миоглобин: структура, свойства, синтез и биологическая роль.- Киев: Наукова думка, 1992.- 281 с.
- Терентьев А.В. Биохимия мышечной ткани: Учебное пособие.- М.: ФГБОУ ВО РНИМУ им. Н.И.Пирогова Минздрава России, 2019.- 2019 с.
С уважением, А.В. Самсонова
Источник
Миоглобин — Myoglobin
Миоглобин (символ MB или MB ) — это связывающий железо и кислород белок, обнаруженный в ткани скелетных мышц позвоночных в целом и почти у всех млекопитающих. Миоглобин отдаленно связан с гемоглобином . По сравнению с гемоглобином миоглобин имеет более высокое сродство к кислороду и не имеет кооперативного связывания с кислородом, как гемоглобин. Но по сути, это белок, связывающий кислород в красных кровяных тельцах . У людей миоглобин обнаруживается в кровотоке только после мышечной травмы .
Высокая концентрация миоглобина в мышечных клетках позволяет организмам задерживать дыхание на более длительный период времени. У ныряющих млекопитающих, таких как киты и тюлени, есть мышцы с особенно высоким содержанием миоглобина. Миоглобин содержится в мышцах типа I, типа II A и типа II B, но в большинстве текстов считается, что миоглобин не обнаруживается в гладких мышцах .
Миоглобин был первым белком, трехмерная структура которого была выявлена с помощью рентгеновской кристаллографии . Об этом достижении сообщили в 1958 году Джон Кендрю и его сотрудники. За это открытие Кендрю разделил Нобелевскую премию по химии 1962 года с Максом Перуцем . Несмотря на то, что это один из наиболее изученных белков в биологии, его физиологическая функция еще не установлена окончательно: мыши, генетически сконструированные с отсутствием миоглобина, могут быть жизнеспособными и фертильными, но демонстрируют множество клеточных и физиологических адаптаций для преодоления потери. Наблюдая за этими изменениями у мышей с истощенным миоглобином, было выдвинуто предположение, что функция миоглобина связана с повышенным транспортом кислорода к мышцам и с накоплением кислорода; кроме того, он служит поглотителем активных форм кислорода .
В организме человека, миоглобина кодируется MB гена .
Миоглобин может принимать формы оксимиоглобина (MbO 2 ), карбоксимиоглобина (MbCO) и метмиоглобина (met-Mb), аналогично гемоглобину, принимающему формы оксигемоглобина (HbO 2 ), карбоксигемоглобина (HbCO) и метгемоглобина (met-Hb).
Отличия от гемоглобина
Как и гемоглобин, миоглобин — это цитоплазматический белок, который связывает кислород с гемовой группой. Он содержит только одну группу глобулинов, тогда как гемоглобин состоит из четырех. Хотя его гемовая группа идентична группе гемоглобина, Mb имеет более высокое сродство к кислороду, чем гемоглобин. Это различие связано с его другой ролью: в то время как гемоглобин транспортирует кислород, функция миоглобина заключается в хранении кислорода.
Роль в кухне
Миоглобин содержит гемы, пигменты, отвечающие за цвет красного мяса . Цвет мяса частично определяется степенью окисления миоглобина. В свежем мясе атом железа находится в степени окисления двухвалентного железа (+2), связанного с молекулой кислорода (O 2 ). Хорошо прожаренное мясо имеет коричневый цвет, потому что атом железа теперь находится в степени окисления трехвалентного железа (+3), потеряв электрон. Если мясо подверглось воздействию нитритов , оно останется розовым, потому что атом железа связан с NO, оксидом азота (например, солонина или вяленая ветчина ). Мясо, приготовленное на гриле, также может иметь красновато-розовое «кольцо дыма», возникающее из-за связывания гемового центра с угарным газом . Сырое мясо, упакованное в атмосфере окиси углерода, также имеет то же розовое «кольцо дыма» из-за тех же принципов. Примечательно, что поверхность этого сырого мяса также имеет розовый цвет, который в сознании потребителей обычно ассоциируется со свежим мясом. Этот искусственно вызванный розовый цвет может сохраняться до одного года. Сообщается, что Hormel и Cargill используют этот процесс упаковки мяса, и мясо, обработанное таким образом, находится на потребительском рынке с 2003 года.
Роль в болезни
Миоглобин выделяется из поврежденной мышечной ткани ( рабдомиолиз ), в которой содержится очень высокая концентрация миоглобина. Высвободившийся миоглобин фильтруется почками, но токсичен для эпителия почечных канальцев и поэтому может вызвать острое повреждение почек . Токсичен не сам миоглобин (это протоксин ), а феррихематная часть, которая отделяется от миоглобина в кислой среде (например, кислая моча, лизосомы ).
Миоглобин является чувствительным маркером мышечного повреждения, что делает его потенциальным маркером сердечного приступа у пациентов с болью в груди . Однако повышенный уровень миоглобина имеет низкую специфичность в отношении острого инфаркта миокарда (ОИМ), поэтому при постановке диагноза следует принимать во внимание CK-MB , сердечный тропонин , ЭКГ и клинические признаки.
Структура и склеивание
Миоглобин принадлежит к суперсемейству белков глобинов и, как и другие глобины, состоит из восьми альфа-спиралей, соединенных петлями. Миоглобин содержит 153 аминокислоты.
Миоглобин содержит порфириновое кольцо с железом в центре. Проксимальная гистидин группа (His-93) прикреплена непосредственно к железу, а дистальный гистидин группа (His-64) парит возле противоположной грани. Дистальный имидазол не связан с железом, но доступен для взаимодействия с субстратом О 2 . Это взаимодействие способствует связыванию O 2 , но не монооксида углерода (CO), который по-прежнему связывается примерно в 240 раз сильнее, чем O 2 .
Связывание O 2 вызывает существенные структурные изменения в центре Fe, который сжимается по радиусу и перемещается в центр кармана N4. Связывание O 2 вызывает «спаривание спинов»: пятикоординатная дезокси-форма двухвалентного железа является высокоспиновой, а шестикоординированная окси-форма низкоспиновой и диамагнитной .
Молекулярно-орбитальное описание взаимодействия Fe-O 2 в миоглобине.
Это изображение оксигенированной молекулы миоглобина. Изображение показывает структурные изменения, когда кислород связывается с атомом железа простетической группы гема. Атомы кислорода окрашены в зеленый цвет, атом железа — в красный, а гемовая группа — в синий цвет.
Синтетические аналоги
Многие модели миоглобина были синтезированы в рамках широкого интереса к дикислородным комплексам переходных металлов . Хорошо известным примером является порфирин из штакетника , который состоит из комплекса железа и пространственно объемного производного тетрафенилпорфирина . В присутствии имидазольного лиганда этот комплекс двухвалентного железа обратимо связывает O 2 . Подложка O 2 имеет изогнутую форму, занимая шестую позицию центра железа. Ключевым свойством этой модели является медленное образование μ-оксодимера, который находится в неактивном диферрическом состоянии. В природе такие пути дезактивации подавляются белковой матрицей, которая предотвращает близкое сближение ансамблей Fe-порфиринов.
Порфириновый комплекс Fe из штакетника с аксиальными координационными центрами, занятыми метилимидазолом (зеленый) и дикислородом . Группы R фланкируют сайт связывания O 2 .
Смотрите также
- Цитоглобин
- Гемоглобин
- Гемопротеин
- Нейроглобин
- Фитоглобин
- Миоглобинурия — наличие миоглобина в моче.
- Ишемически-реперфузионное повреждение аппендикулярно-опорно-двигательного аппарата
Рекомендации
дальнейшее чтение
- Коллман Дж. П., Булатов Р., Сандерленд С. Дж., Фу Л. (февраль 2004 г.). «Функциональные аналоги цитохром с оксидазы, миоглобина и гемоглобина». Химические обзоры . 104 (2): 561-88. DOI : 10.1021 / cr0206059 . PMID 14871135 .
- Ридер Б.Дж., Свистуненко Д.А., Cooper CE, Wilson MT (декабрь 2004 г.). «Радикальная и окислительно-восстановительная химия миоглобина и гемоглобина: от исследований in vitro до патологии человека». Антиоксиданты и редокс-сигналы . 6 (6): 954-66. DOI : 10.1089 / ars.2004.6.954 . PMID 15548893 .
- Schlieper G, Kim JH, Molojavyi A, Jacoby C, Laussmann T., Flögel U, Gödecke A, Schrader J (апрель 2004 г.). «Адаптация мышей с нокаутом миоглобина к гипоксическому стрессу» . Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология . 286 (4): R786-92. DOI : 10,1152 / ajpregu.00043.2003 . PMID 14656764 . S2CID 24831969 .
- Takano T (март 1977 г.). «Структура миоглобина уточнена с разрешением 2-0 A. II. Структура дезоксимиоглобина кашалота». Журнал молекулярной биологии . 110 (3): 569-84. DOI : 10.1016 / S0022-2836 (77) 80112-5 . PMID 845960 .
- Рой А., Сен С., Чакраборти А.С. (февраль 2004 г.). «Неферментное гликирование in vitro усиливает роль миоглобина как источника окислительного стресса». Свободно-радикальные исследования . 38 (2): 139-46. DOI : 10.1080 / 10715160310001638038 . PMID 15104207 . S2CID 11631439 .
- Стюарт Дж. М., Блейкли Дж. А., Карпович П. А., Каланши Е., Тэтчер Б. Дж., Мартин Б. М. (март 2004 г.). «Необычно слабое связывание кислорода, физические свойства, частичная последовательность, скорость автоокисления и потенциальный сайт фосфорилирования миоглобина белухи (Delphinapterus leucas)». Сравнительная биохимия и физиология Б . 137 (3): 401-12. DOI : 10.1016 / j.cbpc.2004.01.007 . PMID 15050527 .
- Ву Г., Уэйнрайт Л. М., Пул Р. К. (2003). Микробные глобины . Успехи микробной физиологии. 47 . С. 255-310. DOI : 10.1016 / S0065-2911 (03) 47005-7 . ISBN 9780120277476 . PMID 14560666 .
- Мирчета С., Синьор А. В., Бернс Дж. М., Коссинс А. Р., Кэмпбелл К. Л., Беренбринк М. (июнь 2013 г.). «Эволюция способности млекопитающих нырять, отслеживаемая чистым поверхностным зарядом миоглобина» . Наука . 340 (6138): 1234192. DOI : 10.1126 / science.1234192 . PMID 23766330 . S2CID 9644255 . . Также см. Статью Proteopedia об этом открытии.
Внешние ссылки
- Онлайн-Менделирующее наследование в человеке (OMIM): 160000 генетика человека
- Белок миоглобин
- RCSB PDB представленная молекула
- «Какой отруб старше? (Это вопрос с подвохом)» , The New York s , 21 февраля 2006 г., статья об использовании в мясной промышленности угарного газа для сохранения красного цвета мяса.
- «Магазины реагируют на сообщения о мясе » , The New York s , 1 марта 2006 г., статья об использовании угарного газа для придания свежести мясу.
- Обзор всей структурной информации, доступной в PDB для UniProt : P02144 (человеческий миоглобин) в PDBe-KB .
Источник