Все о холестерине биохимия
Содержание статьи
Хороший, плохой, злой холестерин
Статья на конкурс «био/мол/текст»: Вряд ли сейчас найдется человек, который не слышал, что высокий холестерин — это плохо. Однако столь же мала вероятность встретить человека, который знает, ПОЧЕМУ высокий холестерин — это плохо. И чем определяется высокий холестерин. И что такое высокий холестерин. И что такое холестерин вообще, зачем он нужен и откуда берется.
Итак, история вопроса такова. Давным-давно, в одна тысяча девятьсот тринадцатом году, петербуржский физиолог Аничков Николай Александрович показал: не что иное, как холестерин, вызывает атеросклероз у экспериментальных кроликов, содержащихся на пище животного происхождения [1]. Вообще же, холестерин необходим для нормального функционирования животных клеток и является основной составляющей клеточных мембран , а также служит субстратом для синтеза стероидных гормонов и желчных кислот.
Главный липидный компонент пищевого жира и жировых отложений — это триглицериды, которые представляют собой эфиры глицерина и жирных кислот. Холестерин и триглицериды, будучи неполярными липидными веществами, транспортируются в плазме крови в составе липопротеиновых частиц. Частицы эти подразделяют по размеру, плотности, относительному содержанию холестерина, триглицеридов и белков на пять больших классов: хиломикроны, липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП) [2]. Традиционно ЛПНП считается «плохим» холестерином, а ЛПВП — «хорошим» (рис. 1).
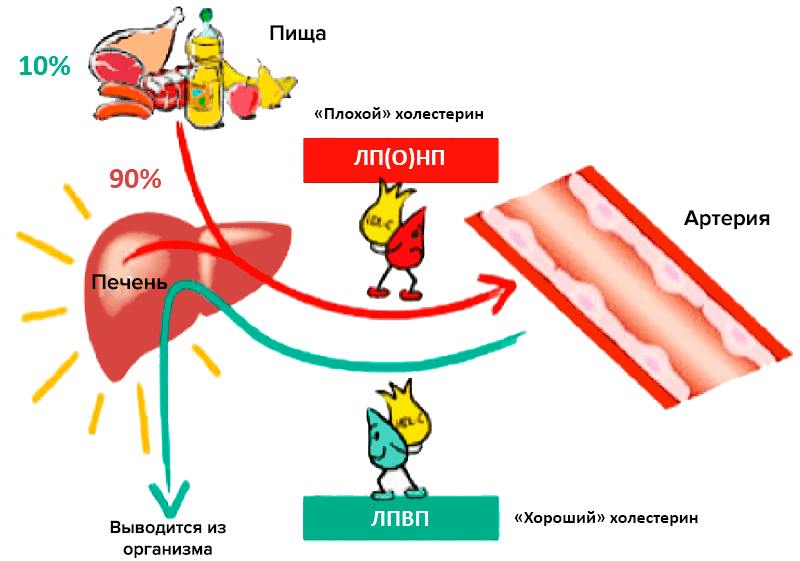
Рисунок 1. «Плохой» и «хороший» холестерины. Участие различных липопротеиновых частиц в транспорте липидов и холестерина.
Схематично структура липопротеина включает неполярное ядро, состоящее по большей части из холестерина и триглицеридов, и оболочку из фосфолипидов и апопротеинов (рис. 2). Ядро — функциональный груз, который доставляется до места назначения. Оболочка же участвует в распознавании клеточными рецепторами липопротеиновых частиц, а также в обмене липидными частями между различными липопротеинами [3].
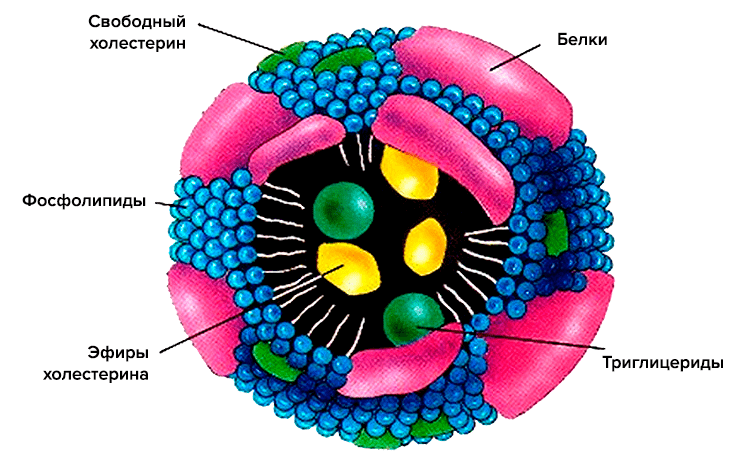
Рисунок 2. Схематическое строение липопротеиновой частицы
Баланс уровня холестерина в организме достигается следующими процессами: внутриклеточный синтез, захват из плазмы (главным образом из ЛПНП), выход из клетки в плазму (главным образом в составе ЛПВП). Предшественник синтеза стероидов — ацетил коэнзим А (CoA). Процесс синтеза включает, по крайней мере, 21 шаг, начиная с последовательного преобразования ацетоацетил CoA. Лимитирующая стадия синтеза холестерина в большой степени определяется количеством холестерина, абсорбируемого в кишечнике и транспортируемого в печень [4]. При недостатке холестерина происходит компенсаторное усиление его захвата и синтеза.
Транспорт холестерина
Систему транспорта липидов можно разделить на две большие части: внешнюю и внутреннюю.
Внешний путь начинается с всасывания в кишечнике холестерина и триглицеридов. Его конечный результат — доставка триглицеридов в жировую ткань и мышцы, а холестерина — в печень. В кишечнике пищевой холестерин и триглицериды связываются с апопротеинами и фосфолипидами, формируя хиломикроны, которые через лимфоток попадают в плазму, мышечную и жировую ткани. Здесь хиломикроны взаимодействуют с липопротеинлипазой — ферментом, который освобождает жирные кислоты. Эти жирные кислоты поступают в жировую и мышечную ткани для накопления и окисления соответственно. После изъятия триглицеридного ядра остаточные хиломикроны содержат большое количество холестерина и апопротеина Е. Апопротеин Е специфически связывается со своим рецептором в клетках печени, после чего остаточный хиломикрон захватывается и катаболизируется в лизосомах. В результате этого процесса освобождается холестерин, который затем преобразуется в желчные кислоты и выводится или участвует в формировании новых липопротеинов, образующихся в печени (ЛПОНП). При нормальных условиях хиломикроны находятся в плазме в течение 1-5 ч. после приема пищи [2], [3].
Внутренний путь. Печень постоянно синтезирует триглицериды, утилизируя свободные жирные кислоты и углеводы. В составе липидного ядра ЛПОНП они выходят в кровь. Внутриклеточный процесс формирования этих частиц схож с таковым для хиломикронов, за исключением различия в апопротеинах. Последующее взаимодействие ЛПОНП с липопротеинлипазой в тканевых капиллярах приводит к формированию остаточных ЛПОНП, богатых холестерином (ЛППП). Примерно половина этих частиц выводится из кровотока клетками печени в течение 2-6 ч. Остальные претерпевают модификацию с замещением оставшихся триглицеридов эфирами холестерина и освобождением от всех апопротеинов, за исключением апопротеина В. В результате формируются ЛПНП, которые содержат ¾ всего плазменного холестерина. Их главная функция — доставка холестерина в клетки надпочечников, скелетных мышц, лимфоцитов, гонад и почек [3]. Модифицированные ЛПНП (окисленные продукты, количество которых возрастает при повышенном содержании в организме активных форм кислорода, так называемом окислительном стрессе) могут распознаваться иммунной системой как нежелательные элементы. Тогда макрофаги их захватывают и выводят из организма в виде ЛПВП. При чрезмерно высоком уровне ЛПНП макрофаги становятся перегруженными липидными частицами и оседают в стенках артерий, образуя атеросклеротические бляшки.
Основные транспортные функции липопротеинов приведены в таблице.
Таблица. Функции липопротеинов [5].
| Класс | Размеры | Функция |
|---|---|---|
| ЛПВП | 4-14 нм | Транспорт холестерина от периферийных тканей к печени |
| ЛПНП | 20-22,5 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| ЛППП | 25-35 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| ЛПОНП | 30-80 нм | Транспорт холестерина, триглицеридов и фосфолипидов от печени к периферийным тканям |
| Хиломикроны | 75-1200 нм | Транспорт холестерина и жирных кислот, поступающих с пищей, из кишечника в периферические ткани и печень |
Регуляция уровня холестерина
Уровень холестерина в крови в большой степени определяется диетой. Пищевые волокна снижают уровень холестерина, а пища животного происхождения повышает его содержание в крови.
Один из основных регуляторов метаболизма холестерина — рецептор LXR (рис. 3). LXR α и β принадлежат к семейству ядерных рецепторов, которые образуют гетеродимеры с ретиноидным Х рецептором и активируют гены-мишени. Их естественные лиганды — оксистерины (окисленные производные холестерина). Обе изоформы идентичны на 80% по аминокислотной последовательности. LXR-α обнаружен в печени, кишечнике, почках, селезенке, жировой ткани; LXR-β в небольшом количестве обнаруживается повсеместно [6]. Метаболический путь оксистеринов быстрее, чем у холестерина, и поэтому их концентрация лучше отражает краткосрочный баланс холестерина в организме. Существует всего три источника оксистеринов: ферментативные реакции, неферментативное окисление холестерина и поступление с пищей. Неферментативные источники оксистеринов как правило минорные, но в патологических состояниях их вклад возрастает (окислительный стресс, атеросклероз), и оксистерины могут действовать наряду с другими продуктами перекисного окисления липидов [6]. Основное влияние LXR на метаболизм холестерина: обратный захват и транспорт в печень, вывод с желчью, снижение кишечного всасывания. Уровень продукции LXR различается на протяжении аорты; в дуге, зоне турбулентности, LXR в 5 раз меньше, чем в участках со стабильным течением. В здоровых артериях повышение экспрессии LXR в зоне сильного потока оказывает антиатерогенное действие [7].
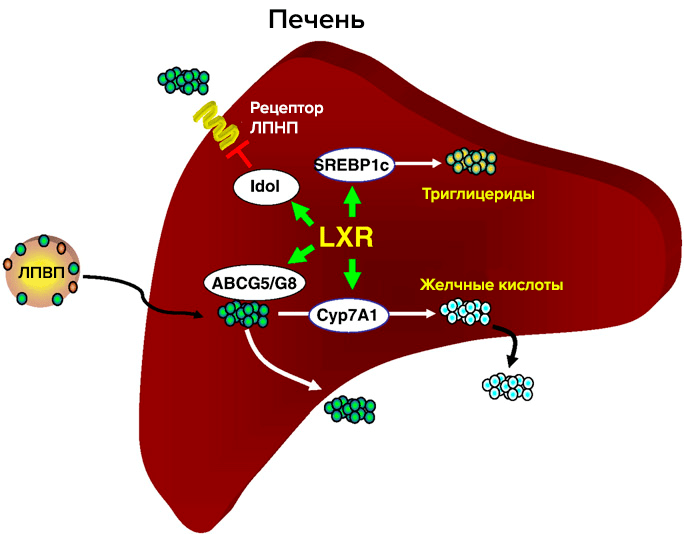
Рисунок 3. Участие рецептора LXR в метаболизме холестерина в печени
Важную роль в метаболизме холестерина и стероидов играет рецептор-«мусорщик» SR-BI (рис. 4). Он был обнаружен в 1996 году как рецептор для ЛПВП [8]. В печени SR-BI отвечает за избирательный захват холестерина из ЛПВП. В надпочечниках SR-BI опосредует избирательный захват этерифицированного холестерина из ЛПВП, который необходим для синтеза глюкокортикоидов. В макрофагах SR-BI связывает холестерин, что является первым этапом в обратном транспорте холестерина. SR-BI также захватывает холестерин из плазмы и опосредует его прямой выход в кишечник [9].
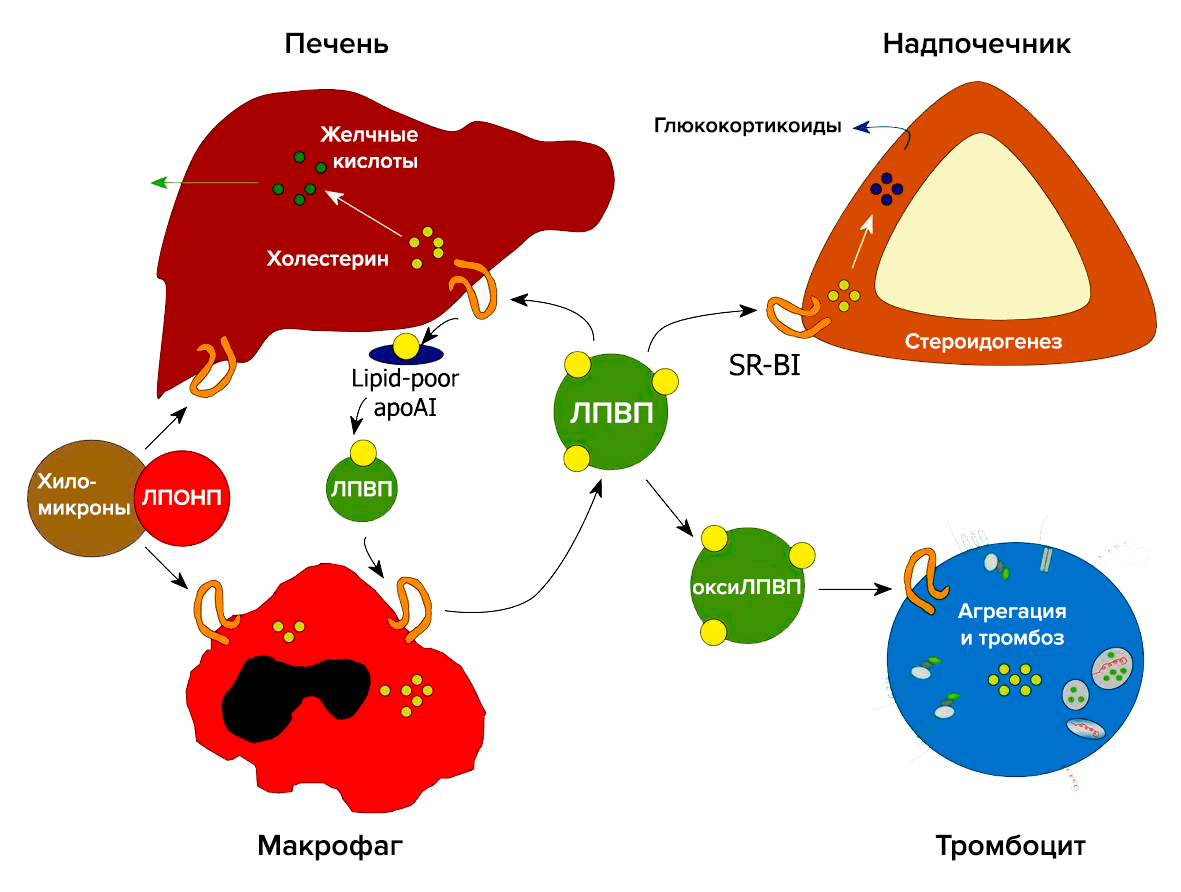
Рисунок 4. Участие рецептора SR-BI в метаболизме холестерина
Выведение холестерина из организма
Классический путь выведения холестерина: транспорт холестерина с периферии в печень (ЛПВП), захват клетками печени (SR-BI), экскреция в желчь и выведение через кишечник, где большая часть холестерина возвращается в кровь [10].
Основная функция ЛПВП — обратный транспорт холестерина в печень. Плазменные ЛПВП являются результатом комплекса различных метаболических событий. Состав ЛПВП очень различается по плотности, физико-химическим свойствам и биологической активности. Это сферические или дисковидные образования. Дисковидные ЛПВП в основном состоят из апопротеина A-I с вложенным слоем фосфолипидов и свободного холестерина. Сферические ЛПВП больше и дополнительно содержат гидрофобное ядро из эфиров холестерина и небольшого количества триглицеридов.
При метаболическом синдроме активируется обмен триглицеридов и эфиров холестерина между ЛПВП и триглицерид-богатыми липопротеинами. В результате содержание триглицеридов в ЛПВП повышается, а холестерина снижается (т.е. холестерин не выводится из организма) [11]. Отсутствие ЛПВП у людей встречается при болезни Tangier, главные клинические проявления которой — увеличенные оранжевые миндалины, роговичная дуга, инфильтрация костного мозга и мукозного слоя кишечника [3].
Если коротко обобщить, то страшен не сам холестерин, который является необходимым компонентом, обеспечивающим нормальную структуру клеточных мембран и транспорт липидов в крови, а кроме того он является сырьем для производства стероидных гормонов. Метаболические расстройства же проявляются при нарушении баланса ЛПНП и ЛПВП , что отражает нарушение системы транспорта липопротеинов, включающей работу печени, образование желчи и участие макрофагов. Поэтому любые заболевания печени, а также аутоиммунные процессы могут вызвать развитие атеросклероза даже при вегетарианской диете. Если мы вернемся к изначальным опытам Н.А. Аничкова по кормлению кроликов пищей, богатой холестерином, то увидим, что холестерин не встречается в естественном рационе кроликов и поэтому, как яд, нарушает работу печени, вызывает сильное воспаление сосудов и, как следствие, образование бляшек.
- Anitschkow N. and Chalatow S. (1983). Classics in arteriosclerosis re: On experimental cholesterin steatosis and its ificance in the origin of some pathological processes by N. Anitschkow and S. Chalatow, translated by Mary Z. Pelias, 1913. Arteriosclerosis, Thrombosis, and Vascular Biology. 3, 178-182;
- Климов А.Н. Причины и условия развития атеросклероза. Превентивная кардиология. М.: «Медицина», 1977. — 260-321 с.;
- Cox R.A. and Garcia-Palmieri M.R. Cholesterol, triglycerides, and associated lipoproteins. Clinical methods: the history, physical, and laboratory examinations (3rd Edition). Boston: Butter-worths, 1990. — 153-160 p.;
- Grundy S.M. (1978). Cholesterol bolism in man. West. J. Med. 128, 13-25;
- Википедия: «Липопротеины»;
- Wójcicka G., Jamroz-Wisniewska A., Horoszewicz K., Beltowski J. (2007). Liver X receptors (LXRs). Part I: Structure, , regulation of activity, and role in lipid bolism. Postepy Hig. Med. Dosw. 61, 736-759;
- Calkin A. and Tontonoz P. (2010). Liver X Receptor aling pathways and atherosclerosis. Arterioscler. Thromb. Vasc. Biol. 30, 1513-1518;
- S. Acton, A. Rigotti, K. T. Landschulz, S. Xu, H. H. Hobbs, M. Krieger. (1996). Identification of Scavenger Receptor SR-BI as a High Density Lipoprotein Receptor. Science. 271, 518-520;
- Vrins C.L.J. (2010). From blood to gut: Direct secretion of cholesterol via transintestinal cholesterol efflux. World J. Gastroenterol. 16, 5953-5957;
- Van der Velde A.E. (2010). Reverse cholesterol transport: From classical view to new insights. World J. Gastroenterol. 16, 5908-5915;
- Wilfried Le Goff, Maryse Guerin, M.John Chapman. (2004). Pharmacological modulation of cholesteryl ester transfer protein, a new therapeutic target in atherogenic dyslipidemia. Pharmacology & Therapeutics. 101, 17-38;
- Липидный фундамент жизни;
- Наночастицами — по «плохому» холестерину!.
Источник
Холестерин в организме: нормы для разного возраста

Это органическое жироподобное вещество выполняет множество важных функций. Без него невозможен синтез гормонов, усвоение большинства витаминов, образование желчных кислот, кроветворение. Большая часть холестерина вырабатывается внутри организма, около 20% поступает извне, с пищей. Повышение уровня этого соединения чревато развитием атеросклероза и других болезней. Излишки холестерина заполняют просвет сосудов, оседают в желчном пузыре в виде камней.
Содержание:
Что такое хороший и плохой холестерин
Измерение уровня холестерина: общие нормы
Изменение норма холестерина по возрасту у женщин
Изменение уровня холестерина по годам у мужчин
Способы поддержания нормального уровня холестерина
Что такое хороший и плохой холестерин
В тканях и крови холестерин образует особые комплексы с группами белков-липопротеидов. Они обеспечивают его стабильно взвешенное состояние. Одни из них имеют высокую плотность, другие — низкую. Эти свойства липопротеидов определяют типы холестерина:
«хороший»: ЛПВС, защищает клетки от повреждений, обеспечивает нормальную текучесть крови, эластичность сосудов;
«плохой»: ЛПНП, склонен к выпадению в осадок, формирует атеросклеротические бляшки.
Именно низкоплотный холестерин имеют в виду, когда говорят о его вреде для здоровья. Это справедливо, так как его излишек прямо связан с сердечно-сосудистыми заболеваниями, сахарным диабетом, нарушением кровообращения и риском инсультов. ЛПНП способствует накоплению триглицеридов — простых жирных кислот, перегружает печень, способствует развитию желчекаменной болезни. Холестерин высокой плотности тормозит эти патологические процессы, частично нейтрализует действие «плохого».
Измерение уровня холестерина: общие нормы
Для определения уровня холестерина в крови применяют специальную единицу: миллимоль (ммоль). Подсчитывают количество ммоль на 1 л биологической жидкости. Значение имеет общее содержание холестерина, а также концентрация ЛПВС и ЛПНП по отдельности. Важен также уровень триглицеридов в крови, по которому судят о риске атеросклеротических изменений в организме, нарушениях жирового обмена и работы печени.
Нормальный показатель общего холестерина: 3-7,8 ммоль/л. В течение жизни он колеблется в зависимости от возраста и гормонального статуса. Это средняя норма в течение жизни, одинаковая для мужчин и женщин.
Холестерин низкой плотности — «плохой» ЛПНП в идеале должен варьироваться в пределах 1,8-2,8 ммоль/л. Верхняя граница для женщин — до 4,5 ммоль/л. Для мужчин — до 4,8 ммоль/л. Предельный его уровень: 5,7 ммоль/л.
Уровень высокоплотный «хороший» ЛПВС в норме вдвое ниже «плохого»: 0,8-2,4 ммоль/л для женщин и 0,7-1,7 ммоль/л — для мужчин.
Чем выше показатель холестерина низкой плотности, тем критичнее состояние здоровья. Особенно, если уровень хорошего высокоплотного соединения не дотягивает до нормы:
опасно регулярное повышение содержания ЛПНП до 4 и более ммоль/л;
постоянное снижение ЛПВС до 0,7 ммоль/л также сигнализирует о нарушениях в организме.
Триглицериды измеряются так же, как остальные показатели холестерина. Их норма в крови на протяжении жизни: до 2,2 ммоль/л. Она одинакова у мужской и женской половин человечества.
Признаки нарушений:
повышенный уровень триглицеридов: 2,3-5,6 ммоль/л;
опасно высокий, сигнализирующий о заболевании: 5,7 ммоль/л и больше.
Риск развития атеросклероза реален в любом возрасте, но молодые люди больше защищены от него благодаря высокой скорости метаболизма. У них холестерин быстро расходуется на гормоны и другие физиологические процессы. Женщин от отложений жировых бляшек в сосудах защищают эстрогены. Однако при малоподвижном образе жизни, любви к вредным продуктам или наличии системных заболеваний холестерин повышается и у молодежи. С годами уровень его растет ещ е быстрее.
Изменение норм холестерина по возрасту у женщин
Различия в обмене веществ и функционировании систем организма на каждом этапе жизни влияют и на уровень холестерина. С годами из-за замедления метаболизма он неизбежно повышается. Меняющиеся средние показатели общего холестерина для женщин:
до 5 лет: от 2,90 до 5,18 ммоль/л;
5-10 лет: от 2,26 до 5,30 ммоль/л;
10-15 лет: от 3,21 до 5,20 ммоль/л;
15-25 лет: от 3,10-5,5 ммоль/л;
25-35 лет: от 3,37 до 5,96 ммоль/л;
35-40 лет: от 3,63 до 6,27 ммоль/л;
40-50 лет: от 3,81 до 6,53 ммоль/л;
50-60 лет: от 4,45 до 7,77 ммоль/л;
60-70 лет: от 4,45 до 7,69 ммоль/л;
70 и более лет: от 4,48 от 7,25 ммоль/л.
Значительное повышение верхней границы показателей у женщин старше 60 лет объясняется угасанием работы яичников. В этот период возрастает риск ожирения, развития диабета второго типа, сердечно-сосудистых заболеваний, остеопороза.
Изменение уровня холестерина по годам у мужчин
Мужчины от природы защищены от атеросклероза меньше женщин. У них нет высокого уровня эстрогенов в организме, зато выше тяга к вредным привычкам, увеличивающим риск опасных заболеваний.
Нормы общего холестерина у мужчин:
до 5 лет: от 2,95-5,25 ммоль/л;
5-10 лет: от 3,13 до 5,25 ммоль/л;
10-15 лет: от 3,08 до 5,23 ммоль/л;
15-25 лет: от 2,93 до 5,59 ммоль/л;
25-35 лет: от 3,44-6,58 ммоль/л;
35-40 лет: от 3,78-6,99 ммоль/л;
40-50 лет: от 3,91 до 7,15 ммоль/л;
50-60 лет: от 4,09 до 7,17 ммоль/л;
60-70 лет: от 4,12 до 7,15 ммоль/л
70 лет и более: от 3,73 до 7,86 ммоль/л.
Чем ближе уровень холестерина к нижней границе нормы, тем безопаснее он для сосудов и сердца. Регулярные отметки, превышающие 5-6 ммоль/л, сигнализируют о необходимости профилактики атеросклероза. Особенно важно контролировать показатели мужчинам старше 50 лет. С этого возраста их рост ускоряется.
Способы поддержания нормального уровня холестерина
Высокие показатели фиксируются в биохимическом анализе крови. Если цифры регулярно превышают норму, важно пройти медицинское обследование щитовидной, поджелудочной железы, печени, сдать тест на гормональный профиль. Для нормализации жирового обмена назначают курсы противолипидных препаратов.
Лечебная диета с низким содержанием мясных и молочных продуктов также способствует снижению общего холестерина. В пищу полезно включать морскую рыбу, содержащую комплекс Омега-3, оливковое, льняное, подсолнечное масла, свежие овощи, зелень.
Опубликовано: 1 Марта 2021
Автор
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Источник